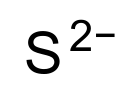 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК Сульфид (2-) (добавка), рекомендуемое название Сульфандиид (заместитель), не часто, редко используется, иногда генерируется автоматическим программным обеспечением номенклатуры в органической химии | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| PubChem CID | |
| UNII | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | S2− |
| Молярная масса | 32,06 г моль -1 |
| Конъюгированная кислота | Бисульфид |
| Родственные соединения | |
| Другие анионы | оксид селенид теллурид |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сульфид ( британский английский и сульфид) является неорганическим анионом из серы с химической формулой S 2- или соединение, содержащее один или более S 2- ионов. Растворы сульфидных солей агрессивны. Сульфид также относится к химическим соединениям большого семейства неорганических и органических соединений, например сульфиду свинца и диметилсульфиду. Сероводород (H 2 S) и бисульфид (SH -) - кислоты, сопряженные с сульфидом.
Сульфид-ион S 2- не существует в водных щелочных растворах Na 2 S. Вместо этого сульфид превращается в гидросульфид:
При обработке кислотой сульфидные соли превращаются в сероводород :
Окисление сульфида - сложный процесс. В зависимости от условий окисление может давать элементарную серу, полисульфиды, политионаты, сульфит или сульфат. Сульфиды металлов реагируют с галогенами с образованием серы и солей металлов.
Водные растворы катионов переходных металлов реагируют с источниками сульфидов (H 2 S, NaHS, Na 2 S) с осаждением твердых сульфидов. Такие неорганические сульфиды обычно имеют очень низкую растворимость в воде, и многие из них относятся к минералам с таким же составом (см. Ниже). Одним из известных примеров является ярко-желтый вид CdS или « желтый кадмий ». Черный налет на стерлинговом серебре - это Ag 2 S. Такие частицы иногда называют солями. Фактически, связь в сульфидах переходных металлов является сильно ковалентной, что обуславливает их полупроводниковые свойства, которые, в свою очередь, связаны с глубокими цветами. Некоторые из них имеют практическое применение в качестве пигментов, солнечных элементов и катализаторов. Гриб Aspergillus niger играет роль в солюбилизации сульфидов тяжелых металлов.
Многие важные металлические руды представляют собой сульфиды. Значительные примеры включают в себя: аргентит ( серебро сульфида), киноварь ( ртуть сульфидных), галенит ( свинец сульфида), молибденит ( молибден сульфида), пентландитовый ( никель - сульфидных), Реальгар ( мышьяк сульфид), и антимонит ( сурьма ), сфалерит ( цинк сульфида) и пирит ( железный дисульфид), и халькопирит ( железо - медь сульфид).
Растворенные свободные сульфиды (H 2 S, HS - и S 2-) являются очень агрессивными веществами для коррозии многих металлов, таких как сталь, нержавеющая сталь и медь. Сульфиды, присутствующие в водном растворе, ответственны за коррозионное растрескивание стали под напряжением (SCC), которое также известно как сульфидное растрескивание под напряжением. Коррозия является серьезной проблемой во многих промышленных установках, перерабатывающих сульфиды: мельницы по производству сульфидной руды, глубокие нефтяные скважины, трубопроводы, транспортирующие закисленную нефть, фабрики по производству крафт-бумаги.
Микробиологическая коррозия (MIC) или биогенная сульфидная коррозия также вызываются сульфатредуцирующими бактериями, производящими сульфид, который выделяется в воздух и окисляется в серной кислоте сероокисляющими бактериями. Биогенная серная кислота вступает в реакцию с канализационными материалами и, как правило, вызывает потерю массы, растрескивание канализационных труб и, в конечном итоге, обрушение конструкции. Такое ухудшение состояния является серьезным процессом, влияющим на канализационные системы во всем мире и приводящим к очень высоким затратам на восстановление.
Окисление сульфида также может образовывать тиосульфат ( S 2О2- 3) промежуточный компонент, ответственный за серьезные проблемы точечной коррозии стали и нержавеющей стали, в то время как среда также подкисляется за счет производства серной кислоты, когда окисление более продвинуто.
В органической химии «сульфид» обычно относится к связи C – S – C, хотя термин тиоэфир менее неоднозначен. Например, диметилсульфид тиоэфира представляет собой CH 3 –S – CH 3. Полифениленсульфид (см. Ниже) имеет эмпирическую формулу C 6 H 4 S. Иногда термин сульфид относится к молекулам, содержащим функциональную группу –SH. Например, метилсульфид может означать CH 3 –SH. Предпочтительным дескриптором для таких SH-содержащих соединений является тиол или меркаптан, то есть метантиол или метилмеркаптан.
Путаница возникает из-за разных значений термина « дисульфид ». Дисульфид молибдена (MoS 2) состоит из отдельных сульфидных центров в ассоциации с молибденом в формальной степени окисления +4 (то есть Mo 4+ и два S 2-). Дисульфид железа ( пирит, FeS 2), с другой стороны, состоит из S2- 2или - S – S - дианион в ассоциации с двухвалентным железом в формальной степени окисления +2 (ион двухвалентного железа: Fe 2+). Диметилдисульфид имеет химическое связывание CH 3 –S – S – CH 3, тогда как сероуглерод не имеет связи S – S, будучи S = C = S (аналог линейной молекулы CO 2). Чаще всего в химии серы и в биохимии термин дисульфид обычно приписывается серному аналогу пероксидной связи –O – O–. Дисульфид связь (-S-S-) играет главную роль в конформации белков, а в каталитической активности ферментов.
| Формула | Точка плавления (° C) | Точка кипения (° C) | Количество CAS | |
|---|---|---|---|---|
| H 2 S | Сероводород - очень токсичный и едкий газ, с характерным запахом «тухлого яйца». | -85,7 | −60,20 | 7783-06-4 |
| CdS | Сульфид кадмия можно использовать в фотоэлементах. | 1750 г. | 1306-23-6 | |
| Полисульфид кальция (« известковая сера ») - традиционный фунгицид в садоводстве. | ||||
| CS 2 | Сероуглерод является предшественником сероорганических соединений. | −111,6 | 46 | 75-15-0 |
| PbS | Сульфид свинца используется в инфракрасных датчиках. | 1114 | 1314-87-0 | |
| МоС 2 | Дисульфид молибдена, минерал молибденит, используется в качестве катализатора для удаления серы из ископаемого топлива; также как смазка для применения в условиях высоких температур и высокого давления. | 1317-33-5 | ||
| Cl – CH 2 CH 2 –S – CH 2 CH 2 –Cl | Серный иприт (горчичный газ) - это сероорганическое соединение (тиоэфир), которое использовалось в качестве химического оружия во время Первой мировой войны. | 13–14 | 217 | 505-60-2 |
| Ag 2 S | Сульфид серебра является компонентом потускнения серебра. | 21548-73-2 | ||
| Na 2 S | Сульфид натрия в виде гидрата используется в производстве крафт- бумаги и в качестве предшественника сероорганических соединений. | 920 | 1180 | 1313-82-2 |
| ZnS | Сульфид цинка используется для изготовления линз и других оптических устройств в инфракрасной части спектра. ZnS, легированный серебром, используется в альфа-детекторах, в то время как сульфид цинка со следами меди находит применение в фотолюминесцентных полосах для аварийного освещения и светящихся циферблатах часов. | 1185 | 1314-98-3 | |
| C 6 H 4 S | Полифениленсульфид - это полимер, обычно называемый «сульфар». Его повторяющиеся звенья связаны вместе сульфидными (тиоэфирными) связями. | 26125-40-6 25212-74-2 | ||
| SeS 2 | Дисульфид селена - это противогрибковое средство, используемое в препаратах против перхоти, таких как Selsun Blue. Присутствие высокотоксичного селена в продуктах здравоохранения и косметики представляет собой общую проблему для здоровья и окружающей среды. | lt;100 | 7488-56-4 | |
| FeS 2 | Пирит, известный как «золото дураков», является обычным минералом. | 600 | 1317-66-4 |
Сульфидные соединения можно получить несколькими способами:
Многие сульфиды металлов настолько нерастворимы в воде, что, вероятно, не очень токсичны. Некоторые сульфиды металлов при воздействии сильной минеральной кислоты, в том числе желудочной кислоты, выделяют токсичный сероводород.
Органические сульфиды легко воспламеняются. При сгорании сульфида образуется газообразный диоксид серы (SO 2).
Сероводород, некоторые его соли и почти все органические сульфиды имеют сильный гнилостный запах; гниющая биомасса высвобождает их.
Систематические названия сульфандиид и сульфид (2-), действительные названия IUPAC, определяются согласно заместительной и аддитивной номенклатуре, соответственно. Однако название сульфид также используется в номенклатуре композиций ИЮПАК, которая не принимает во внимание природу вовлеченного связывания. Примеры такого наименования включают дисульфид селена и сульфид титана, которые не содержат сульфид-ионы.