 | |||
| |||
 | |||
| Названия | |||
|---|---|---|---|
| Название IUPAC Гидрокарбонат натрия | |||
| Другие названия Пищевая сода, бикарбонат (лабораторный сленг), бикарбонат соды, нахколит | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 4153970 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.122 | ||
| Номер ЕС |
| ||
| Номер E | E500 (ii) (регуляторы кислотности,...) | ||
| IUPHAR / BPS | |||
| KEGG | |||
| MeSH | Натрий + бикарбонат | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | NaHCO. 3 | ||
| Молярная масса | 84,0066 г / моль | ||
| Внешний вид | Белые кристаллы | ||
| Запах | Без запаха | ||
| Плотность |
| ||
| Температура плавления | (Разлагается до натрия карбонат начиная с 50 ° C) | ||
| Растворимость в воде |
| ||
| Растворимость | 0,02 мас.% ацетона, 2,13 мас.% метанола при 22 ° C. не растворим в этаноле | ||
| log P | -0,82 | ||
| Кислотность (pKa) |
| ||
| Показатель преломления (nD) | nα = 1,377 nβ = 1,501 nγ = 1,583 | ||
| Структура | |||
| Кристаллическая структура | Моноклинная | ||
| Термохимия | |||
| Теплоемкость (C) | 87,6 Дж / моль K | ||
| Стандартный молярный. энтропия (S 298) | 101,7 Дж / моль K | ||
| Стандартная энтальпия. образования (ΔfH298) | -950,8 кДж / моль | ||
| свободная энергия Гиббса (ΔfG˚) | -851,0 кДж / моль | ||
| Фармакология | |||
| Код ATC | B05CB04 (WHO ) B05XA02 (WHO ), QG04BQ01 (ВОЗ ) | ||
| Пути. введения | Внутривенно, перорально | ||
| Опасности | |||
| Основные опасности | Вызывает серьезное раздражение глаз | ||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| NFPA 704 (огненный алмаз) |  0 2 1 0 2 1 | ||
| Температура вспышки | Негорючий | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LD50(средняя доза ) | 4220 мг / кг (крыса, перорально) | ||
| Родственные соединения | |||
| Другие анионы | Карбонат натрия | ||
| Другие катионы | |||
| Родственные соединения | |||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
 Кексы, запеченные с пищевой содой в качестве разрыхлителя
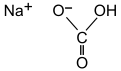
Кексы, запеченные с пищевой содой в качестве разрыхлителя Бикарбонат натрия (название ИЮПАК : гидрокарбонат натрия ), широко известный как пищевая сода (особенно в Северной Америке и Новой Зеландии ) или бикарбонат натрия, представляет собой химическое соединение с формулой NaHCO 3. Это соль, состоящая из катиона натрия (Na ) и бикарбонатного аниона (HCO 3 ). Бикарбонат натрия представляет собой белое твердое вещество, кристаллическое, но часто выглядит как мелкий порошок. Он имеет слегка соленый, щелочной вкус, напоминающий вкус стиральной соды (карбонат натрия ). Природная минеральная форма - нахколит. Он входит в состав минерала натрон и растворен во многих минеральных источниках.
Потому что это давно известно и широко используется, соль имеет много родственных названий, таких как пищевая сода, пищевая сода, пищевая сода и бикарбонат соды . Термин пищевая сода более распространен в Соединенных Штатах, тогда как бикарбонат соды более распространен в Австралии и Великобритании. В разговорной речи названия бикарбонат натрия и бикарбонат соды часто сокращаются; распространены такие формы, как бикарбонат натрия, бикарбонат натрия, бикарбонат и бикарбонат.
Слово saleratus, от латинского sal æratus (что означает «газированная соль»), широко использовалось в 19 век как для бикарбоната натрия, так и для бикарбоната калия.
Он известен как одна из E number пищевых добавок E500 .
Приставка bi в бикарбонате от устаревшей системы именования и основывается на наблюдении, что на один натрий в бикарбонате натрия (NaHCO 3) содержится вдвое больше карбоната (CO 3), чем присутствует в карбонате натрия (Na 2CO3). Современные химические формулы этих соединений выражают их точный химический состав (который был неизвестен, когда были придуманы названия карбонат натрия и бикарбонат натрия) как гидрокарбонат натрия (NaHCO 3) и карбонат натрия (Na 2CO3).. Эти названия однозначны, поскольку натрий всегда имеет степень окисления +1 , а карбонат - степень окисления -2.
В кулинарии пищевая сода в основном используется в выпечке как разрыхлитель. Когда он вступает в реакцию с кислотой, выделяется углекислый газ, который вызывает расширение жидкого теста и формирует характерную текстуру и зерно в пирогах, быстром хлебе, содовом хлебе и других выпеченных и жареных продукты. Кислотно-основная реакция может быть в общих чертах представлена следующим образом:
Кислотные материалы, которые вызывают эту реакцию, включают гидрофосфаты, винный камень, лимонный сок, йогурт, пахта, какао, и уксус. Пищевая сода может использоваться вместе с закваской, которая является кислой, что позволяет получить более легкий продукт с менее кислым вкусом.
Тепло также само по себе может заставить бикарбонат натрия действовать как разрыхлитель в выпекание из-за термического разложения с выделением диоксида углерода при температурах выше 80 ° C (180 ° F) следующим образом:
При использовании таким способом самостоятельно, без присутствия кислотного компонента (будь то тесто или разрыхлитель, содержащий кислоту), только половина доступного CO 2 (одна молекула CO 2 образуется на каждые два эквивалента NaHCO 3). Кроме того, в отсутствие кислоты термическое разложение бикарбоната натрия также дает карбонат натрия, который является сильно щелочным и придает выпеченному продукту горький, «мыльный» вкус и желтый цвет. Поскольку реакция протекает медленно при комнатной температуре, смеси (тесто для пирогов и т. Д.) Можно выдерживать, не поднимаясь, пока они не нагреются в духовке.
При добавлении кислоты, щелочных ингредиентов, таких как цельное молоко или Обработанное голландцами какао часто добавляют в выпечку, чтобы избежать чрезмерно кислого привкуса из-за добавленной кислоты.
Разрыхлитель, также продается для приготовления пищи, содержит около 30% бикарбоната и различные кислотные ингредиенты, которые активируются при добавлении воды без необходимости добавления кислот в среду для приготовления пищи. Многие формы разрыхлителя содержат бикарбонат натрия в сочетании с кислым фосфатом кальция, фосфатом натрия-алюминия или кремом от зубного камня. Пищевая сода щелочная; кислота, используемая в разрыхлителе, избегает металлического привкуса, когда химические изменения во время выпечки создают карбонат натрия.
Бикарбонат натрия иногда использовался при приготовлении зеленых овощей, так как он придает им ярко-зеленый цвет - который был описан как искусственно выглядящий - из-за его реакции с хлорофиллом с образованием хлорофиллина. Однако это имеет тенденцию влиять на вкус, текстуру и содержание питательных веществ и больше не является распространенным явлением.
Пищевая сода используется для смягчения бобовых (горох, фасоль) до и во время приготовления, как в традиционный британский мягкий горох рецепт замачивания гороха. Основным действием бикарбоната натрия является изменение pH раствора для замачивания и воды для приготовления пищи; это смягчает твердую внешнюю оболочку, сокращает время приготовления и может изменить процентное содержание питательных веществ в блюде, его вкус и консистенцию.
Пищевая сода может вступать в реакцию с кислотами в пище, включая витамин C (L-аскорбиновая кислота).
Используется в азиатской и латиноамериканской кухне для смягчения мяса. Он также используется в панировке, например, для жареной пищи, для повышения хрустящей корочки и обеспечения выхода пара, чтобы панировка не сдувалась во время приготовления.
Бикарбонат натрия может быть эффективным способом контроля роста грибков и в США зарегистрирован Агентством по охране окружающей среды как биопестицид.
Бикарбонат натрия можно добавлять в бассейны, спа и садовые пруды для повышения общей щелочности (увеличения pH).
Натрий бикарбонат - один из основных компонентов распространенного фейерверка «черная змея». Эффект вызван термическим разложением, в результате которого образуется углекислый газ с образованием длинного змееподобного пепла в качестве продукта сгорания другого основного компонента, сахарозы.
Он обладает слабыми дезинфицирующими свойствами и может быть эффективным фунгицидом против некоторых организмов. Поскольку пищевая сода впитывает затхлый запах, она стала для продавцов подержанных книг надежным методом уменьшения неприятного запаха в книгах.
Бикарбонат натрия можно использовать для тушите небольшое возгорание жира или электрического тока, бросая его на огонь, поскольку нагревание бикарбоната натрия выделяет углекислый газ. Однако его нельзя применять при пожарах во фритюрницах ; внезапный выброс газа может вызвать разбрызгивание смазки. Бикарбонат натрия используется в огнетушителях BC сухих химикатов в качестве альтернативы более агрессивному диаммонийфосфату в огнетушителях ABC. Щелочная природа бикарбоната натрия делает его единственным сухим химическим агентом, помимо Purple-K, который использовался в крупномасштабных системах пожаротушения, установленных на коммерческих кухнях. Поскольку он может действовать как щелочь, агент оказывает умеренное омыление горячей смазки, которое образует удушающую мыльную пену.
Бикарбонат натрия самопроизвольно реагирует с кислотами, выделяя газ CO 2 в качестве продукта реакции. Он обычно используется для нейтрализации нежелательных кислотных растворов или разливов кислоты в химических лабораториях. Нецелесообразно использовать бикарбонат натрия для нейтрализации основания, даже если он амфотерный, реагирующий как с кислотами, так и с основаниями.
Бикарбонат натрия, смешанный с воду можно использовать в качестве антацида для лечения кислотного несварения и изжоги. Его реакция с желудочной кислотой дает соль, воду и двуокись углерода :
Смесь бикарбоната натрия и полиэтиленгликоля, такого как PegLyte, растворенная в воде и принимаемая перорально, является эффективным препаратом для промывания желудочно-кишечного тракта и слабительное перед операцией на желудочно-кишечном тракте, гастроскопией и т. Д.
внутривенное введение бикарбоната натрия в водном растворе иногда используется в случаях ацидоза или при недостаточном количестве ионов натрия или бикарбоната в крови. В случае респираторного ацидоза введенный ион бикарбоната сдвигает углекислотный / бикарбонатный буфер плазмы влево и, таким образом, повышает pH. По этой причине бикарбонат натрия используется в сердечно-легочной реанимации под медицинским наблюдением. Инфузия бикарбоната показана только в том случае, если pH крови заметно низок (< 7.1–7.0).
HCO 3 используется для лечения гиперкалиемии, так как он будет возвращать K обратно в клетки в периоды ацидоза..Поскольку бикарбонат натрия может вызвать алкалоз, его иногда используют для лечения передозировки аспирина. Для правильного всасывания аспирина требуется кислая среда, а щелочная среда снижает абсорбцию аспирина в случае передозировки. Бикарбонат натрия также оказывает использовался при лечении передозировки трициклическим антидепрессантом. Его также можно применять местно в виде пасты, с тремя частями пищевой соды на одну часть воды, для облегчения некоторых видов укусов и укусов насекомых (а также сопутствующих
Некоторые практикующие альтернативные методы, такие как Туллио Симончини, продвигали пищевую соду как лекарство от рака, от чего Американское онкологическое общество предостерегало из-за обоих его недоказанная эффективность и потенциальная опасность в использовании. Эдзард Эрнс назвал продвижение бикарбоната натрия в качестве лекарства от рака «одной из самых отвратительных альтернативных схем, которые я видел в течение долгого времени».
Бикарбонат натрия можно добавлять к местным анестетикам, чтобы ускорить наступление эффекта и сделать инъекцию менее болезненной. Он также является компонентом раствора Моффетта, используемого в назальной хирургии.
Было высказано предположение, что кислая диета ослабляет кости. Один систематический мета-анализ исследования не показывает такого эффекта. Другой также считает, что нет доказательств того, что щелочная диета улучшает здоровье костей, но предполагает, что щелочная диета «может иметь некоторую ценность» по другим причинам.
Растворы антацидов (например, пищевой соды) были приготовлены и используется протестующими для смягчения последствий воздействия слезоточивого газа во время протестов.
Подобно его использованию в выпечке, бикарбонат натрия используется вместе с мягкой кислотой, такой как винная кислота, в качестве вспомогательного вещества. в шипучих таблетках: когда такую таблетку бросают в стакан с водой, карбонат покидает реакционную среду в виде газообразного диоксида углерода (HCO 3 + H → H 2 O + CO 2 ↑ или, точнее, HCO 3 + H 3 O → 2 H 2 O + CO 2 ↑), оставляя лекарство растворенным в воде вместе с образовавшейся солью (в данном примере тартратом натрия).
Зубная паста, содержащая бикарбонат натрия, в нескольких исследованиях показала, что лучшее отбеливание и налет Эффект удаления, чем зубные пасты без него.
Бикарбонат натрия также используется в качестве ингредиента в некоторых жидкостях для полоскания рта. Обладает противокариесными и абразивными свойствами. Он действует как механическое очищающее средство для зубов и десен, нейтрализует выработку кислоты во рту, а также действует как антисептик для предотвращения инфекций. Бикарбонат натрия в сочетании с другими ингредиентами можно использовать для приготовления сухого или влажного дезодоранта. Бикарбонат натрия можно использовать в качестве буферного агента в сочетании с поваренной солью при создании раствора для орошения носа.
. Он используется в гигиене глаз для лечения блефарита. Это делается путем добавления чайной ложки бикарбоната натрия в прохладную воду, которая была недавно кипячена, с последующей осторожной очисткой основания ресниц ватным тампоном, смоченным в растворе.
Бикарбонат натрия используется в качестве добавки к корму для крупного рогатого скота, в частности в качестве буферного агента для рубца.
Хотя небольшие дозы бикарбоната натрия использовались в качестве добавка для спортсменов в соревнованиях на скорость, таких как бег на средние дистанции, доказательств ее пользы недостаточно, а передозировка представляет собой риск для здоровья, поскольку бикарбонат натрия может вызвать раздражение желудочно-кишечного тракта.
Бикарбонат натрия используется в процессе удаления краски и коррозии, называемом гидробластинг. В качестве абразивной среды бикарбонат натрия используется для удаления поверхностных загрязнений с более мягких и менее эластичных субстратов, таких как алюминий, медь или дерево, которые могут быть повреждены абразивным материалом из кварцевого песка.
A производитель рекомендует пасту из пищевой соды с минимальным количеством воды в качестве мягкого чистящего порошка, которая полезна для удаления поверхностной ржавчины, так как ржавчина образует водорастворимое соединение в концентрированном щелочном растворе; следует использовать холодную воду, так как растворы горячей воды могут вызвать коррозию стали. Бикарбонат натрия разрушает тонкий защитный оксидный слой, который образуется на алюминии, что делает его непригодным для очистки этого металла. Раствор в теплой воде удалит налет с серебра при контакте серебра с куском алюминиевой фольги. Пищевая сода обычно добавляется в стиральные машины в качестве замены смягчителя воды и для удаления запахов с одежды. Он также эффективен для удаления тяжелых пятен от чая и кофе с чашек при разбавлении теплой водой.
Во время Манхэттенского проекта по разработке ядерной бомбы в начале 1940-х годов химическая токсичность урана была проблемой. Было обнаружено, что оксиды урана очень хорошо прилипают к хлопковой ткани и не смываются мылом или стиральным порошком. Однако уран вымывается 2% -ным раствором бикарбоната натрия. Одежда может быть загрязнена токсичной пылью обедненного урана (DU), которая очень плотная и поэтому используется в качестве противовесов в гражданском контексте и в бронебойных снарядах. DU не удаляется обычной стиркой; промывка примерно 6 унциями (170 г) пищевой соды в 2 галлонах (7,5 л) воды поможет вымыть ее.
Часто утверждают, что пищевая сода неэффективна. эффективное средство для удаления запаха, и часто рекомендуется хранить открытую коробку в холодильнике для поглощения запаха. Эту идею продвигал ведущий американский бренд пищевой соды Arm Hammer в рекламной кампании, начавшейся в 1972 году. Хотя эта кампания считается классикой маркетинга, ведущей в более чем в половине американских холодильников, содержащих коробку пищевой соды, мало доказательств того, что он действительно эффективен в этом приложении.
Бикарбонат натрия - это амфотерный соединение. Водные растворы являются умеренно щелочными из-за образования угольной кислоты и иона гидроксида :
Бикарбонат натрия можно использовать в качестве промывки для удаления любых кислотных примесей из «сырой» жидкости, что позволяет получить более чистый образец. Взаимодействие бикарбоната натрия и кислоты дает соль и угольную кислоту, которая легко разлагается до диоксида углерода и воды:
Бикарбонат натрия реагирует с уксусной кислотой (обнаруженной в уксусе ), образуя ацетат натрия, вода и диоксид углерода :
Бикарбонат натрия реагирует с основаниями, такими как гидроксид натрия, с образованием карбонатов:
При температурах 80–100 ° C (176–212 ° F) бикарбонат натрия постепенно разлагается на карбонат натрия, воду и углерод. диоксид. Преобразование происходит быстрее при 200 ° C (392 ° F):
Большинство бикарбонатов подвергаются этому реакция дегидратации. Дальнейшее нагревание превращает карбонат в оксид (выше 850 ° C / 1560 ° F):
Эти преобразования актуальны для использования NaHCO 3 в качестве огнетушащего вещества («порошок BC») в некоторых порошковых огнетушителях.
В 1791 году французский химик Николя Леблан производил карбонат натрия, также известный как кальцинированная сода. В 1846 году два американских пекаря, Джон Дуайт и Остин Черч, основали первый в США завод по производству пищевой соды из карбоната натрия и диоксида углерода.
Saleratus., бикарбонат калия или натрия, упоминается в романе Captains Courageous Редьярда Киплинга как широко используемый в 1800-х годах в коммерческом рыболовстве для предотвращения порчи только что пойманной рыбы.
В 1919 году сенатор США заявил, что бикарбонат соды может вылечить испанский грипп... В разгар дебатов 26 января 1919 года сенатор Оверман прервал дискуссию, чтобы объявить об открытии лекарства. «Я хочу сказать для тех, кто проводит это расследование, - сообщил он, - что мне сказал судья вышестоящего суда в горной стране Северной Каролины, что они открыли лекарство от этой болезни». Предполагаемое лекарство предполагало критику современной науки и признание простой мудрости простых людей. «Они говорят, что обычная пищевая сода вылечит болезнь, - продолжил он, - что они вылечили ее с ее помощью, что у них вообще нет смертей; они используют обычную пищевую соду, которая лечит болезнь». - Американская пандемия: затерянные миры эпидемии гриппа 1918 г., Oxford University Press, 15 марта 2012 г., стр. 178
Бикарбонат натрия промышленно производится из карбоната натрия :
Производится в масштабе около 100000 тонн / год (по состоянию на 2001 год). Коммерческие количества пищевой соды также производятся аналогичным способом: кальцинированная сода, добываемая в виде руды трона, растворяется в воде и обрабатывается диоксидом углерода. Бикарбонат натрия выпадает в осадок из этого раствора в виде твердого вещества.
Что касается процесса Сольвея, бикарбонат натрия является промежуточным продуктом в реакции хлорида натрия, аммиака и диоксид углерода. Однако продукт имеет низкую чистоту (75%).
Несмотря на отсутствие практической ценности, NaHCO 3 может быть получен реакцией диоксида углерода с водным раствор гидроксида натрия:
Природные месторождения нахколита (NaHCO 3) обнаружены в эоцене - возраст (55,8–33,9 млн лет назад) Формация Грин-Ривер, Бассейн Писенс в Колорадо. Нахколит отлагался пластами в периоды сильного испарения в бассейне. Он добывается в промышленных масштабах с использованием обычных методов подземной добычи, таких как буровая, барабанная и длинная забойная разработка, аналогично добыче угля.
Ограниченное количество продукта дополнительно получают путем добычи раствора, прокачивая нагретую воду через ранее добытые слои нахколита и восстановление растворенного нахколита над землей в процессе кристаллизации при естественном охлаждении. В настоящее время только компания Genesis Alkali (ранее Tronox, ранее FMC) в бассейне Грин-Ривер, штат Вайоминг, успешно добыла продукт в коммерческих растворах.
Бикарбонат натрия, как «гидрокарбонат соды», был частым источником изюминки для Граучо Маркса в фильмах братьев Маркс. В Утиный суп Маркс играет лидера нации, находящейся в состоянии войны. В одной из сцен он получает сообщение с поля боя, что его генерал сообщает о газовой атаке, и Граучо говорит своему помощнику: «Скажите ему, чтобы он выпил чайную ложку соды и полстакана воды». В Ночь в Опере персонаж Граучо обращается к толпе на открытии оперы, говоря о ведущем теноре: «Синьор Ласспарри происходит из очень известной семьи. Его мать была известной бас-певицей. Его отец был первым человеком, который заправил спагетти бикарбонатом соды, тем самым вызвав и вылечив одновременно несварение желудка ».
| На Викискладе есть медиафайлы по теме Бикарбонат натрия. |
| Викиучебник Поваренная книга содержит рецепт / модуль по |