 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | |
| Торговые наименования | Fareston, другие |
| Другие названия | (Z) -Торемифен; 4-хлоротамоксифен; 4-КТ; Акаподен; CCRIS-8745; FC-1157; FC-1157a; GTx-006; НК-622; NSC-613680 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a608003 |
| Данные лицензии | |
| Способы введения. | Внутрь |
| Класс препарата | Селективный модулятор рецепторов эстрогена |
| Код АТС | |
| Фармакокинетические данные данные | |
| Биодоступность | Хорошая |
| Связывание с белками | >99% |
| Метаболизм | Печень (CYP3A4 ) |
| Метаболиты | N-десметилторемифен; 4-гидрокситоремифен; Оспемифен |
| Период полувыведения | Торемифен: 5–6 дней. Метаболиты: 4–21 день |
| Экскреция | Кал : 70% (в виде метаболитов) |
| Идентификаторы | |
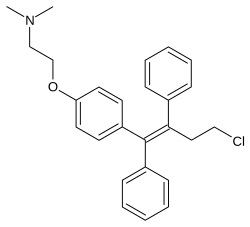
Название ИЮПАК
| |
| Номер CAS |
|
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL <37167>ChEMBL <37167>ChEMBL 357>PDB лига nd | |
| CompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.125.139 |
| Химические и физические данные | |
| Формула | C26H28ClNO |
| Молярная масса | 405,97 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Торемифен, продаваемый, среди прочего, под торговой маркой Фарестон, является лекарством, которое используется в лечение распространенного рака груди у женщин в постменопаузе. Его принимают внутрь.
Побочные эффекты торемифена включают приливы, потливость, тошноту, рвоту, головокружение, выделения из влагалища и вагинальное кровотечение. Он также может вызывать сгустки крови, нерегулярное сердцебиение, катаракту, нарушения зрения, повышение ферментов печени, гиперплазия эндометрия и рак эндометрия. Высокий уровень кальция в крови может наблюдаться у женщин с метастазами в кости.
Лекарство представляет собой селективный эстроген модулятор рецептора (SERM) и, следовательно, является смешанным агонистом - антагонистом рецептора эстрогена (ER), биологической мишени эстрогенов, таких как эстрадиол. Он оказывает эстрогенное действие на кости, печень, а также матку и антиэстрогенные эффекты в грудь. Это производное трифенилэтилена и тесно связано с тамоксифеном.
. Торемифен был представлен для медицинского применения в 1997 году. Это был первый антиэстроген, который вводится с момента появления тамоксифена в 1978 году. Он доступен как непатентованный препарат в США.
Торемифен одобрен для лечения метастатического рака груди у женщин в постменопаузе с рецептор-положительными эстрогенами или опухолями с неизвестным статусом . Это единственное разрешенное использование в США. Он показывает эффективность, эквивалентную тамоксифену по этому показанию. Было обнаружено, что торемифен эффективен при лечении боли в груди и может быть более эффективным лекарством, чем тамоксифен при этом показании. Он также имеет превосходные эффекты на минеральную плотность кости и липидный профиль, включая уровни холестерина и триглицеридов, по сравнению с тамоксифеном. Сообщалось, что торемифен значительно облегчает симптомы гинекомастии у мужчин.
Торемифен предоставляется в форме 60 мг перорально таблетки.
Побочные эффекты торемифена аналогичны таковым тамоксифена. Наиболее частый побочный эффект - приливы. Другие побочные эффекты включают потливость, тошноту, рвоту, головокружение, выделения из влагалища и вагинальные выделения. кровотечение. У женщин с метастазами в кости может возникнуть гиперкальциемия. Торемифен имеет небольшой риск тромбоэмболических событий. Сообщалось о катаракте, изменении зрения и повышении уровня ферментов печени. Препарат удлиняет интервал QT и, следовательно, имеет риск потенциально смертельных аритмий. Риск аритмий можно снизить, отказавшись от применения у пациентов с гипокалиемией, гипомагниемией, уже существующим удлинением интервала QT и у пациентов, принимающих другие препараты, удлиняющие интервал QT. Поскольку торемифен оказывает эстрогенное действие в матке, он может увеличить риск гиперплазии эндометрия и рака эндометрия.
Торемифен кажется более безопасным, чем тамоксифен. Он имеет более низкий риск венозной тромбоэмболии (VTE) (например, легочной эмболии ), инсульта и катаракты. Более низкий риск ВТЭ может быть связан с тем, что тамоксифен снижает уровень антитромбина III в значительно большей степени, чем торемифен в дозе 60 или 200 мг / день.
Торемифен является субстратом CYP3A4, ферментом цитохрома P450 и, следовательно, лекарствами, которые индуцируют или ингибировать этот фермент может соответственно уменьшать или увеличивать уровни торемифена в организме.
Торемифен является селективным рецептором эстрогена модулятор (SERM). То есть, это селективный смешанный агонист-антагонист рецепторов эстрогена (ER), с эстрогенным действием в некоторых ткани и антиэстрогенное действие на другие ткани. Торемифен имеет сходные сродства к ER, как тамоксифен и ралоксифен, показывая константу ингибирования (Ki) значения 20,3 ± 0,1 нМ для ERα и 15,4 ± 3,1 нМ для ERβ. Препарат оказывает эстрогенное действие на кости, частичное эстрогенное действие на матку и печень, а также антиэстрогенное действие на груди..
Торемифен очень похож на тамоксифен и разделяет большинство его свойств. Есть некоторые признаки того, что торемифен может быть более безопасным, чем тамоксифен, поскольку он не является гепатоканцерогеном у животных и может иметь меньший потенциал генотоксичности. Однако клинические исследования не обнаружили существенных различий между торемифеном и тамоксифеном, в том числе с точки зрения эффективности, переносимости и безопасности, и, следовательно, клинического применения торемифена. был несколько ограничен.
Было обнаружено, что торемифен оказывает антигонадотропный эффект у женщин в постменопаузе, прогонадотропный эффект у мужчин, увеличивает глобулин, связывающий половые гормоны. уровней и для снижения уровней инсулиноподобного фактора роста 1 примерно на 20% у женщин и мужчин в постменопаузе.
Торемифен имеет примерно одну треть активности тамоксифена; то есть 60 мг торемифена примерно эквивалентны 20 мг тамоксифена при лечении рака груди.
| Лекарство | Грудь | Кость | Печень | Матка | Влагалище | Мозг | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Липиды | Коагуляция | SHBG | IGF-1 | Приливы | Гонадотропины | |||||||||
| Эстрадиол | + | + | + | + | + | + | + | + | + | + | ||||
| «Идеальная SERM» | – | + | + | ± | ± | ± | – | + | + | ± | ||||
| Базедоксифен | – | + | + | + | + | ? | – | ± | – | ? | ||||
| Кломифен | – | + | + | ? | + | + | – | ? | – | ± | ||||
| Ласофоксифен | – | + | + | + | ? | ? | ± | ± | – | ? | ||||
| Оспемифен | – | + | + | + | + | + | ± | ± | – | ± | ||||
| Ралоксифен | – | + | + | + | + | + | ± | – | – | ± | ||||
| Тамоксифен | – | + | + | + | + | + | + | – | – | ± | ||||
| Торемифен | – | + | + | + | + | + | + | – | – | ± | ||||
| Эффект: + = эстрогенный / агонистический. ± = Смешанный или нейтральный. - = Антиэстрогенный / антагонистический. Примечание: SERM обычно повышают уровень гонадотропина у мужчин с гипогонадизмом и эугонадой, а также у женщин в пременопаузе (антиэстрогенные), но снижают уровень гонадотропинов у женщин в постменопаузе (эстрогенные). Источники: См. Шаблон. | ||||||||||||||
Биодоступность торемифена точно не определена, но известно, что она хорошая. Препарат более чем на 99% связывается с белками плазмы. Он метаболизируется в печени в первую очередь CYP3A4, а затем подвергается вторичному гидроксилированию. Метаболиты торемифена включают N-десметилторемифен и 4-гидрокситоремифен, и они менее активны, чем сам торемифен. Оспемифен (деаминогидрокситоремифен) также является основным метаболитом торемифена. Торемифен и 4-гидрокситоремифен имеют очень длительный период полувыведения от 5 до 6 дней, в то время как N-десметилторемифен имеет еще более длительный период полувыведения от 6 до 21 дня, а оспемифен имеет период полувыведения. 4 дня. Длительный период полувыведения торемифена и его метаболитов можно отнести к энтерогепатической рециркуляции. Торемифен выводится на 70% с фекалиями в виде метаболитов.
В отличие от тамоксифена торемифен не является пролекарством и не зависит от метаболизма по CYP2D6 для биоактивации ; следовательно, тамоксифен может быть предпочтительнее при CYP2D6 слабых метаболизаторах или у пациентов, принимающих препарат, ингибирующий CYP2D6.
Торемифен, также известный как 4-хлоротамоксифен, представляет собой производное трифенилэтилена и близкий аналог тамоксифена. Он также тесно связан с афимоксифеном (4-гидрокситамоксифен) и спемифеном (дезаминогидрокситоремифеном).
Торемифен был введен в США в 1997 году. Это был первый антиэстроген, представленный в этой стране после тамоксифена в 1978 году.
Торемифен - это генерическое название препарата и его INN и BAN, а торемифен цитрат - это его USAN и JAN, а torémifène - это его DCF.
Торемифен продается почти исключительно под торговой маркой Fareston.
Торемифен широко продается во всем мире и доступен в Соединенных Штатах, Соединенное Королевство, Ирландия, многие другие европейские страны, Южная Африка, Австралия, Новая Зеландия, а еще
Торемифен также оценивался на предмет предотвращения рака простаты и имел предварительную торговую марку Acapodene.
В 2007 году фармацевтическая компания GTx, Inc проводила два различных этапа 3 клинических испытаний ; Во-первых, основная фаза клинических испытаний по лечению серьезных побочных эффектов андрогенной депривационной терапии (ADT) (особенно переломов позвонков / позвоночника и приливов, липидного профиля и гинекомастия ) при распространенном раке простаты, и, во-вторых, ключевое клиническое испытание фазы III по профилактике рака простаты у мужчин с высоким риском с высокой степенью интраэпителиальной неоплазии простаты, или PIN. Результаты этих испытаний ожидаются к первому кварталу 2008 года.
NDA для первой заявки (облегчение побочных эффектов ADT рака простаты) было представлено в феврале 2009 года, а в октябре 2009 года FDA заявило, что им потребуется больше клинических данных. данные, например другое исследование фазы III.
В конечном итоге разработка была прекращена, и торемифен никогда не продавался для лечения осложнений, связанных с ADT или лечением или профилактикой рака простаты.
Торемифен может быть полезен для предотвращения бикалутамид -индуцированная гинекомастия.
Было проведено двойное слепое плацебо-контролируемое рандомизированное трехлетнее клиническое испытание торемифена с выборкой из 1260 человек. мужчины. Средний возраст субъектов составлял 64 года, и у них была диагностирована интраэпителиальная неоплазия предстательной железы высокой степени (HGPIN), которая считается предраковой, хотя Томпсон и Лич считают, что ПИН низкой степени также может считаться предраковым.
Спонсор, GTx, который разработал и руководил исследованием, обнаружил, что у 34,7% групп плацебо и 32,3% групп торемифена были случаи рака. Не было обнаружено различий в показателях Глисона для обеих групп.
Предыдущие исследования на мышах с использованием трансгенной аденокарциномы простаты мышей (TRAMP) показали, что торемифен предотвращал пальпируемые опухоли у 60% животных. В этом исследовании торемифен использовался в качестве раннего профилактического средства, что отличает его от исследований фазы III на людях.