В фармакологии, биодоступность (BA или F ) является подкатегорией абсорбции и представляет собой долю (%) введенного лекарственного средства, которая достигает большого круга кровообращения.
По определению, когда лекарство вводится внутривенно, его биодоступность составляет 100%. Однако, когда лекарство вводится путями, кроме внутривенного, его биодоступность обычно ниже, чем при внутривенном введении, из-за абсорбции кишечного эндотелия и метаболизма первого прохождения. Таким образом, математически биодоступность равна отношению сравнения площади под кривой концентрации лекарственного средства в плазме от времени (AUC) для внесосудистого препарата с AUC для внутрисосудистого препарата. AUC используется, потому что AUC пропорциональна дозе, попавшей в большой круг кровообращения.
Биодоступность лекарственного средства - это среднее значение ; для учета изменчивости популяции диапазон отклонения показан как ±. Чтобы гарантировать, что принимающий лекарство, который имеет плохую абсорбцию, получил надлежащую дозу, нижнее значение диапазона отклонения используется для представления реальной биодоступности и для расчета дозы лекарства, необходимой принимающему лекарство для достижения системных концентраций, аналогичных внутривенному составу. Для дозирования, не зная скорости абсорбции у принимающего лекарство, используется нижнее значение диапазона отклонения для обеспечения предполагаемой эффективности, если только лекарство не связано с узким терапевтическим окном.
Для пищевых добавок, травы и другие питательные вещества, путь введения которых почти всегда пероральный, биодоступность обычно обозначает просто количество или фракцию принятой дозы, которая абсорбируется.
В фармакологии биодоступность является мерой Изменение скорости и степени, в которой лекарство достигает места действия. Обозначается буквой f (или, если выражается в процентах, буквой F).
В науках о питании, которые охватывают потребление питательных веществ и немедикаментозных диетических ингредиентов, концепция биодоступности не имеет четко определенных стандартов, связанных с фармацевтической промышленностью. Фармакологическое определение не может применяться к этим веществам, поскольку усвоение и абсорбция являются функцией пищевого статуса и физиологического состояния субъекта, что приводит к еще большим различиям от человека к человеку (индивидуальные различия). Следовательно, биодоступность пищевых добавок можно определить как долю введенного вещества, способную абсорбироваться и доступную для использования или хранения.
Как в фармакологии, так и в науках о питании, биодоступность измеряется с помощью вычисление площади под кривой (AUC) временного профиля концентрации лекарственного средства.
Биодоступность - это мера, с помощью которой различные вещества из окружающей среды могут проникать в живые организмы. Обычно он является ограничивающим фактором при выращивании сельскохозяйственных культур (из-за ограничения растворимости или поглощения питательных веществ растений коллоидами почвы) и при удалении токсичных веществ из пищевой цепи микроорганизмами (из-за сорбции или распределения других разлагаемых веществ в недоступные фазы в среде). Заслуживающим внимания примером для сельского хозяйства является дефицит фосфора в растениях, вызванный осаждением фосфатами железа и алюминия при низком pH почвы и осаждением фосфатов кальция при высоком pH почвы. Токсичные материалы в почве, такие как свинец из краски, могут быть недоступны для животных, глотающих зараженную почву, из-за избытка фосфорных удобрений. Органические загрязнители, такие как растворители или пестициды, могут оказаться недоступными для микроорганизмов и, таким образом, сохраняться в окружающей среде, когда они адсорбируются на минералы почвы или распределяются между гидрофобными органическими веществами.
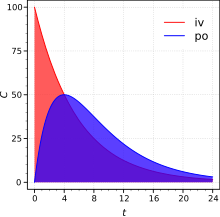 Абсолютная биодоступность - это соотношение области под кривыми. IV, внутривенно; ПО, устный маршрут. C - концентрация в плазме (произвольные единицы).
Абсолютная биодоступность - это соотношение области под кривыми. IV, внутривенно; ПО, устный маршрут. C - концентрация в плазме (произвольные единицы). Абсолютная биодоступность сравнивает биодоступность активного лекарственного средства в системном кровотоке после не- внутривенного введения (т.е. после перорального, глазное, ректальное, трансдермальное, подкожное или сублингвальное введение) с биодоступностью того же лекарственного средства после внутривенного введения. Это доля лекарства, абсорбированная при не внутривенном введении, по сравнению с соответствующим внутривенным введением того же лекарства. Сравнение должно быть нормализовано по дозам (например, учитывать разные дозы или различный вес субъектов); следовательно, поглощенное количество корректируется путем деления соответствующей введенной дозы.
В фармакологии, чтобы определить абсолютную биодоступность лекарственного средства, необходимо провести фармакокинетическое исследование, чтобы получить график зависимости концентрации лекарственного средства в плазме от времени для лекарственного средства после внутривенного (в / в) и внесосудистое (не внутривенное, т.е. пероральное) введение. Абсолютная биодоступность - это площадь под кривой с поправкой на дозу (AUC) при не внутривенном введении, деленная на AUC при внутривенном введении. Формула для расчета абсолютной биодоступности F лекарственного средства, вводимого перорально (перорально), приведена ниже (где D - введенная доза).

Следовательно, препарат, вводимый внутривенно, будет иметь абсолютную биодоступность 100% (f = 1), тогда как препараты, вводимые другими путями, обычно имеют абсолютную биодоступность менее единицы. Если мы сравним две разные лекарственные формы, содержащие одинаковые активные ингредиенты, и сравним биодоступность двух лекарств, это называется сравнительной биодоступностью.
Хотя знание истинной степени системной абсорбции (называемой абсолютной биодоступностью), безусловно, полезно, на практике он определяется не так часто, как можно подумать. Причина в том, что для его оценки требуется внутривенное введение; то есть такой способ введения, который гарантирует, что все введенное лекарство достигнет системного кровообращения. Такие исследования сопряжены со значительными затратами, не последней из которых является необходимость проведения доклинических испытаний на токсичность для обеспечения адекватной безопасности, а также потенциальные проблемы из-за ограничений растворимости. Однако эти ограничения могут быть преодолены путем введения очень низкой дозы (обычно несколько микрограммов) меченного изотопами одновременно с терапевтической пероральной дозой, не меченной изотопами (внутривенная доза, меченная изотопами, достаточна низкие, чтобы не нарушать системные концентрации лекарственного средства, достигаемые при пероральной дозе без маркировки). Затем внутривенные и пероральные концентрации можно деконволютировать в силу их различного изотопного состава и, таким образом, можно использовать для определения пероральной и внутривенной фармакокинетики при введении одной и той же дозы. Этот метод устраняет фармакокинетические проблемы с неэквивалентным клиренсом, а также позволяет вводить внутривенную дозу с минимумом токсикологии и рецептуры. Впервые этот метод был применен с использованием стабильных изотопов, таких как C, и масс-спектрометрии, чтобы различать изотопы по разнице масс. В последнее время препараты, меченные С, вводят внутривенно, а масс-спектрометрия с ускорителем (AMS) используется для измерения изотопно меченого лекарственного средства наряду с масс-спектрометрией для немеченого лекарственного средства.
Нет нормативных требований для определения внутривенной фармакокинетики или абсолютной биодоступность, однако, регулирующие органы иногда запрашивают информацию об абсолютной биодоступности экстраваскулярного пути в случаях, когда биодоступность явно низкая или вариабельная и существует доказанная взаимосвязь между фармакодинамикой и фармакокинетикой при терапевтических дозах. Во всех таких случаях для проведения исследования абсолютной биодоступности требуется, чтобы препарат вводился внутривенно.
Внутривенное введение развивающегося препарата может предоставить ценную информацию об основных фармакокинетических параметрах объема распределения (V) и очистка (CL).
В фармакологии относительная биодоступность измеряет биодоступность (оцениваемую как AUC) состава (A) определенного лекарственного средства по сравнению с другим составом (B) того же лекарственного средства, обычно установленным стандартом, или путем введения другим путем. Когда стандарт состоит из препарата, вводимого внутривенно, это называется абсолютной биодоступностью (см. выше).

Относительная биодоступность - это один из показателей, используемых для оценки биоэквивалентности (BE) между двумя лекарственными препаратами.. Для утверждения FDA производитель дженериков должен продемонстрировать, что 90% доверительный интервал для отношения средних ответов (обычно AUC и максимальной концентрации C max) его продукта к доля «фирменного препарата» находится в пределах от 80% до 125%. Где AUC относится к концентрации лекарственного средства в крови с течением времени от t = 0 до t = ∞, C max относится к максимальной концентрации лекарственного средства в крови. Когда указывается T max, это относится ко времени, которое требуется лекарству для достижения C max.
. Хотя механизмы, с помощью которых состав влияет на биодоступность и биоэквивалентность, были широко изучены в лекарствах, Факторы состава, влияющие на биодоступность и биоэквивалентность пищевых добавок, в значительной степени неизвестны. В результате в науках о питании относительная биодоступность или биоэквивалентность является наиболее распространенной мерой биодоступности, сравнивая биодоступность одного препарата одного и того же диетического ингредиента с другим.
Абсолютная биодоступность лекарственного средства при введении внесосудистым путем обычно меньше единицы (например, F < 100%). Various physiological factors reduce the availability of drugs prior to their entry into the systemic circulation. Whether a drug is taken with or without food will also affect absorption, other drugs taken concurrently may alter absorption and first-pass metabolism, intestinal motility alters the dissolution of the drug and may affect the degree of chemical degradation of the drug by intestinal microflora. Disease states affecting liver metabolism or gastrointestinal function will also have an effect.
Другие факторы могут включать, но не ограничиваются на:
Каждый из этих факторов может варьироваться от пациента к пациенту (индивидуально вариации), а также у одного и того же пациента с течением времени (внутрииндивидуальные вариации). В клинических испытаниях межличностные вариации являются критическим параметром, используемым для оценки различий в биодоступности от пациента к пациенту, чтобы гарантировать предсказуемость дозирования.
По сравнению с лекарствами, существуют значительные различия в пищевых добавках, которые влияют на оценку их биодоступности. Эти различия включают следующее: тот факт, что пищевые добавки обеспечивают переменные и часто качественные преимущества; неточности измерения усвоения питательных веществ; пищевые добавки употребляются для профилактики и улучшения самочувствия; пищевые добавки не показывают характерных кривых зависимости реакции от дозы ; и интервалы дозирования пищевых добавок, следовательно, не имеют решающего значения в отличие от лекарственной терапии.
Кроме того, отсутствие определенной методологии и правил, касающихся потребления пищевых добавок, препятствует применению мер биодоступности по сравнению с лекарствами.. В клинических испытаниях пищевых добавок биодоступность в первую очередь фокусируется на статистических описаниях средних или средних различий AUC между группами лечения, при этом часто не удается сравнить или обсудить их стандартные отклонения или межиндивидуальные вариации. Эта неудача оставляет открытым вопрос о том, сможет ли человек в группе испытать преимущества, описываемые сравнениями средней разницы. Кроме того, даже если бы этот вопрос обсуждался, было бы трудно передать значение этих межпредметных различий потребителям и / или их врачам.
Один из способов решения этой проблемы - определить «надежную биодоступность» как положительные результаты биодоступности (абсорбция, отвечающая заранее определенному критерию), которые включают 84% испытуемые и «универсальная биодоступность» включают 98% испытуемых. Эта надежная универсальная структура улучшит общение с врачами и потребителями, так что, если бы она была включена, например, на этикетках продуктов, они могли бы сделать осознанный выбор в отношении преимуществ рецептуры непосредственно для них. Кроме того, универсальная основа надежности аналогична построению доверительных интервалов, которые статистики давно предлагают в качестве одного из возможных решений для работы с небольшими выборками, нарушениями статистических допущений или большими стандартными отклонениями.
^TH: Одно из немногих исключений, когда препарат показывает F более 100% это теофиллин. При введении перорального раствора F составляет 111%, поскольку лекарство полностью абсорбируется и метаболизм первого прохождения в легких после внутривенного введения обходится.. ^OB: Лекарственные препараты, перечисленные в справочнике (т. Е. Новаторские). как генерические лекарственные препараты, одобренные на основании Сокращенной заявки на новые лекарства, приведены в Orange Book..