| Андрогенная депривация | |
|---|---|
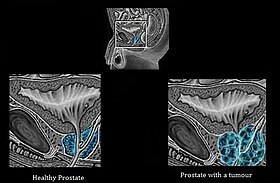 Различия между здоровой простатой и простатой с опухолью Различия между здоровой простатой и простатой с опухолью | |
| Другие названия | Андрогенная супрессивная терапия |
| Специальность | онкология |
| [редактирование в Викиданных ] | |
Андрогенная депривационная терапия (ADT ), также называемая андрогенной супрессивной терапией, антигормональная терапия, основное применение которой - лечение рака простаты. Клеткам рака простаты для роста обычно требуются андрогенные гормоны, такие как тестостерон. ADT снижает уровень андрогенных гормонов с помощью лекарств или хирургического вмешательства, чтобы предотвратить рост клеток рака простаты. Фармацевтические подходы включают антиандрогены и химическую кастрацию.
. Несколько исследований пришли к выводу, что ADT продемонстрировала пользу у пациентов с метастатическим заболеванием, а также в качестве дополнения к лучевой терапии у пациентов с местно-распространенным заболеванием, так как а также пациентов с неблагоприятным локализованным заболеванием промежуточного или высокого риска. Однако у пациентов с раком простаты низкого риска ADT не продемонстрировала преимущества в выживаемости и не продемонстрировала значительного вреда, такого как импотенция, диабет и потеря костной массы.
Терапия также может устранить раковые клетки, индуцируя андроген. старение, вызванное депривацией. Снижение уровня андрогенов или предотвращение их попадания в клетки рака простаты часто приводит к сокращению или замедлению роста рака простаты на какое-то время. Однако это лечение необходимо сочетать с лучевой терапией (ЛТ), потому что ADT сама по себе не устраняет рак ; это просто снижает его агрессивность.
 Процесс синтеза тестостерона
Процесс синтеза тестостерона Синтез тестостерона опосредуется цепочкой процессов, которые запускаются в нашем мозгу. Когда наш организм обнаруживает низкий уровень тестостерона, гипоталамус начинает вырабатывать LHRH, гормон, который, будучи полученным гипофизом, активирует синтез LH (лютеинизирующий гормон). ЛГ попадает в яички, где вызывает образование тестостерона. Существует два метода терапии андрогенной депривации, основанные на лекарствах. Один работает, не позволяя гипофизу выделять ЛГ, а другой блокирует способность организма использовать андрогены.
Нормальная мужская сексуальность, похоже, зависит от очень специфических и сложных гормональных паттернов, которые до конца не изучены. Одно исследование предполагает, что АДТ может изменять гормональный баланс, необходимый для мужской сексуальной активности. С возрастом у мужчин уровень тестостерона снижается примерно на 1% в год после 30 лет; однако важно определить, является ли низкий уровень тестостерона результатом нормального старения или заболевания, например гипогонадизма. Тестостерон играет важную роль в сексуальном функционировании; поэтому естественное снижение уровня тестостерона может привести к снижению нормального сексуального функционирования. Дальнейшее снижение уровня тестостерона в сыворотке крови может отрицательно сказаться на нормальной сексуальной функции, приводя к снижению качества жизни.
Эректильная дисфункция не редкость после радикальной простатэктомии, и мужчины, которым в дополнение к ней выполняются АДТ, могут демонстрируют дальнейшее снижение их способности участвовать в проникающем половом акте, а также их желание делать это. В исследовании, посвященном различиям в использовании ГнРГ-А (и подавляющего андрогены) или орхиэктомии, сообщается о различиях в сексуальном интересе, опыте эрекции и распространенности участия в сексуальной активности. У мужчин, у которых отсутствует сексуальный интерес, увеличилось с 27,6% до 63,6% после орхиэктомии и с 31,7% до 58,0% после гонадолиберин-А; мужчин, у которых не было эрекции, увеличилось с 35,0% до 78,6%; а у мужчин, которые не сообщали о сексуальной активности, увеличилось с 47,9% до 82,8% после орхиэктомии и с 45,0% до 80,2%. Это исследование предполагает, что гонадолиберин-А и орхиэктомия оказали сходное влияние на сексуальное функционирование. Порочный круг, в котором снижение уровня тестостерона приводит к снижению сексуальной активности, что, в свою очередь, вызывает еще большее снижение уровня как свободного, так и общего тестостерона. Это демонстрирует важность андрогенов для поддержания половых структур и функций.
Хотя нацеливание на ось андрогенов имеет очевидный терапевтический эффект, его эффективность носит временный характер, поскольку клетки опухоли простаты адаптируются для выживания и расти. Было показано, что удаление андрогенов активирует эпителиально-мезенхимальный переход (EMT), нейроэндокринную трансдифференцировку (NEtD) и генные программы, подобные раковым стволовым клеткам.
Таким образом активация этих программ посредством ингибирования оси андрогена обеспечивает механизм, с помощью которого опухолевые клетки могут адаптироваться, способствуя рецидиву и прогрессированию заболевания.
Орхиэктомия, аналоги LHRH и антагонисты LHRH могут вызывать сходные побочные эффекты, из-за изменения уровней половых гормонов (тестостерон).
Для пациентов и их партнеров была разработана программа, позволяющая распознавать и контролировать более обременительные побочные эффекты терапии депривацией андрогенов. Одна программа построена на основе книги 2014 года «Андрогенная депривационная терапия: важное руководство для пациентов с раком простаты и их близких», одобренной Канадской урологической ассоциацией.
Недавние исследования показали, что АДТ может увеличивать риск болезни Альцгеймера или деменции. Повышение риска может быть связано с продолжительностью ADT. Хотя некоторые исследования сообщают о снижении определенных областей когнитивных функций, таких как пространственные способности, внимание и вербальная память, связанное с ADT, данные в целом остаются противоречивыми.. Полезные профилактические вмешательства могут включать, среди прочего, социальное взаимодействие, физические упражнения и «».