 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Хлорид цинка | |
| Другие имена Хлорид цинка (II). Дихлорид цинка. Масло цинка | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.028. 720 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| UN номер | 2331 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | ZnCl 2 |
| Молярная масса | 136,315 г / моль |
| Внешний вид | белое кристаллическое твердое вещество. гигроскопичный и очень жидкий |
| Запах | без запаха |
| Плотность | 2,907 г / см |
| Точка плавления | 290 ° C (554 ° F; 563 K) |
| Температура кипения | 732 ° C (1350 ° F; 1005 K) |
| Растворимость в воде | 432,0 г / 100 г (25 ° C) |
| Растворимость | растворим в этанол, глицерин и ацетон |
| Растворимость в спирте | 430,0 г / 100 мл |
| Магнитная восприимчивость (χ) | -65,0 · 10 см / моль |
| Структура | |
| Координационная геометрия | Тетраэдр, линейная в газовой фазе |
| Фармакология | |
| Код АТС | B05XA12 (ВОЗ ) |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Классификация ЕС (DSD) (устарело) | Вредно (Xn). Коррозионно (C). Опасно для окружающей среды (N) |
| R-фразы (устаревшие) | R22, R34, R50 / 53 |
| S-фразы (устаревшие) | (S1 / 2), S26, S36 / 37/39, S45, S60, S61 |
| NFPA 704 (огненный алмаз) |  0 3 0 0 3 0 |
| Летальная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 350 мг / кг (крыса, перорально). 350 мг / кг (мышь, перорально). 200 мг / кг (морская свинка, перорально). 1100 мг / кг (крыса, перорально). 1250 мг / кг (мышь, перорально) |
| LC50(средняя концентрация ) | 1260 мг / м (крыса, 30 мин). 1180 мг-мин / м |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 1 мг / м (дым) |
| REL (Рекомендуется) | TWA 1 мг / м ST 2 мг / м (дым) |
| IDLH (Непосредственная опасность) | 50 мг / м (дым) |
| Родственные соединения | |
| Прочие анионы | Фторид цинка. Бромид цинка. Йодид цинка |
| Прочие катионы | Хлорид кадмия. Хлорид ртути (II) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Хлорид цинка - это название химических соединений с формулой ZnCl 2 и его гидраты. Хлориды цинка, из которых известно девять кристаллических форм, являются бесцветными или белыми и хорошо растворимы в воде. ZnCl 2 сам по себе гигроскопичен и даже расплывается. Поэтому образцы должны быть защищены от источников влаги, включая водяной пар, присутствующий в окружающем воздухе. Хлорид цинка находит широкое применение в обработке текстиля, металлургических флюсах и химическом синтезе. Ни один минерал с таким химическим составом не известен, кроме очень редкого минерала симонколлеит, Zn 5 (OH) 8Cl2·H2O.
Известны четыре кристаллические формы (полиморфы ) ZnCl 2 : α, β, γ и δ, и в каждой если ионы Zn тетраэдрически координированы с четырьмя ионами хлорида.
| Форма | Симметрия | Символ Пирсона | Группа | No | a (нм) | b (нм) | c (нм) | Z | ρ (г / см) |
|---|---|---|---|---|---|---|---|---|---|
| α | тетрагональный | tI12 | I42d | 122 | 0,5398 | 0,5398 | 0,64223 | 4 | 3,00 |
| β | тетрагональный | tP6 | P42/nmc | 137 | 0,3696 | 0,3696 | 1,071 | 2 | 3,09 |
| γ | моноклинический | mP36 | P21/c | 14 | 0,654 | 1.131 | 1,23328 | 12 | 2,98 |
| δ | орторомбический | oP12 | Pna21 | 33 | 0,6125 | 0,6443 | 0,7693 | 4 | 2,98 |
Здесь a, b и c - постоянные решетки, Z - количество структурных единиц на элементарную ячейку, а ρ - плотность, рассчитанная на основе параметров структуры.
Чистая безводная орторомбическая форма (δ) быстро превращается в одну из других форм при воздействии атмосферы, и возможное объяснение состоит в том, что ионы ОН, происходящие из поглощенной воды, способствуют перегруппировке. Быстрое охлаждение расплавленного ZnCl 2 дает стекло.
На ковалентный характер безводного материала указывает его относительно низкая температура плавления, равная 275. ° C. Дополнительное доказательство ковалентности обеспечивается высокой растворимостью дихлорида в эфирных растворителях, где он образует аддукты с формулой ZnCl 2L2, где L = лиганд такой как O (C 2H5)2. В газовой фазе молекулы ZnCl 2 линейны с длиной связи 205 мкм.
Расплавленный ZnCl 2 имеет высокую вязкость при температуре плавления и сравнительно низкую электропроводность, которая заметно увеличивается с температурой. Исследование расплава комбинационным рассеянием показало присутствие полимерных структур, а исследование рассеяния нейтронов показало, что наличие тетраэдрических комплексов {ZnCl 4 }.
Известно пять гидратов хлорида цинка: ZnCl 2(H2O)nс n = 1, 1,5, 2,5, 3 и 4. Тетрагидрат ZnCl 2(H2O)4кристаллизуется из водных растворов хлорида цинка.
Можно получить безводный ZnCl 2 из цинка и хлористого водорода :
Гидратированные формы и водные растворы могут быть легко получены аналогичным образом путем обработки металлического Zn соляной кислотой. Оксид цинка и сульфид цинка реагируют с HCl:
В отличие от многих других элементов, цинк по существу существует только в одной степени окисления, 2+, что упрощает очистку хлорида.
Коммерческие образцы хлорида цинка обычно содержат воду и продукты гидролиза в качестве примесей. Такие образцы могут быть очищены перекристаллизацией из горячего диоксана. Безводные образцы могут быть очищены посредством сублимации в потоке газа хлористого водорода с последующим нагреванием возгонки до 400 ° C в потоке сухого газа азота. Наконец, самый простой метод основан на обработке хлорида цинка тионилхлоридом.
Расплавленный безводный ZnCl 2 при 500–700 ° C растворяет металлический цинк и При быстром охлаждении расплава образуется желтое диамагнитное стекло, которое, как показывают исследования комбинационного рассеяния, содержит ион Zn. 2.
Ряд солей, содержащих анион тетрахлорцинката, ZnCl. 4, известны. «Реагент Колтона», V 2Cl3(thf) 6Zn2Cl6является примером соли, содержащей Zn 2Cl. 6. Соединение Cs 3 ZnCl 5 содержит тетраэдрические анионы ZnCl. 4и Cl. Никакие соединения, содержащие ион ZnCl. 6, не охарактеризованы.
Хотя хлорид цинка хорошо растворяется в воде, нельзя считать, что растворы содержат просто сольватированные ионы Zn и ионы Cl, ZnCl xH2O(4-x) виды также присутствуют. Водные растворы ZnCl 2 являются кислыми: водный раствор 6 M имеет pH, равный 1. Кислотность водных растворов ZnCl 2 по сравнению с растворами других солей Zn происходит из-за образования тетраэдрических хлор-аквакомплексов, где уменьшение координационного числа с 6 до 4 еще больше снижает прочность связей O – H в сольватированных молекулах воды.
В растворе щелочи в присутствии иона ОН в растворе присутствуют различные анионы гидроксихлорида цинка, например Выпадает Zn (OH) 3 Cl, Zn (OH) 2Cl. 2, ZnOHCl. 3и Zn 5 (OH) 8Cl2·H2O (симонколлеит).
Когда аммиак барботируется через раствор хлорида цинка, гидроксид не осаждается, вместо этого образуются соединения, содержащие комплексный аммиак (аммины), Zn (NH 3)4Cl2·H2O и при концентрации ZnCl 2 ( NH 3)2. Первый содержит ион Zn (NH 3)6, а второй является молекулярным с искаженной тетраэдрической геометрией. Частицы в водном растворе были исследованы и показали, что Zn (NH 3)4является основным присутствующим компонентом с Zn (NH 3)3Cl также присутствует при более низком соотношении NH 3 : Zn.
Водный хлорид цинка реагирует с оксидом цинка с образованием аморфного цемента, который впервые был исследован в 1855 г. Станислав Сорел. Позже Сорел продолжил исследование родственного цемента на основе оксихлорида магния, который носит его имя.
Когда гидратированный хлорид цинка нагревается, получается остаток Zn (OH) Cl, например,
Соединение ZnCl 2 · ⁄ 2 HCl · H 2 O может быть получено осторожным осаждением из раствора ZnCl 2 подкисляют HCl. Он содержит полимерный анион (Zn 2Cl5)nс уравновешиванием моногидратированных ионов гидроксония, ионов H 5O2.
Образование высокореакционного безводного газообразного HCl, образующегося при нагревании гидратов хлорида цинка, происходит основа качественных неорганических точечных тестов.
Использование хлорида цинка в качестве флюса, иногда в смеси с хлоридом аммония (см. также Цинк-аммонийхлорид ), включает образование HCl и его последующую реакцию с поверхностными оксидами. Хлорид цинка образует две соли с хлоридом аммония: (NH 4)2ZnCl 4 и (NH 4)3ClZnCl 4, которые разлагаются при нагревании с высвобождением HCl, как это делает гидрат хлорида цинка. Действие флюсов хлорида цинка / хлорида аммония, например, в процессе горячего цинкования дает H 2 газ и пары аммиака.
Целлюлоза растворяется в водных растворах ZnCl 2, и были обнаружены комплексы цинк-целлюлоза. Целлюлоза также растворяется в расплавленном гидрате ZnCl 2 и карбиде боксилирование и ацетилирование проводят на полимере целлюлозы.
Таким образом, хотя многие соли цинка имеют разные формулы и разные кристаллические структуры, эти соли ведут себя очень сходно в водном растворе. Например, растворы, полученные из любого из полиморфов ZnCl 2, а также других галогенидов (бромида, йодида) и сульфата, часто могут использоваться взаимозаменяемо для получения других соединений цинка. Наглядным примером является получение карбоната цинка:
Хлорид цинка обладает способностью реагировать с оксидами металлов (МО) с образованием производных формулы MZnOCl 2. Эта реакция имеет отношение к использованию раствора ZnCl 2 в качестве флюса для пайки - он растворяет оксидные покрытия, обнажая чистую металлическую поверхность. Флюсы с ZnCl 2 в качестве активного ингредиента иногда называют «жидкостью тонировщика». Обычно этот флюс получают растворением цинковой фольги в разбавленной соляной кислоте до тех пор, пока жидкость не перестанет выделять водород; по этой причине такие потоки когда-то были известны как «убитые духи». Из-за своей коррозионной природы этот флюс не подходит для ситуаций, когда любые остатки не могут быть удалены, например, при работе с электроникой. Это свойство также приводит к его использованию в производстве магнезиальных цементов для зубных пломб и некоторых жидкостей для полоскания рта в качестве активного ингредиента.
Раннее использование хлорида цинка (Silzic) заключалось в создании углеродных скелетов путем конденсации молекул метанола. Ненасыщенные углеводороды являются основными продуктами, при этом условия реакции влияют на распределение продуктов, хотя некоторые ароматические соединения были образованы. В 1880 году было обнаружено, что расплавленный хлорид цинка катализирует реакцию ароматизации с образованием гексаметилбензола. При температуре плавления ZnCl 2 (283 ° C) реакция имеет ΔG = -1090 кДж / моль и может быть идеализирована как
Первооткрыватели этой реакции рационализировали ее как включающую конденсацию метиленовых звеньев с последующим полным метилированием по Фриделю-Крафтсу образующееся бензольное кольцо с хлорметаном, генерируемым in situ. Такое превращение алкилирования представляет собой применение умеренной силы хлорида цинка, такой как кислота Льюиса, которая является ее основной ролью в лабораторном синтезе. Другие примеры включают катализирование (A) синтеза индола по Фишеру, а также (B) реакций ацилирования Фриделя-Крафтса с участием активированных ароматических колец

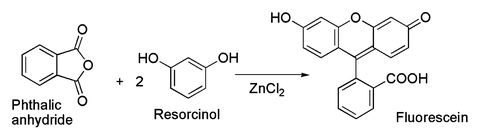
, относящихся к последний представляет собой классический препарат красителя флуоресцеин из фталевого ангидрида и резорцина, который включает ацилирование Фриделя-Крафтса. на самом деле было выполнено используя даже образец гидратированного ZnCl 2, показанный на рисунке выше.
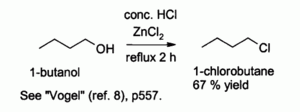
Соляная кислота сама по себе плохо реагирует с первичными спиртами и вторичными спиртами, но комбинация HCl с ZnCl 2 (известная вместе как " Реагент Лукаса ") эффективен для получения алкилхлоридов. Типичные реакции проводят при 130 ° C. Эта реакция, вероятно, протекает по механизму SN2 с первичными спиртами, но по SN1 пути со вторичными спиртами.
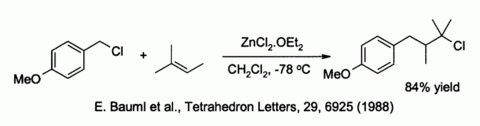
Хлорид цинка также активирует бензиловые и аллильные галогениды в сторону замещения слабыми нуклеофилами, такими как алкены :
. Аналогичным образом ZnCl 2 способствует селективному восстановлению NaBH 3CN третичных, аллильных или бензильных галогенидов до соответствующих углеводородов.
Хлорид цинка также является полезным исходным реагентом для синтеза многих цинкорганических реагентов, таких как те, которые используются в катализируемом палладием сочетании Негиши с арилгалогенидами. или винилгалогениды. В таких случаях цинкорганическое соединение обычно получают трансметаллированием из литийорганического или реактива Гриньяра, например:

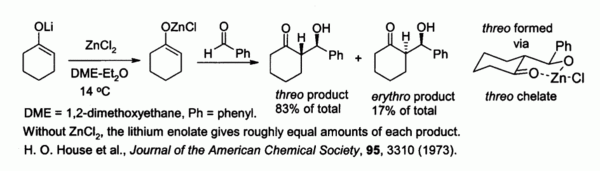
еноляты цинка , полученные из енолятов щелочных металлов и ZnCl 2, обеспечивают контроль стереохимии в реакциях альдольной конденсации за счет хелатирования цинка.. В примере, показанном ниже, продукт трео имел преимущество перед эритро в 5: 1, когда ZnCl 2 в DME / эфир. Хелат более стабилен, когда объемная фенильная группа является псевдо экваториальной, а не псевдо аксиальной, то есть трео, а не эритро.
Концентрированные водные растворы хлорида цинка (более 64% вес / вес хлорида цинка в воде) обладают интересным свойством растворения крахмала, шелк и целлюлоза. Таким образом, такие растворы нельзя фильтровать через стандартные бумажные фильтры. В связи с его сродством к этим материалам ZnCl 2 используется в качестве антипирена и в «освежителях» тканей, таких как Febreze. Вулканизированное волокно получают путем замачивания бумаги в концентрированном хлориде цинка.
Дымовая смесь хлорида цинка («HC»), используемая в дымовых гранатах, содержит оксид цинка, гексахлорэтан и гранулированный алюминиевый порошок, которые при воспламенении реагируют с образованием дыма хлорида цинка, углерода и оксида алюминия, эффективной дымовой завесы.
Нингидрин реагирует с аминокислотами и аминами с образованием окрашенного соединения «пурпур Рухемана» (RP). При опрыскивании раствором хлорида цинка образуется комплекс RP: ZnCl (H 2O)2в соотношении 1: 1, который легче обнаруживается, поскольку он флуоресцирует лучше, чем пурпурный цвет Рухемана.
Исторически сложилось так, что разбавленный водный раствор хлорида цинка использовался в качестве дезинфицирующего средства под названием «Дезинфицирующая жидкость Бернетта». Он также используется в некоторых коммерческих марках антисептических жидкостей для полоскания рта.
Хлорид цинка имеет использовались в альтернативной медицине для образования струпов, корок отмерших тканей, в попытке вылечить рак кожи. Различные продукты, такие как Cansema или «черная мазь», содержащие хлорид цинка и продаваемые как лекарства от рака, были перечислены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) как подделка с предупреждениями, рассылаемыми поставщикам.
В многочисленных отчетах в медицинской литературе описываются серьезные рубцы и повреждения нормальная кожа эхаротическими веществами. Учитывая эти побочные эффекты, его использование в лечении не Гораздо более безопасные и эффективные альтернативы, такие как лучевая терапия и хирургия Мооса.
Хлорид цинка вызывает раздражение кожи. При попадании на кожу необходимо немедленно удалить с помощью мыла и большого количества воды. При попадании в глаза адекватные меры: промыть большим количеством воды или другим промытьем для глаз и как можно скорее обратиться к офтальмологу.
Хлорид цинка оказывает едкое воздействие на желудочно-кишечный тракт, иногда приводя к его появлению. к гематемезис. Симптомами острой интоксикации являются расстройство желудочно-кишечного тракта, диарея, тошнота и боли в животе. Рвота возникает почти повсеместно. Смертельная доза для человека составляет 3–5 г. В обеззараживании желудочно-кишечного тракта после перорального приема соединений цинка в большинстве случаев нет необходимости, поскольку у пациентов обычно достаточно рвоты. Для уменьшения всасывания металла можно давать молоко. Уровни цинка можно нормализовать с помощью солей ЭДТА.
Хлорид цинка чрезвычайно вреден для легких, а воздействие дыма хлорида цинка на легкие ранее приводило к смертельному исходу. Вдыхание паров цинка, оксида цинка или хлорида цинка приводит к отеку легких и лихорадке паров металлов. Начало наступает в течение 4–6 часов и может задерживаться до 8 часов. Симптомы включают учащенное дыхание, одышку, кашель, лихорадку, дрожь, потливость, боль в груди и ногах, миалгию, усталость, металлический привкус, слюноотделение, жажду и лейкоцитоз, который может длиться от 24 до 48 часов. В случае вдыхания дыма препараты кортизона следует применять немедленно (например, путем вдыхания), чтобы избежать развития отека легких.