Ароматизация - это химическая реакция, в которой ароматическая система образуется из единственный неароматический предшественник. Обычно ароматизация достигается дегидрированием существующих циклических соединений, что иллюстрируется превращением циклогексана в бензол. Ароматизация включает образование гетероциклических систем.
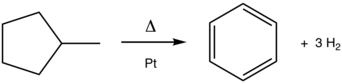
 Превращение метилциклогексана в толуол является классической реакцией ароматизации. Этот процесс, катализируемый платиной (Pt), широко применяется в производстве бензина из нефти.
Превращение метилциклогексана в толуол является классической реакцией ароматизации. Этот процесс, катализируемый платиной (Pt), широко применяется в производстве бензина из нефти.Хотя ароматизация не практикуется под этим названием, она является краеугольным камнем переработки нефти. Одной из основных реакций риформинга является дегидрирование нафтенов в ароматические углеводороды. Примером процесса, который катализируется платиной, является превращение метилциклогексана (нафтен) в толуол (ароматический). Дегидроциклизация превращает парафины (ациклические углеводороды)) в ароматические углеводороды. Родственный процесс ароматизации включает дегидроизомеризацию метилциклопентана в бензол:

Ароматазы представляют собой ферменты, которые частично ароматизируют стероиды. Конкретные преобразования: тестостерон в эстрадиол и андростендион в эстрон. Каждая из этих ароматизаций включает окисление C-19 метил группы до муравьиной кислоты, чтобы обеспечить образование ароматической системы, превращения, которые являются необходимыми частями эстрогенового туморогенеза. в развитии рака груди и рака яичников у женщин в постменопаузе и гинекомастии у мужчин. Ингибиторы ароматазы как экземестан (который образует постоянную и дезактивирующую связь с ферментом ароматазы) и анастрозол и летрозол (которые конкурируют за фермент), как было показано, более эффективны, чем антиэстрогеновые препараты, такие как тамоксифен, вероятно, потому, что они предотвращают образование эстрадиола.
Для циклогексана, циклогексена и циклогексадиена дегидрирование является концептуально простейшим путем ароматизации. Барьер активации уменьшается со степенью ненасыщенности. Таким образом, циклогексадиены особенно склонны к ароматизации. Формально дегидрирование - это окислительно-восстановительный процесс. Дегидрогенизирующая ароматизация обратна гидрированию арена. По существу, катализаторы гидрирования эффективны для обратной реакции. Катализируемое платиной дегидрирование циклогексанов и родственного сырья является наиболее масштабным применением этой реакции (см. Выше).
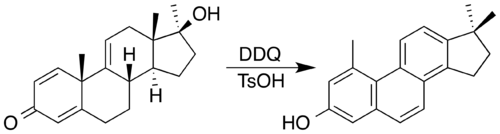
2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ) часто используется реагент выбора. DDQ и кислотный катализатор были использованы для синтеза стероида с ядром фенантрена путем окисления, сопровождаемого двойной миграцией метила. В процессе сам DDQ восстанавливается до ароматического гидрохинона.
Сера и селен традиционно используются при ароматизации, уходящей группой является сероводород.
Растворимые комплексы переходных металлов могут вызывать окислительную ароматизацию, сопровождающуюся комплексообразованием. α-Фелландрен (2-метил-5-изопропил-1,3-циклогексадиен) окисляется до п-изопропилтолуола с восстановлением трихлорида рутения.
Окислительное дегидрирование дигидропиридина приводит к ароматизации, давая пиридин.
 Синтез Семмлера-Вольфа анилина
Синтез Семмлера-Вольфа анилина Неароматические кольца можно ароматизировать многими способами. Дегидратация позволяет Семмлера-Вольфа превращать 2-циклогексенон оксим в анилин в кислых условиях.
 1,4-диоксотетралин и его ароматизированный таутомер 1,4-нафталиндиол сосуществуют в растворе в равном количестве.
1,4-диоксотетралин и его ароматизированный таутомер 1,4-нафталиндиол сосуществуют в растворе в равном количестве. изомеризация циклогексадиенонов дает ароматический таутомер фенол. Изомеризация 1,4-нафталиндиола при 200 ° C дает смесь 2: 1 с его кетоформой, 1,4-диоксотетралином.
Классически реакции ароматизации включают изменение соотношение C: H субстрата. При применении к циклопентадиену удаление протона дает ароматическое сопряженное основание циклопентадиенил-анион, выделяемое как циклопентадиенид натрия :
Ароматизация может повлечь за собой удаление гидрида. Тропилий, C. 7H. 7возникает в результате реакции ароматизации циклогептатриена с акцепторами гидрида.
 Перегруппировка Чамикиана-Денштедта пиррола в пиридин. Первый шаг включает деароматизацию . Вторая стадия включает ароматизацию.
Перегруппировка Чамикиана-Денштедта пиррола в пиридин. Первый шаг включает деароматизацию . Вторая стадия включает ароматизацию. Ароматизация ациклических предшественников встречается реже в органическом синтезе, хотя она является важным компонентом производства БТК на нефтеперерабатывающих заводах.
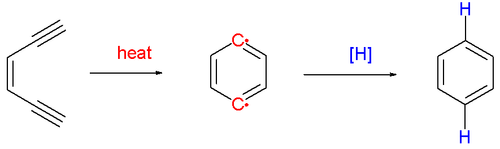
Среди ациклических предшественников алкины относительно склонны к ароматизации, поскольку они частично дегидрированы. Циклизация Бергмана представляет собой превращение ендиина в промежуточный дегидробензол бирадикал, который отводит водород для ароматизации. Ендииновый фрагмент может быть включен в существующее кольцо, обеспечивая доступ к бициклической системе в мягких условиях, как следствие кольцевого штамма в реагенте. Циклодека-3-ен-1,5-диин реагирует с 1,3-циклогексадиеном с образованием бензола и тетралина при 37 ° C, причем реакция является очень благоприятной из-за образования два новых ароматических кольца: