 | |||
 | |||
| |||
 . Анион циклопентадиенида . Анион циклопентадиенида | |||
| Имена | |||
|---|---|---|---|
| Другие названия циклопентадиенилид натрия, циклопентадиенилнатрий | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.023.306 | ||
| Номер EC |
| ||
| PubChem CID | |||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | C5H5Na | ||
| Молярная масса | 88,085 г · моль | ||
| Внешний вид | бесцветное твердое вещество | ||
| Плотность | 1,113 г / см | ||
| Растворимость в ваттах er | разложение | ||
| Растворимость | THF | ||
| Опасности | |||
| Основные опасности | воспламеняющиеся | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Циклопентадиенид натрия представляет собой натрийорганическое соединение с формулой C5H5Na. Соединение часто обозначают аббревиатурой NaCp, где Cp представляет собой анион циклопентадиенида. Циклопентадиенид натрия представляет собой бесцветное твердое вещество, хотя образцы часто имеют розовый цвет из-за следов окисленных примесей.
Циклопентадиенид натрия коммерчески доступен в виде раствора в ТГФ. Его получают путем обработки циклопентадиена с натрием :
Обычно преобразование проводят путем нагревания суспензии расплавленного натрия в дициклопентадиен. В прежние времена натрий обычно предоставлялся в форме «натриевой проволоки» или «натриевого песка», тонкой дисперсии натрия, полученной плавлением натрия в кипящем ксилоле и быстром перемешивании. Гидрид натрия - удобное основание:
В ранних работах реактивы Гриньяра использовались в качестве оснований. При pKa, равном 15, циклопентадиен может быть депротонирован многими реагентами.
Циклопентадиенид натрия является обычным реагентом для получения замещенных циклопентадиенильных солей, таких как сложноэфирные и формильные соединения NaC 5H4X (CO 2 Me, CHO):
Циклопентадиенид натрия является обычным реагентом для получения металлоценов. Например, получение ферроцена и дихлорида цирконоцена :
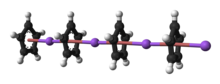
Природа NaCp сильно зависит от среды, в которой он используется, и для целей планирования синтезов реагент часто представляет собой соль Na. C. 5H. 5. Кристаллический NaCp без растворителя, который встречается редко, представляет собой «полидеккер» сэндвич-комплекс, состоящий из бесконечной цепочки чередующихся центров Na, расположенных между лигандами μ -η : η-C 5H5. В качестве раствора в донорных растворителях NaCp обладает высокой сольватированностью, особенно в щелочном металле, как предполагает Изоляция аддукта Na(tmeda )Cp.
В отличие от циклопентадиенидов щелочных металлов, тетрабутиламмоний циклопентадиенид (Bu 4NC5H5) был было обнаружено, что он полностью поддерживается ионной связью, и его структура представляет структуру аниона циклопентадиенида (C 5H5, Cp) в твердом состоянии. Однако анион несколько отклоняется от плоского правильного пятиугольника с длиной связей C – C в диапазоне 138,0–140,1 пм и валентными углами C – C – C в диапазоне 107,5–108,8 °.