 Пример μ-мостикового лиганда
Пример μ-мостикового лиганда В координационной химии, a мостиковый лиганд представляет собой лиганд, который соединяет два или более атомов, обычно ионы металлов. Лиганд может быть атомным или многоатомным. Практически все сложные органические соединения могут служить мостиковыми лигандами, поэтому термин обычно ограничивается небольшими лигандами, такими как псевдогалогениды, или лигандами, которые специально предназначены для связывания двух металлов.
В названии комплекса, в котором один атом связывает два металла, мостиковому лиганду предшествует греческая буква мю, μ с надстрочным индексом число, обозначающее количество металлов, связанных с мостиковым лигандом. μ часто обозначают просто μ. При описании координационных комплексов следует проявлять осторожность, чтобы не путать μ с η («эта»), что относится к тактильности. Лиганды, не являющиеся мостиковыми, называются концевыми лигандами (см. Рисунок).
Известно, что практически все лиганды образуют мостик, за исключением аминов и аммиака. Обычные неорганические мостиковые лиганды включают большинство обычных анионов.
| Мостиковый лиганд | Название | Пример |
|---|---|---|
| OH-. | гидроксид | [Fe. 2 (OH). 2 (H. 2O). 8], см. олатион |
| O | оксид | [Cr. 2O. 7], см. полиоксометаллат |
| SH-. | гидросульфидо | Cp. 2Mo. 2 (SH). 2S. 2 |
| NH-. 2 | амидо | HgNH. 2Cl |
| N | нитрид | [Ir. 3N (SO. 4). 6 (H. 2O). 3], см. нитридокомплекс металла |
| CO | карбонил | Fe. 2 (CO). 9, см. мостиковый карбонил |
| Cl-. | хлорид | Nb. 2Cl. 10, см. галогенидные лиганды |
| H−. | гидрид | B. 2H. 6 |
| CN-. | цианид | прибл. Fe. 7 (CN). 18 (берлинская лазурь ), см. цианометаллат |
| PPh-. 2 | дифенилфосфид | см. фосфидокомплексы переходных металлов |
Многие простые органические лиганды образуют прочные мосты между металлическими центрами. Многие общие примеры включают органические производные вышеуказанных неорганических лигандов (R = алкил, арил): OR-., SR-., NR-. 2, NR (имидо), PR-. 2 (фосфидо, обратите внимание на двусмысленность с предыдущей записью), PR (фосфинидино) и многие другие.
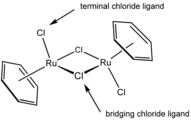
В этом рутениевом комплексе ((бензол) дихлорид дихлорида рутения ) два хлоридных лиганда являются концевыми и два - мостиковые μ.

Пиразин является мостиковым лигандом в этом соединении дирутения, называемом комплексом Крейца – Таубе.

В кобальтовом кластере Co. 3 (CO). 9 (Ct. Bu) лиганд Ct. Bu является трехкомпонентным, хотя этот аспект обычно не указывается в формуле.
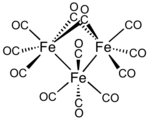
В додекарбониле трижелеза два лиганда CO являются мостиковыми, а десять - концевыми лигандами. Концевые и мостиковые лиганды CO быстро меняются местами.

В NbCl 5 имеется два мостиковых и восемь концевых хлоридных лиганда.

Кластер [Au. 6C (PPh. 3). 6] содержит лиганд μ- карбид, хотя, опять же, обозначение «μ» обычно не используется.

В триоксиде рения все оксидные лиганды представляют собой μ. Эти оксидные лиганды «склеивают» металлические центры.
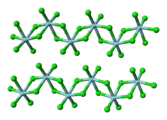
В случае ZrCl. 4 присутствуют как концевые, так и двояковыпуклые хлоридные лиганды.

В ацетате родия (II) четыре ацетатные группы являются мостиковыми лигандами.
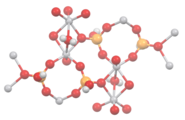
В VO (HPO. 4) · 0,5H 2 O пары центров ванадия (IV) соединены водными лигандами.
Для двойного связывания (μ-) лиганды, два ограничивающих представления - это 4-электронные и 2-электронные связывающие взаимодействия. Эти случаи проиллюстрированы в химии основных групп с помощью [Me. 2Al (μ-Cl)]. 2 и [Me. 2Al (μ-Me)]. 2. Этот анализ усложняется возможностью соединения металл-металл. Вычислительные исследования показывают, что связь металл-металл отсутствует во многих соединениях, где металлы разделены мостиковыми лигандами. Например, расчеты показывают, что в Fe. 2 (CO). 9 отсутствует связь железо-железо в силу 2-электронной связи с 3 центрами с участием одного из три мостиковых лиганда CO.
 Представления двух видов взаимодействий μ-мостиковых лигандов: 3-центральная, 4-электронная связь (слева) и 3-центральная, 2-электронная связь.
Представления двух видов взаимодействий μ-мостиковых лигандов: 3-центральная, 4-электронная связь (слева) и 3-центральная, 2-электронная связь. Полифункциональные лиганды могут присоединяться к металлам разными способами и, таким образом, могут связывать металлы различными способами, включая совместное использование одного атома или использование нескольких атомов. Примерами таких многоатомных лигандов являются оксоанионы CO2-. 3 и родственные карбоксилаты, PO3-. 4 и полиоксометаллаты.. Было разработано несколько фосфорорганических лигандов, связывающих пары металлов, хорошо известным примером является Ph. 2PCH. 2PPh. 2.
| title =()