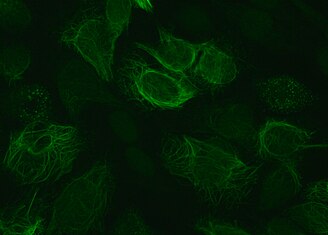
 Иммунофлуоресцентное окрашивание антител к виментину. Получают путем инкубации первичных антител виментина и вторичных антител, меченных FITC, с клетками HEp-20-10.
Иммунофлуоресцентное окрашивание антител к виментину. Получают путем инкубации первичных антител виментина и вторичных антител, меченных FITC, с клетками HEp-20-10. Виментин представляет собой структурный белок, который у человека кодируется геном VIM . Его название происходит от латинского vimentum, что относится к массиву гибких стержней.
 Иммунофлуоресцентное окрашивание клеток HeLa антителами для выявления виментина, содержащего промежуточные волокна зеленого цвета и антитела к LAMP1, чтобы выявить красные лизосомы. Ядерная ДНК показана синим цветом. Антитела и изображения любезно предоставлены EnCor Biotechnology Inc.
Иммунофлуоресцентное окрашивание клеток HeLa антителами для выявления виментина, содержащего промежуточные волокна зеленого цвета и антитела к LAMP1, чтобы выявить красные лизосомы. Ядерная ДНК показана синим цветом. Антитела и изображения любезно предоставлены EnCor Biotechnology Inc.Виментин представляет собой белок промежуточного филамента (IF) типа III , который экспрессируется в мезенхимальных клетках. Белки ПФ обнаружены во всех клетках животных, а также в бактериях. IF, наряду с тубулином, микротрубочками и актиновыми микрофиламентами, составляет цитоскелет. Все белки IF экспрессируются в высокой степени регулируемым путем развития; виментин является основным цитоскелетным компонентом мезенхимальных клеток. Из-за этого виментин часто используется в качестве маркера мезенхимальных клеток или клеток, претерпевающих эпителиально-мезенхимальный переход (EMT) как во время нормального развития, так и во время метастатической прогрессии.
Мономер виментина, как и все другие промежуточные филаменты, имеет центральный α-спиральный домен, закрытый на каждом конце не- спиральным амино (головной) и карбоксильным (хвостовым) доменами.. Два мономера, вероятно, ко-трансляционно экспрессируются таким образом, чтобы облегчить их образование димера спиральной спирали, который является основной субъединицей сборки виментина.
α-спиральные последовательности содержат структуру гидрофобных аминокислот, которые способствуют образованию «гидрофобного уплотнения» на поверхности спирали. Кроме того, существует периодическое распределение кислотных и основных аминокислот, которое, по-видимому, играет важную роль в стабилизации димеров спиральной спирали. Расстояние между заряженными остатками является оптимальным для ионных солевых мостиков, что позволяет стабилизировать структуру α-спирали. Хотя этот тип стабилизации является интуитивно понятным для внутрицепочечных взаимодействий, а не для межцепочечных взаимодействий, ученые предположили, что, возможно, переход от внутрицепочечных солевых мостиков, образованных кислотными и основными остатками, к межцепочечным ионным ассоциациям, способствует сборке филамента.
Виментин играет важную роль в поддержке и закреплении положения органелл в цитозоле. Виментин прикрепляется к ядру, эндоплазматическому ретикулуму и митохондриям либо латерально, либо окончательно.
Динамическая природа виментина важна, когда предлагая ячейке гибкость. Ученые обнаружили, что виментин придает клеткам устойчивость, отсутствующую в сетях микротрубочек или актиновых филаментов, когда они подвергаются механическому стрессу in vivo. Таким образом, в целом считается, что виментин является компонентом цитоскелета, ответственным за поддержание целостности клетки. (Было обнаружено, что клетки без виментина чрезвычайно чувствительны при воздействии микропунктуры.) Трансгенные мыши, у которых отсутствует виментин, выглядели нормальными и не демонстрировали функциональных различий. Возможно, что сеть микротрубочек могла компенсировать отсутствие промежуточной сети. Этот результат подтверждает тесное взаимодействие между микротрубочками и виментином. Более того, когда присутствовали деполимеризаторы микротрубочек, происходила реорганизация виментина, что еще раз указывает на взаимосвязь между двумя системами. С другой стороны, раненые мыши, у которых отсутствует ген виментина, заживают медленнее, чем их аналоги дикого типа.
По сути, виментин отвечает за поддержание формы клеток, целостность цитоплазмы и стабилизацию взаимодействий с цитоскелетом. Было показано, что виментин устраняет токсичные белки в JUNQ и IPOD телец включения при асимметричном делении клеточных линий.
млекопитающих. Кроме того, обнаружено, что виментин контролирует транспорт липопротеин низкой плотности, ЛПНП, холестерин из лизосомы в место этерификации. При блокировании транспорта холестерина, полученного из ЛПНП, внутри клетки было обнаружено, что клетки накапливают гораздо более низкий процент липопротеина, чем нормальные клетки с виментином. Эта зависимость, по-видимому, является первым процессом биохимической функции в любой клетке, который зависит от клеточной сети промежуточных филаментов. Этот тип зависимости имеет разветвления на клетки надпочечников, которые зависят от эфиров холестерина, полученных из ЛПНП.
Виментин играет роль в формировании агресомы, где он образует клетку, окружающую ядро агрегированного
Он был использован в качестве саркомы маркера опухоли для идентификации мезенхимы.
Метилирование виментина Ген был установлен как биомаркер рака толстой кишки, и он используется при разработке фекальных тестов на рак толстой кишки. Статистически значимые уровни метилирования гена виментина также наблюдались при некоторых патологиях верхних отделов желудочно-кишечного тракта, таких как пищевод Барретта, аденокарцинома пищевода и рак желудка кишечного типа. Высокие уровни метилирования ДНК в промоторной области также были связаны с заметным снижением выживаемости при гормон-положительном раке молочной железы. Подавление виментина было выявлено при кистозном варианте папиллярной карциномы щитовидной железы с использованием протеомного подхода. См. Также антитело к цитруллинированному белку для его использования в диагностике ревматоидного артрита.
Было показано, что виментин взаимодействует с:
3 'UTR мРНК Vimentin было обнаружено, что он связывает белок 46 кДа.