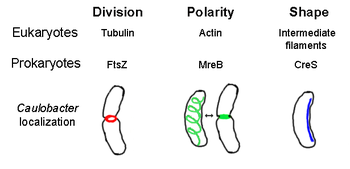
 Элементы цитоскелета Caulobacter crescentus. Прокариотические цитоскелетные элементы соответствуют их эукариотическому гомологу и предполагаемой клеточной функции.
Элементы цитоскелета Caulobacter crescentus. Прокариотические цитоскелетные элементы соответствуют их эукариотическому гомологу и предполагаемой клеточной функции. прокариотический цитоскелет - это собирательное название всех структурных нитей в прокариот. Когда-то считалось, что прокариотические клетки не обладают цитоскелетом, но достижения в технологии визуализации и определения структуры привели к открытию филаментов в этих клетках в начале 1990-х годов. Были обнаружены не только аналоги всех основных белков цитоскелета у эукариот у прокариот, но и белки цитоскелета без известных эукариотических гомологов. Элементы цитоскелета играют важную роль в делении клеток, защите, определении формы и полярности у различных прокариот.
FtsZ, первый идентифицированный прокариотический цитоскелетный элемент, образует нитевидную кольцевую структуру, расположенную в середине клетки, называемую Z-кольцом, которое сжимается во время деления клетки, подобно сократительному кольцу актин-миозина у эукариот. Z-кольцо представляет собой высокодинамичную структуру, которая состоит из многочисленных пучков протофиламентов, которые расширяются и сжимаются, хотя механизм сокращения Z-кольца и количество вовлеченных протофиламентов неясны. FtsZ действует как белок-организатор и необходим для деления клеток. Это первый компонент перегородки во время цитокинеза, и он привлекает все другие известные белки клеточного деления к участку деления.
Несмотря на это функциональное сходство с актин, FtsZ гомологичен эукариальному тубулину. Хотя сравнение первичных структур FtsZ и тубулина показывает слабую взаимосвязь, их трехмерные структуры удивительно похожи. Кроме того, как тубулин, мономерный FtsZ связывается с GTP и полимеризуется с другими мономерами FtsZ с гидролизом GTP по механизму, аналогичному димеризации тубулина. Поскольку FtsZ необходим для деления клеток у бактерий, этот белок является мишенью для разработки новых антибиотиков. В настоящее время существует несколько моделей и механизмов, которые регулируют образование Z-кольца, но эти механизмы зависят от вида. Несколько видов палочкообразных, включая Escherichia coli и Caulobacter crescentus, используют один или несколько ингибиторов сборки FtsZ, которые образуют биполярный градиент в клетке, усиливая полимеризацию FtsZ в центре клетки. Одна из этих систем, образующих градиент, состоит из белков MinCDE (см. Ниже).
MreB представляет собой бактериальный белок, который считается аналогом эукариального актина. MreB и актин имеют слабое соответствие первичной структуры, но очень похожи с точки зрения трехмерной структуры и полимеризации филаментов.
Почти все несферические бактерии полагаются на MreB для определения своей формы. MreB собирается в спиральную сеть нитевидных структур прямо под цитоплазматической мембраной, покрывая всю длину клетки. MreB определяет форму клетки, опосредуя положение и активность ферментов, которые синтезируют пептидогликан, и действуя как жесткая нить под клеточной мембраной, которая оказывает давление наружу, чтобы сформировать и укрепить клетку. MreB конденсируется из своей нормальной спиральной сети и образует плотное кольцо на перегородке в Caulobacter crescentus прямо перед делением клетки, механизм, который, как полагают, помогает определить местонахождение перегородки, смещенной от центра. MreB также важен для определения полярности у полярных бактерий, поскольку он отвечает за правильное расположение по крайней мере четырех различных полярных белков у C. crescentus.
Crescentin (кодируется геном creS) является аналогом эукариотических промежуточных филаментов (IFs). В отличие от других аналогичных взаимосвязей, обсуждаемых здесь, crescentin имеет довольно большую первичную гомологию с белками IF в дополнение к трехмерному сходству - последовательность creS имеет 25% идентичность и 40% сходство с цитокератином 19 и совпадение на 24% и сходство на 40% с ядерным ламином A. Кроме того, филаменты сресцентина имеют диаметр примерно 10 нм и, таким образом, попадают в диапазон диаметров эукариальных IF (8-15 нм). Кресцентин образует непрерывную нить от полюса к полюсу вдоль внутренней вогнутой стороны бактерии в форме полумесяца Caulobacter crescentus. И MreB, и crescentin необходимы C. crescentus для существования в его характерной форме; Считается, что MreB придает клетке форму стержня, а серпентин изгибает эту форму в форме полумесяца.
ParM представляет собой элемент цитоскелета, который имеет структуру, аналогичную актин, хотя функционально он ведет себя как тубулин. Кроме того, он полимеризуется в двух направлениях и проявляет динамическую нестабильность, которые являются поведением, характерным для полимеризации тубулина. Он образует систему с ParR и parC, которая отвечает за разделение плазмиды R1. ParM прикрепляется к ParR, ДНК-связывающему белку, который специфически связывается с 10 прямыми повторами в области parC на плазмиде R1. Это связывание происходит на обоих концах нити ParM. Затем эта нить удлиняется, разделяя плазмиды. Система аналогична эукариотической сегрегации хромосом, поскольку ParM действует как эукариотический тубулин в митотическом веретене, ParR действует как комплекс кинетохора, а parC действует как центромера хромосомы. сегрегация плазмиды F происходит в аналогичной системе, где SopA действует как филамент цитоскелета, а SopB связывается с последовательностью sopC в плазмиде F, как кинетохора и центромера соответственно. Недавно актиноподобный гомолог ParM был обнаружен в грамположительной бактерии Bacillus thuringiensis, которая собирается в микротрубочеподобную структуру и участвует в плазмиде сегрегация.
Система MinCDE - это система волокон, которая правильно позиционирует перегородку в середине ячейки в Escherichia coli. Согласно Shih et al., MinC ингибирует образование перегородки, запрещая полимеризацию Z-кольца. MinC, MinD и MinE образуют спиральную структуру, которая наматывается вокруг клетки и связывается с мембраной с помощью MinD. Спираль MinCDE занимает полюс и оканчивается нитевидной структурой, называемой E-кольцом, сделанной из MinE, на самом среднем краю полярной зоны. В этой конфигурации E-кольцо будет сжиматься и двигаться к этому полюсу, разбирая спираль MinCDE по мере ее движения. Одновременно разобранные фрагменты снова соберутся на противоположном полярном конце, преобразовав катушку MinCDE на противоположном полюсе, в то время как текущая спираль MinCDE будет разрушена. Затем этот процесс повторяется, спираль MinCDE колеблется от полюса к полюсу. Это колебание происходит неоднократно в течение клеточного цикла, таким образом поддерживая MinC (и его эффект ингибирования перегородки) на более низком уровне усредненной по времени концентрации в середине клетки, чем на концах клетки.
Динамическое поведение клетки Белки Min были реконструированы in vitro с использованием искусственного липидного бислоя в качестве имитации клеточной мембраны. MinE и MinD самоорганизуются в параллельные и спиральные белковые волны посредством механизма реакции-диффузии.
Бактофилин (InterPro : IPR007607 ) представляет собой цитоскелетный элемент, который образует волокна в клетках палочковидной протеобактерии Myxococcus xanthus. Белок бактофилин, BacM, необходим для поддержания правильной формы клетки и целостности клеточной стенки. Клетки M. xanthus, лишенные BacM, имеют деформированную морфологию, характеризующуюся изогнутым клеточным телом, а мутанты bacM обладают пониженной устойчивостью к антибиотикам, направленным на стенку бактериальной клетки. Белок M. xanthus BacM отщепляется от его полноразмерной формы, чтобы обеспечить полимеризацию. Бактофилины участвуют в регуляции формы клеток у других бактерий, включая искривление клеток Proteus mirabilis, формирование стебля Caulobacter crescentus и спиралевидную форму Helicobacter pylori.
Кренактин - это гомолог актина, уникальный для царства архей Crenarchaeota, который был обнаружен в отрядах Thermoproteales и Candidatus Korarchaeum. Он имеет самое высокое сходство последовательностей с эукариотическими актинами из всех известных гомологов актина. Кренактин хорошо охарактеризован у Pyryobaculum calidifontis (A3MWN5 ), и было показано, что он обладает высокой специфичностью к АТФ и ГТФ. Все виды, содержащие кренактин, имеют форму стержня или иглы, а у P. calidifontis было показано, что кренактин образует спиральные структуры, охватывающие длину клетки, что предполагает роль кренактина в определении формы, аналогичную роли MreB у других прокариот.
Внутри филума спирохеты ряд видов разделяет нитевидную цитоплазматическую ленточную структуру, образованную отдельными филаментами, состоящими из белка CfpA (Cytoplasmic filament protein A, Q56336 ), соединенные между собой соединительными элементами и анкерами с внутренней мембраной. Хотя они присутствуют в родах Treponema, Spirochaeta, Pillotina, Leptonema, Hollandina и Diplocalyx, они, однако, отсутствуют у некоторых видов, как в примере Treponema primitia. При размере поперечного сечения 5 x 6 нм (горизонтально / вертикально) они попадают в диапазон диаметров эукариальных промежуточных филаментов (IF) (8-15 нм). Treponema denticola, лишенные белка CfpA, образуют длинные сцепленные клетки с дефектом сегрегации хромосомной ДНК, фенотип, также влияющий на патогенность этого организма. Отсутствие другой ультраструктуры клетки, пучка филаментов периплазматических жгутиков, не изменяет структуру цитоплазматической ленты.