 Промежуточные филаменты кератина в эпителиальных клетках (красное пятно).
Промежуточные филаменты кератина в эпителиальных клетках (красное пятно). Цитокератины - это кератин белки, обнаруженные в внутрицитоплазматическом цитоскелете эпителиальной ткани. Они являются важным компонентом промежуточных волокон, которые помогают клеткам противостоять механическим воздействиям. Экспрессия этих цитокератинов в эпителиальных клетках в значительной степени специфична для конкретных органов или тканей. Таким образом, они используются в клинической практике для определения клетки происхождения различных опухолей человека.
Термин " цитокератин »начали использовать в конце 1970-х годов, когда впервые были идентифицированы и охарактеризованы белковые субъединицы кератиновых промежуточных филаментов внутри клеток. В 2006 году была создана новая систематическая номенклатура кератинов млекопитающих, а белки, ранее называемые «цитокератинами», просто называются кератинами (категория эпителия человека). Например, цитокератин-4 (CK-4) был переименован в кератин-4 (K4). Однако в клинической практике они по-прежнему часто называют цитокератинами.
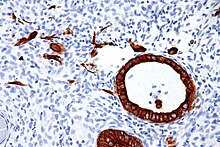 Микрофотография, показывающая окрашивание низкомолекулярным цитокератином (LMWCK) промежуточного трофобласта (плацентарная ткань ) и эндометриальных желез.
Микрофотография, показывающая окрашивание низкомолекулярным цитокератином (LMWCK) промежуточного трофобласта (плацентарная ткань ) и эндометриальных желез. Там представляют собой две категории цитокератинов: кислые цитокератины типа I и основные или нейтральные цитокератины типа II. Внутри каждой категории цитокератины пронумерованы в порядке убывания размера от низкомолекулярного (LMWCK) до высокомолекулярного (HMWCK). Цитокератины обычно находятся в гетеродимерных парах кислотных и основных субъединиц одинакового размера.
| Основные CK. (Тип B / Класс II) | Кислые CK. (Тип A / Класс I) | |
|---|---|---|
| HMWCK. «плоские кератины» | CK-1. CK-2. CK-3. CK-4. CK-5. CK-6 | CK -9. CK-10. CK-11. CK-12. CK-13. CK-14. CK-15. CK-16. CK-17 |
| LMWCK. "простые кератины" | CK-7. CK-8 | CK-18. CK-19. CK-20 |
Экспрессия этих цитокератинов в значительной степени зависит от органа или ткани. Подмножества цитокератинов, которые экспрессируются эпителиальной клеткой, в основном зависят от типа эпителия, момента терминальной дифференцировки и стадии развития. Таким образом, определенный профиль экспрессии цитокератина позволяет идентифицировать эпителиальные клетки. Кроме того, это относится также к злокачественным аналогам эпителия (карциномы ), так как профиль цитокератина обычно сохраняется. Таким образом, изучение экспрессии цитокератина с помощью методов иммуногистохимии является чрезвычайно ценным инструментом, широко используемым для диагностики и характеристики опухолей при хирургической патологии.
| Цитокератин | Сайты |
|---|---|
| Цитокератин 4 |
|
| Цитокератин 7 |
|
| Цитокератин 8 |
|
| Цитокератин 10 |
|
| Цитокератин 13 |
|
| Цитокератин 14 |
|
| цитокератина 18 |
|
| Цитокератин 19 |
Не реагирует с гепатоцитами и гепатоцеллюлярной карциномой |
| Cytokeratin 20 |
|
Цитокератины кодируются семейством, состоящим из 30 генов. Среди них 20 - эпителиальные гены и остальные 10 специфичны для трихоцитов.
Все цепи цитокератина состоят из центрального богатого α-спиралями домена (с 50-90% идентичностью последовательностей среди цитокератинов одного типа и примерно 30% между цитокератинами другой тип) с не-α-спиральными N- и С-концевыми доменами. α-спиральный домен состоит из 310-150 аминокислот и включает четыре сегмента, в которых повторяется паттерн из семи остатков. В этом повторяющемся паттерне первый и четвертый остатки гидрофобны, а заряженные остатки демонстрируют чередующуюся положительную и отрицательную полярность, в результате чего полярные остатки располагаются на одной стороне спирали. Этот центральный домен цепи обеспечивает выравнивание молекул в структуре кератина и заставляет цепи образовывать спиральные димеры в решение.
Конец домаи n последовательностей цепей цитокератина типа I и II содержат с обеих сторон стержневого домена субдомены V1 и V2, которые имеют переменный размер и последовательность. Тип II также представлен консервативными субдоменами H1 и H2, включающими 36 и 20 остатков соответственно. Субдомены V1 и V2 содержат остатки, обогащенные глицинами и / или серинами, причем первые придают цитокератиновой цепи сильный нерастворимый характер и облегчают взаимодействие с другими молекулами. Эти концевые домены также важны для определения функции цитокератиновой цепи, характерной для определенного типа эпителиальных клеток.
Два димера цитокератиновой группы превращаются в тетрамер кератина путем антипараллельного связывания. Этот тетрамер цитокератина считается основным строительным блоком цитокератиновой цепи. Путем соединения тетрамеров цитокератина голова-хвост образуются протофиламенты, которые, в свою очередь, попарно переплетаются с образованием протофибрилл. Четыре протофибриллы уступают место одной цитокератиновой нити.
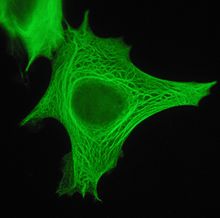 Цитокератиновые нити в эпителиальной клетке человека
Цитокератиновые нити в эпителиальной клетке человека В цитоплазме кератиновые нити образуют сложную сеть, которая простирается от поверхности ядра до клеточной мембраны. Многочисленные дополнительные белки участвуют в возникновении и поддержании такой структуры.
Эта ассоциация между плазматической мембраной и поверхностью ядра обеспечивает важные последствия для организации цитоплазмы и механизмов клеточной коммуникации. Помимо относительно статических функций, обеспечиваемых с точки зрения поддержки ядра и обеспечения прочности на разрыв клетки, сети цитокератина подвергаются быстрому фосфатному обмену, опосредованному деполимеризацией, что имеет важные последствия для более динамичных клеточных процессов, таких как митоз и постмитотический период, клетка движение и дифференцировка.
Цитокератины взаимодействуют с десмосомами и гемидесмосомами, таким образом взаимодействуя с клеточно-клеточной адгезией и соединительной тканью, лежащей в основе базальных клеток.
Промежуточные филаменты эукариотического цитоскелета, которые цитокератины являются одним из трех его компонентов, также были исследованы на предмет ассоциации с белковой сетью комплекса анкирина и спектрина.