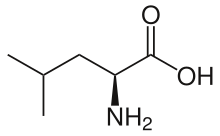
 . L-Лейцин . L-Лейцин | |
 | |
| Имена | |
|---|---|
| Имя IUPAC Лейцин | |
| Другие имена 2-амино-4-метилпентановая кислота | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.475 |
| IUPHAR/BPS | |
| KEGG | |
| PubChem CID | |
| UNII | |
| CompTox Dashboard ( EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C6H13NO2 |
| Молярная масса | 131 0,175 г · моль |
| Кислотность (pK a) | 2,36 (карбоксил), 9,60 (амино) |
| Магнитная восприимчивость (χ) | -84,9 · 10 см / моль |
| Страница дополнительных данных | |
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая постоянная (εr) и т. Д. |
| Термодинамические. данные | Фазовое поведение. твердое тело – жидкость – газ |
| Спектральные данные | UV, IR, ЯМР, MS |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в информационном окне | |
лейцин (символ Leu или L ) представляет собой незаменимую аминокислоту, которая используется в биосинтезе белков. Лейцин является α-аминокислотой, что означает, что он содержит α- аминогруппу (которая находится в протонированной форме -NH 3 в биологических условиях), α- карбоксильную группу. кислотная группа (которая находится в депротонированной форме -COO в биологических условиях) и боковая цепь изобутильная группа, что делает ее неполярной алифатической аминокислота. Он необходим для человека, то есть организм не может его синтезировать: он должен быть получен с пищей. Источники питания человека - это продукты, содержащие белок, такие как мясо, молочные продукты, соевые продукты, бобы и другие бобовые. Он кодируется кодонами UUA, UUG, CUU, CUC, CUA и CUG.
Подобно валину и изолейцину, лейцин представляет собой аминокислоту с разветвленной цепью. Основными конечными продуктами метаболизма метаболизма лейцина являются ацетил-КоА и ацетоацетат ; следовательно, это одна из двух исключительно кетогенных аминокислот, а лизин является другой. Это наиболее важная кетогенная аминокислота для человека.
Лейцин и β-гидрокси β-метилмасляная кислота, минорный метаболит лейцина , проявляют фармакологическую активность у людей, и было продемонстрировано, что они способствуют биосинтезу белка посредством фосфорилирования механистической мишени рапамицина (mTOR).
В качестве пищевой добавки, L-лейцин имеет номер E E641 и классифицируется как усилитель вкуса.
Совет по пищевым продуктам и питанию (FNB) Институт медицины США установил Рекомендуемые диетические нормы (RDA) для незаменимых аминокислот в 2002 году. эуцин, для взрослых 19 лет и старше, 42 мг / кг массы тела / день.
| Пища | г / 100 г |
|---|---|
| Сывороточный протеин концентрат, сухой порошок | 10,0-12,0 |
| Концентрат соевого белка, сухой порошок | 7,5-8,5 |
| Концентрат горохового белка, сухой порошок | 6,6 |
| Соя, зрелые семена, обжаренные, соленые | 2,87 |
| Семена конопли лущеные | 2,16 |
| Говядина, круглая, верхняя круглая, сырая | 1,76 |
| Арахис | 1,67 |
| Рыба, лосось, розовый, сырой | 1,62 |
| Зародыши пшеницы | 1,57 |
| Миндаль | 1,49 |
| Цыпленок, бройлеры или фритюрницы, бедро, сырое | 1,48 |
| Куриное яйцо, желток, сырое | 1,40 |
| Овес | 1,28 |
| Эдамаме (соевые бобы, зеленые, сырые) | 0,93 |
| Фасоль, пинто, приготовленная | 0,78 |
| Чечевица, вареный | 0,65 |
| Нут, вареный | 0,63 |
| Кукуруза, желтый | 0,35 |
| Коровье молоко, цельное, 3,25% молочного жира | 0,27 |
| Ri ce, коричневое, среднезернистое, вареное | 0,19 |
| Молоко, человеческое, зрелое, жидкое | 0,10 |
Было обнаружено, что в качестве пищевой добавки лейцин замедляет деградацию мышечной ткани за счет увеличения синтеза мышечных белков у старых крыс. Однако результаты сравнительных исследований противоречивы. Длительный прием лейцина не увеличивает мышечную массу или силу у здоровых пожилых мужчин. Необходимы дополнительные исследования, желательно основанные на объективной случайной выборке общества. Такие факторы, как выбор образа жизни, возраст, пол, диета, физические упражнения и т. Д., Должны быть учтены в анализах, чтобы изолировать эффекты дополнительного лейцина как отдельного препарата или его приема с другими аминокислотами с разветвленной цепью (BCAA).). До тех пор лейцин нельзя считать основной причиной мышечного роста или оптимального поддержания здоровья для всего населения.
И L-лейцин, и D-лейцин защищают мышей от судорог. D-лейцин также прекращает судороги у мышей после начала судорожной активности, по крайней мере так же эффективно, как диазепам, и без седативных эффектов. Сниженное потребление L-лейцина с пищей способствует ожирению у мышей. Высокий уровень лейцина в крови связан с инсулинорезистентностью у людей, мышей и грызунов. Это может быть связано с действием лейцина на стимуляцию передачи сигналов mTOR. Диетическое ограничение лейцина и других BCAA может обратить вспять вызванное диетой ожирение у мышей дикого типа за счет увеличения расхода энергии и может ограничить набор жировой массы у гиперфагических крыс.
Токсичность лейцина, как видно из декомпенсированной болезни мочи кленовым сиропом, вызывает делирий и неврологические нарушения и может быть опасным для жизни.
Высокое потребление лейцина может вызвать или усугубить симптомы пеллагры у людей с низким статусом ниацина, поскольку он препятствует превращению L-триптофана в ниацин.
Лейцин в дозе, превышающей 500 мг / кг / день наблюдалась с гипераммониемией. Таким образом, неофициально допустимый верхний уровень потребления (UL) лейцина у здоровых взрослых мужчин может быть предложен на уровне 500 мг / кг / день или 35 г / день при острых диетических условиях.
Лейцин - это пищевая аминокислота со способностью напрямую стимулировать синтез миофибриллярного мышечного белка. Этот эффект лейцина является результатом его роли как активатора механистической мишени рапамицина (mTOR), серин-треониновой протеинкиназы, которая регулирует биосинтез белка и рост клеток. Активация mTOR лейцином опосредуется Rag GTPases, связыванием лейцина с лейцил-тРНК-синтетазой, связыванием лейцина с сестрином 2, и, возможно, другие механизмы.
Метаболизм лейцина происходит во многих тканях человеческого тела ; однако большая часть диетического лейцина метаболизируется в печени, жировой ткани и мышечной ткани. Жировая и мышечная ткань использует лейцин для образования стеролов и других соединений. Комбинированное использование лейцина в этих двух тканях в семь раз больше, чем в печени.
У здоровых людей примерно 60% диетического L-лейцина метаболизируется через несколько часов, причем примерно 5% (диапазон 2–10%) диетического L-лейцин превращается в β-гидрокси β-метилмасляную кислоту (HMB). Около 40% диетического L-лейцина превращается в ацетил-КоА, который впоследствии используется в синтезе других соединений.
Подавляющее большинство метаболизма L-лейцина первоначально катализируется аминокислотой с разветвленной цепью фермент аминотрансфераза, продуцирующий α-кетоизокапроат (α-KIC). α-KIC в основном метаболизируется митохондриальным ферментом дегидрогеназой α-кетокислоты с разветвленной цепью, который превращает его в изовалерил-КоА. Изовалерил-КоА впоследствии метаболизируется изовалерил-КоА дегидрогеназой и превращается в МС-КоА, который используется в синтезе ацетил-КоА и других соединений. Во время дефицита биотина HMB может быть синтезирован из MC-CoA через еноил-CoA гидратазу и неизвестный фермент тиоэстеразу, которые превращают MC-CoA в HMB-CoA. и HMB-CoA в HMB соответственно. Относительно небольшое количество α-KIC метаболизируется в печени с помощью цитозольного фермента 4-гидроксифенилпируватдиоксигеназы (KIC-диоксигеназа), который превращает α-KIC в HMB. У здоровых людей этот второстепенный путь - который включает превращение L-лейцина в α-KIC, а затем HMB - является преобладающим путем синтеза HMB.Небольшая часть метаболизма L-лейцина - всего менее 5% ткани, за исключением семенников, где он составляет около 33% - первоначально катализируется лейцинаминомутазой, производя β-лейцин, который впоследствии метаболизируется в β-кетоизокапроат (β-KIC), а затем ацетил-КоА с помощью ряда не охарактеризованных ферментов.
Метаболизм HMB катализируется не охарактеризованным ферментом, который превращает его в β-гидрокси β-метилбутирил-КоА (HMB-CoA). HMB-CoA метаболизируется еноил-CoA гидратазой или другим не охарактеризованным ферментом, продуцируя β-метилкротонил-CoA (MC-CoA) или гидроксиметилглутарил-CoA ( HMG-CoA) соответственно. Затем MC-CoA превращается ферментом метилкротонил-CoA-карбоксилазой в метилглутаконил-CoA (MG-CoA), который впоследствии превращается в HMG-CoA с помощью метилглутаконил-CoA. гидратаза. Затем HMG-CoA расщепляется на ацетил-CoA и ацетоацетат с помощью HMG-CoA лиазы или используется в производстве холестерина через мевалонатный путь.
Лейцин является незаменимой аминокислотой в рационе животных, потому что у них отсутствует полный ферментный путь для его синтеза de novo из потенциальных соединений-предшественников. Следовательно, они должны принимать его внутрь, обычно как компонент белков. Растения и микроорганизмы синтезируют лейцин из пировиноградной кислоты с помощью ряда ферментов:
Синтез небольшой гидрофобной аминокислоты валин также включает начальную часть этого пути.
 (S) -Лейцин (или L -лейцин), слева; (R) -лейцин (или D -лейцин), справа, в цвиттерионной форме при нейтральном pH
(S) -Лейцин (или L -лейцин), слева; (R) -лейцин (или D -лейцин), справа, в цвиттерионной форме при нейтральном pH Лейцин представляет собой аминокислоту с разветвленной цепью (BCAA), поскольку он обладает алифатическим содержанием Боковая цепь, которая не является линейной.
Рацемический лейцин подвергали циркулярно поляризованной синхротронной радиации, чтобы лучше понять происхождение биомолекулярной асимметрии. Было индуцировано энантиомерное повышение на 2,6%, что указывает на возможное фотохимическое происхождение гомохиральности биомолекул.