Изомеразы - это общий класс ферментов, которые превращают молекулу из одного изомера в другой. Изомеразы способствуют внутримолекулярным перегруппировкам, в которых связи разрываются и образуются. Общая форма такой реакции следующая:
А – Б → Б – А
Есть только один субстрат, дающий один продукт. Этот продукт имеет ту же молекулярную формулу, что и субстрат, но отличается связностью соединений или пространственным расположением. Изомеразы катализируют реакции во многих биологических процессах, например, в гликолизе и углеводном обмене.
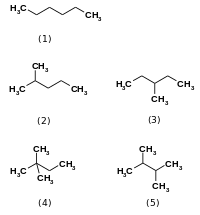 Структурные изомеры гексана
Структурные изомеры гексана  Цис-2-бутен и транс-2-бутен
Цис-2-бутен и транс-2-бутен 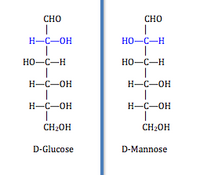 Эпимеры: D-глюкоза и D-манноза
Эпимеры: D-глюкоза и D-манноза Изомеразы катализируют изменения внутри одной молекулы. Они превращают один изомер в другой, что означает, что конечный продукт имеет ту же молекулярную формулу, но другую физическую структуру. Сами изомеры существуют во многих разновидностях, но обычно их можно классифицировать как структурные изомеры или стереоизомеры. Структурные изомеры имеют разный порядок связей и / или разную связность связей друг с другом, как в случае гексана и его четырех других изомерных форм ( 2-метилпентан, 3-метилпентан, 2,2-диметилбутан и 2,3 -метилпентан). диметилбутан ).
Стереоизомеры имеют одинаковый порядок отдельных связей и такую же связность, но трехмерное расположение связанных атомов различается. Например, 2-бутен существует в двух изомерных формах: цис- 2-бутен и транс- 2-бутен. Подкатегории изомераз, содержащие рацемазы, эпимеразы и цис-транс-изомеры, являются примерами ферментов, катализирующих взаимное превращение стереоизомеров. Внутримолекулярные лиазы, оксидоредуктазы и трансферазы катализируют взаимное превращение структурных изомеров.
Преобладание каждого изомера в природе частично зависит от энергии изомеризации, разницы в энергии между изомерами. Близкие по энергии изомеры могут легко преобразовываться друг в друга, и их часто можно увидеть в сопоставимых пропорциях. Энергия изомеризации, например, для превращения стабильного цис- изомера в менее стабильный транс- изомер больше, чем для обратной реакции, что объясняет, почему в отсутствие изомераз или внешнего источника энергии, такого как ультрафиолетовое излучение, данный цис- изомер имеет тенденцию к присутствовать в больших количествах, чем транс- изомер. Изомеразы могут увеличивать скорость реакции за счет снижения энергии изомеризации.
Расчет кинетики изомеразы на основе экспериментальных данных может быть более трудным, чем для других ферментов, потому что использование экспериментов по ингибированию продукта нецелесообразно. То есть изомеризация не является необратимой реакцией, поскольку реакционный сосуд будет содержать один субстрат и один продукт, поэтому типичная упрощенная модель для расчета кинетики реакции не работает. Существуют также практические трудности при определении стадии, определяющей скорость при высоких концентрациях при однократной изомеризации. Вместо этого с помощью индикатора можно преодолеть эти технические трудности, если существует две формы несвязанного фермента. Этот метод использует изотопный обмен для косвенного измерения взаимного превращения свободного фермента между двумя его формами. Субстрат и продукт с радиоактивной меткой диффундируют в зависимости от времени. Когда система достигает равновесия, добавление немеченого субстрата нарушает или нарушает баланс. Когда снова устанавливается равновесие, радиоактивно меченные субстрат и продукт отслеживаются для определения энергетической информации.
Самое раннее использование этого метода прояснило кинетику и механизм, лежащие в основе действия фосфоглюкомутазы, в пользу модели непрямого переноса фосфата с одним промежуточным соединением и прямого переноса глюкозы. Затем этот метод был использован для изучения профиля пролин-рацемазы и двух ее состояний: формы, изомеризующей L- пролин, и другой формы для D-пролина. При высоких концентрациях было показано, что переход состояния в этом взаимопревращения является ограничивающим скорость, и что эти формы фермента могут отличаться только в протонирования в кислотных и основных групп в активном центре.
Обычно «названия изомераз образуются как« субстратная изомераза »(например, еноил-КоА-изомераза ) или как« субстратный тип изомеразы »(например, фосфоглюкомутаза )».
Каждой реакции, катализируемой ферментами, присвоен уникальный классификационный номер. Катализируемые изомеразой реакции имеют свою собственную категорию ЕС : ЕС 5. Изомеразы далее подразделяются на шесть подклассов:
Эта категория (EC 5.1) включает ( рацемазы ) и эпимеразы ). Эти изомеразы инвертируют стереохимию целевого хирального углерода. Рацемазы воздействуют на молекулы с одним хиральным атомом углерода для инверсии стереохимии, тогда как эпимеразы воздействуют на молекулы-мишени с несколькими хиральными атомами углерода и воздействуют на один из них. Молекула только с одним хиральным углеродом имеет две энантиомерные формы, такие как серин, имеющий изоформы D-серина и L-серина, отличающиеся только абсолютной конфигурацией хирального углерода. Молекула с несколькими хиральными атомами углерода имеет две формы у каждого хирального углерода. Изомеризация нескольких хиральных атомов углерода дает эпимеры, которые отличаются друг от друга по абсолютной конфигурации только у одного хирального углерода. Например, D- глюкоза и D- манноза различаются по конфигурации только у одного хирального атома углерода. Этот класс далее подразделяется на группу, на которую действует фермент:
| Номер ЕС | Описание | Примеры |
|---|---|---|
| EC 5.1.1 | Воздействие на аминокислоты и производные | аланин рацемаза, метионин рацемаза |
| EC 5.1.2 | Воздействие на оксикислоты и производные | лактатрацемаза, тартрат-эпимераза |
| EC 5.1.3 | Воздействие на углеводы и производные | рибулозо-фосфат-3-эпимераза, UDP-глюкозо-4-эпимераза |
| 5.1.99 EC | Воздействие на другие соединения | метилмалонил-КоА эпимераза, гидантоин рацемаза |
В эту категорию (EC 5.2) входят ферменты, катализирующие изомеризацию цис-транс-изомеров. Алкены и циклоалканы могут иметь цис-транс стереоизомеры. Эти изомеры различаются не абсолютной конфигурацией, а скорее положением групп заместителей относительно плоскости отсчета, как поперек двойной связи, так и относительно кольцевой структуры. Цис- изомеры имеют группы заместителей на одной стороне, а транс- изомеры имеют группы на противоположных сторонах.
Эта категория больше не разбивается. Все записи в настоящее время включают:
 Конверсия опосредована пептидилпролилизомеразой (PPIase).
Конверсия опосредована пептидилпролилизомеразой (PPIase). | Номер ЕС | Примеры |
|---|---|
| EC 5.2.1.1 | Малеат изомераза |
| EC 5.2.1.2 | Малеилацетоацетат изомераза |
| EC 5.2.1.4 | Малеилпируват изомераза |
| EC 5.2.1.5 | Линолеат-изомераза |
| EC 5.2.1.6 | Фурилфурамид изомераза |
| EC 5.2.1.8 | Пептидилпролилизомераза |
| EC 5.2.1.9 | Фарнезол 2-изомераза |
| EC 5.2.1.10 | 2-хлор-4-карбоксиметиленбут-2-ен-1,4-олидизомераза |
| EC 5.2.1.12 | Зета-каротин изомераза |
| EC 5.2.1.13 | Проликопен изомераза |
| EC 5.2.1.14 | Бета-каротин изомераза |
В эту категорию (EC 5.3) входят внутримолекулярные оксидоредуктазы. Эти изомеразы катализируют перенос электронов от одной части молекулы к другой. Другими словами, они катализируют окисление одной части молекулы и одновременное восстановление другой части. Подкатегории этого класса:
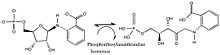 реакция, катализируемая фосфорибозилантранилат-изомеразой
реакция, катализируемая фосфорибозилантранилат-изомеразой | Номер ЕС | Описание | Примеры |
|---|---|---|
| EC 5.3.1 | Взаимопревращение альдозов и кетозов | Триозо-фосфат-изомераза, Рибозо-5-фосфат-изомераза |
| EC 5.3.2 | Взаимопревращение кето- и енольных групп | Фенилпируваттаутомераза, Оксалоацетаттаутомераза |
| EC 5.3.3 | Транспонирование двойных облигаций C = C | Стероид-дельта-изомераза, L-допахром-изомераза |
| EC 5.3.4 | Транспонирование облигаций ГЦБ | Белковая дисульфид-изомераза |
| EC 5.3.99 | Другие внутримолекулярные оксидоредуктазы | Простагландин-D-синтаза, алленоксидциклаза |
В эту категорию (EC 5.4) входят внутримолекулярные трансферазы ( мутазы ). Эти изомеразы катализируют перенос функциональных групп от одной части молекулы к другой. Фосфотрансферазы (EC 5.4.2) были классифицированы как трансферазы (EC 2.7.5) с регенерацией доноров до 1983 года. Этот подкласс можно разделить в соответствии с функциональной группой, переносимой ферментом:
 реакция, катализируемая фосфоенолпируватмутазой
реакция, катализируемая фосфоенолпируватмутазой | Номер ЕС | Описание | Примеры |
|---|---|---|
| EC 5.4.1 | Перенос ацильных групп | Лизолецитинацилмутаза, Прекоррин-8X метилмутаза |
| EC 5.4.2 | Фосфотрансферазы (фосфомутазы) | Фосфоглюкомутаза, Фосфопентомутаза |
| EC 5.4.3 | Перенос аминокислотных групп | Бета-лизин 5,6-аминомутаза, тирозин 2,3-аминомутаза |
| EC 5.4.4 | Перенос гидроксигрупп | (гидроксиамино) бензолмутаза, изохоризматсинтаза |
| 5.4.99 по К.Э. | Перенос других групп | Метиласпартатмутаза, хоризматмутаза |
Эта категория (EC 5.5) включает внутримолекулярные лиазы. Эти ферменты катализируют «реакции, в которых группа может считаться удаленной из одной части молекулы, оставляя двойную связь, оставаясь ковалентно присоединенной к молекуле». Некоторые из этих катализируемых реакций включают разрыв кольцевой структуры.
Эта категория больше не разбивается. Все записи в настоящее время включают:
| Номер ЕС | Примеры |
|---|---|
| EC 5.5.1.1 | Муконат циклоизомераза |
| EC 5.5.1.2 | 3-карбокси-цис, цис-муконатциклоизомераза |
| EC 5.5.1.3 | Тетрагидроксиптеридин циклоизомераза |
| EC 5.5.1.4 | Инозитол-3-фосфатсинтаза |
| EC 5.5.1.5 | Карбокси-цис, цис-муконатциклаза |
| EC 5.5.1.6 | Халкон-изомераза |
| EC 5.5.1.7 | Хлормуконат циклоизомераза |
| EC 5.5.1.8 | (+) - борнилдифосфатсинтаза |
| EC 5.5.1.9 | Циклоэукаленол циклоизомераза |
| EC 5.5.1.10 | Альфа-пинен-оксид дециклаза |
| EC 5.5.1.11 | Дихлормуконат циклоизомераза |
| EC 5.5.1.12 | Копалилдифосфатсинтаза |
| EC 5.5.1.13 | Энт-копалилдифосфатсинтаза |
| EC 5.5.1.14 | Син-копалил-дифосфат-синтаза |
| EC 5.5.1.15 | Терпентиенил-дифосфатсинтаза |
| EC 5.5.1.16 | Галимадиенил-дифосфатсинтаза |
| EC 5.5.1.17 | (S) -бета-макрокарпен-синтаза |
| EC 5.5.1.18 | Ликопин-эпсилон-циклаза |
| EC 5.5.1.19 | Ликопин бета-циклаза |
| EC 5.5.1.20 | Просоланапирон-III циклоизомераза |
| EC 5.5.1.n1 | D-рибозопираназа |
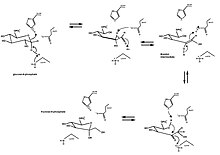 Изомеризация глюкозо-6-фосфата глюкозо-6-фосфат-изомеразой
Изомеризация глюкозо-6-фосфата глюкозо-6-фосфат-изомеразой Классическим примером раскрытия и сжатия кольца является изомеризация глюкозы ( альдегида с шестичленным кольцом) до фруктозы ( кетон с пятичленным кольцом). Превращение D-глюкозо-6-фосфата в D-фруктозо-6-фосфат катализируется глюкозо-6-фосфат-изомеразой, внутримолекулярной оксидоредуктазой. Общая реакция включает раскрытие кольца с образованием альдозы посредством кислотно-основного катализа и последующее образование промежуточного цис-эндиола. Затем образуется кетоза, и кольцо снова замыкается.
Глюкозо-6-фосфат сначала связывается с активным центром изомеразы. Изомераза открывает кольцо: его остаток His388 протонирует кислород на кольце глюкозы (и тем самым разрывает связь O5-C1) вместе с Lys518, депротонируя гидроксильный кислород C1. Кольцо открывается, образуя альдозу с прямой цепью с кислым протоном C2. Связь C3-C4 вращается, и Glu357 (с помощью His388) депронизирует C2 с образованием двойной связи между C1 и C2. Цис-endiol промежуточного соединения создаются и С1 кислород протонируются путем каталитического остатка, сопровождаются депротонирования endiol C2 кислорода. Образуется кетоза с прямой цепью. Чтобы замкнуть фруктозное кольцо, происходит обратное раскрытие кольца, и кетоза протонируется.
 Превращение рибулозо-5-фосфата в ксилулозо-5-фосфат
Превращение рибулозо-5-фосфата в ксилулозо-5-фосфат Пример эпимеризации находится в цикле Кальвина, когда D-рибулозо-5-фосфат превращается в D-ксилулозо-5-фосфат с помощью рибулозо-фосфат-3-эпимеразы. Субстрат и продукт различаются только стереохимией у третьего атома углерода в цепи. Основной механизм включает депротонирование этого третьего углерода с образованием реакционноспособного енолятного промежуточного соединения. Активный центр фермента содержит два остатка Asp. После связывания субстрата с ферментом первый Asp депротонирует третий углерод с одной стороны молекулы. Это оставляет планарный sp 2 -гибридизированный промежуточный продукт. Второй Asp расположен на противоположной стороне активной стороны и протонирует молекулу, эффективно добавляя протон с обратной стороны. Эти связанные шаги инвертируют стереохимию у третьего углерода.
 Предлагаемый механизм хоризматмутазы. Кларк, Т., Стюарт, Дж. Д. и Ганем, Б. Аналоги-ингибиторы переходного состояния хлоризматмутазы. Тетраэдр 46 (1990) 731–748. © IUBMB 2001
Предлагаемый механизм хоризматмутазы. Кларк, Т., Стюарт, Дж. Д. и Ганем, Б. Аналоги-ингибиторы переходного состояния хлоризматмутазы. Тетраэдр 46 (1990) 731–748. © IUBMB 2001 Хоризматмутаза - это внутримолекулярная трансфераза, катализирующая превращение хоризмата в префенат, используемый в качестве предшественника L-тирозина и L-фенилаланина в некоторых растениях и бактериях. Эта реакция представляет собой перегруппировку Клайзена, которая может протекать как с изомеразой, так и без нее, хотя скорость увеличивается в 10 6 раз в присутствии хоризматмутазы. Реакция проходит через переходное состояние кресла с субстратом в транс-диаксиальном положении. Экспериментальные данные показывают, что изомераза избирательно связывает переходное состояние кресла, хотя точный механизм катализа неизвестен. Считается, что это связывание стабилизирует переходное состояние за счет электростатических эффектов, что объясняет резкое увеличение скорости реакции в присутствии мутазы или при добавлении специально размещенного катиона в активном центре.
 Конверсия изомеразой IPP
Конверсия изомеразой IPP Изопентенил-дифосфат-дельта-изомераза типа I (также известная как IPP-изомераза) проявляется в синтезе холестерина и, в частности, катализирует превращение изопентенилдифосфата (IPP) в диметилаллилдифосфат (DMAPP). В этой реакции изомеризации стабильный углерод-углеродная двойная связь перестраивается сверху создать очень электрофильный аллильный изомер. Изомераза IPP катализирует эту реакцию стереоселективной антарафациальной транспозицией одиночного протона. Двойная связь протонируются у С4 с образованием третичного карбкатиона промежуточного у С3. Соседний углерод C2 депротонируется с противоположной стороны с образованием двойной связи. Фактически сдвигается двойная связь.
Изомераза играет важную роль в заболеваниях человека. Недостаток этого фермента может вызвать расстройства у человека.
Дефицит фосфогексозо-изомеразы (PHI) также известен как дефицит фосфоглюкозо-изомеразы или дефицит глюкозо-6-фосфат-изомеразы и является наследственным дефицитом ферментов. PHI - вторая по частоте эртоэнзиопатия при гликолизе, помимо недостаточности пируваткиназы, и связана с несфероцитарной гемолитической анемией различной степени тяжести. В основе этого заболевания лежит глюкозо-6-фосфатный белок. Этот белок можно найти в секрете некоторых раковых клеток. PHI является результатом димерного фермента, который катализирует обратимое взаимное превращение фруктозо-6-фосфата и глюозо-6-фосфата.
PHI - очень редкое заболевание, на сегодняшний день в литературе зарегистрировано только 50 случаев.
Диагноз ставится на основании клинической картины в сочетании с биохимическими исследованиями, выявляющими дефицит GPI эритроцитов (от 7 до 60% от нормы) и идентификацией мутации в гене GPI с помощью молекулярного анализа.
Дефицит изомеразы фосфогексозы может привести к состоянию, называемому гемолитическим синдромом. Как и у человека, гемолитический синдром, который характеризуется уменьшением количества эритроцитов, более низким гематокритом, более низким уровнем гемоглобина, более высоким количеством ретикулоцитов и концентрацией билирубина в плазме, а также повышенными соматическими показателями печени и селезенки, проявлялся исключительно у гомозиготных мутантов..
Заболевание, называемое дефицитом триозофосфат-изомеразы (ДПИ), является тяжелым аутосомно-рецессивным наследственным мультисистемным нарушением метаболизма гликолей. Он характеризуется гемолитической анемией и нейродегенерацией и вызывается анаэробной метаболической дисфункцией. Эта дисфункция является результатом миссенс-мутации, которая влияет на кодируемый белок TPI. Наиболее распространенной мутацией является замена гена Glu104Asp, который вызывает наиболее тяжелый фенотип и отвечает примерно за 80% клинического дефицита ТПИ.
Дефицит ТПИ встречается очень редко, в литературе описано менее 50 случаев. Поскольку это аутосомно-рецессивное наследственное заболевание, дефицит TPI имеет 25% риск рецидива в случае гетерозиготных родителей. Это врожденное заболевание, которое чаще всего проявляется гемолитической анемией и проявляется желтухой. Большинство пациентов с TPI по мутации Glu104Asp или гетерозиготными по нулевому аллелю TPI и Glu104Asp имеют ожидаемую продолжительность жизни от младенчества до раннего детства. Пациенты с TPI с другими мутациями обычно демонстрируют более длительную продолжительность жизни. На сегодняшний день зарегистрировано только два случая людей с TPI, живущих в возрасте старше 6 лет. В этих случаях участвуют два брата из Венгрии, один, у которого не развились неврологические симптомы до 12 лет, и старший брат, у которого нет неврологических симптомов и страдает только анемией.
У лиц с TPI очевидные симптомы проявляются в возрасте от 6 до 24 месяцев. Эти симптомы включают: дистонию, тремор, дискинезию, признаки пирамидного тракта, кардиомиопатию и вовлечение спинномозговых мотонейронов. У пациентов также наблюдаются частые бактериальные инфекции дыхательной системы.
TPI обнаруживается по недостаточности ферментативной активности и накоплению в эритроцитах дигироксиацетонфосфата (DHAP), который является токсичным субстратом. Это можно обнаружить при физическом осмотре и серии лабораторных работ. При обнаружении обычно наблюдаются миопатические изменения в мышцах и хроническая аксональная нейропатия в нервах. Диагноз TPI может быть подтвержден с помощью молекулярной генетики. Анализ ДНК ворсинок хориона или анализ эритроцитов плода можно использовать для выявления TPI при антенатальной диагностике.
Лечение TPI неспецифично, но варьируется в зависимости от случая. Из-за ряда симптомов, вызываемых TPI, может потребоваться группа специалистов для лечения одного человека. Эта группа специалистов будет состоять из педиатров, кардиологов, неврологов и других медицинских работников, которые могут разработать комплексный план действий.
Поддерживающие меры, такие как переливание эритроцитов в случаях тяжелой анемии, также могут быть приняты для лечения TPI. В некоторых случаях удаление селезенки (спленэктомия) может улучшить анемию. Не существует лечения для предотвращения прогрессирующего неврологического нарушения или каких-либо других негематологических клинических проявлений заболевания.
Безусловно, наиболее распространенное использование изомераз в промышленности - это производство сахара. Глюкозоизомераза (также известная как ксилозоизомераза ) катализирует превращение D- ксилозы и D- глюкозы в D- ксилулозу и D- фруктозу. Как и большинство сахарных изомераз, глюкозоизомераза катализирует взаимное превращение альдоз и кетозов.
Превращение глюкозы во фруктозу является ключевым компонентом производства кукурузного сиропа с высоким содержанием фруктозы. Изомеризация более специфична, чем старые химические методы производства фруктозы, что приводит к более высокому выходу фруктозы и отсутствию побочных продуктов. Фруктоза, полученная в результате этой реакции изомеризации, более чистая, без остаточных привкусов от загрязняющих веществ. Кукурузный сироп с высоким содержанием фруктозы предпочитают многие производители кондитерских изделий и газированных напитков из-за высокой подслащивающей способности фруктозы (вдвое больше сахарозы), ее относительно низкой стоимости и неспособности кристаллизоваться. Фруктоза также используется в качестве подсластителя для диабетиков. Основные проблемы использования глюкозоизомеразы связаны с ее инактивацией при более высоких температурах и требованием высокого pH (от 7,0 до 9,0) в реакционной среде. Умеренно высокие температуры, выше 70 ° C, увеличивают выход фруктозы по крайней мере наполовину на стадии изомеризации. Для максимальной активности ферменту требуется двухвалентный катион, такой как Co 2+ и Mg 2+, что требует дополнительных затрат для производителей. Глюкозоизомераза также имеет гораздо более высокое сродство к ксилозе, чем к глюкозе, что требует тщательно контролируемой среды.
Изомеризация ксилозы в ксилулозу имеет свои коммерческие применения, поскольку интерес к биотопливу возрос. Эта реакция часто наблюдается в естественных условиях у бактерий, которые питаются разлагающимся растительным веществом. Наиболее распространенное промышленное использование в производстве этанола, достигнутом с помощью ферментации из ксилулозы. Использование гемицеллюлозы в качестве исходного материала очень распространено. Гемицеллюлоза содержит ксилан, который сам по себе состоит из ксилозы в amp; beta ; (1,4) связей. Использование глюкозоизомеразы очень эффективно превращает ксилозу в ксилулозу, на которую затем можно воздействовать путем ферментации дрожжей. В целом, обширные исследования в области генной инженерии были вложены в оптимизацию изомеразы глюкозы и облегчение ее извлечения из промышленных приложений для повторного использования.
Глюкозоизомераза способна катализировать изомеризацию ряда других сахаров, включая D- рибозу, D- аллозу и L- арабинозу. Наиболее эффективными субстратами являются субстраты, подобные глюкозе и ксилозе, имеющие экваториальные гидроксильные группы у третьего и четвертого атомов углерода. Текущая модель механизма изомеразы глюкозы - это модель гидридного сдвига, основанная на рентгеновской кристаллографии и исследованиях изотопного обмена.
Некоторые изомеразы связываются с биологическими мембранами как белки периферической мембраны или заякорены посредством единственной трансмембранной спирали, например изомеразы с тиоредоксиновым доменом и некоторые пролилизомеразы.