| Перегруппировка Клейзена | |
|---|---|
| Названа в честь | Райнера Людвига Клайзена |
| Тип реакции | Реакция перегруппировки |
| Идентификаторы | |
| Портал органической химии | перегруппировка Клайзена |
| RSC ID онтологии | RXNO: 0000148 |
Перегруппировка Клайзена является мощным углерод –углерод связь - химическая реакция, открытая Райнером Людвигом Клайзеном. Нагревание аллил винил эфира инициирует [3,3] -сигматропную перегруппировку с образованием γ, δ-ненасыщенной карбонил.

Обнаруженная в 1912 году перегруппировка Клейзена является первым зарегистрированным примером [3,3] -сигматропной перегруппировки. Написано много обзоров.
Перегруппировка Клейзена является экзотермической, согласованной ( разрыв связи и рекомбинация) перициклическая реакция. Правила Вудворда – Хоффмана показывают надфасциальный стереоспецифический путь реакции. Кинетика первого порядка, и все превращение происходит через высокоупорядоченное циклическое переходное состояние и является внутримолекулярным. Кроссинговые эксперименты исключают возможность перегруппировки, происходящей через межмолекулярный механизм реакции, и согласуются с внутримолекулярным процессом.
Существуют существенные эффекты растворителя наблюдается в перегруппировке Клайзена, где полярные растворители имеют тенденцию в большей степени ускорять реакцию. Растворители, связывающие водород, дали самые высокие константы скорости. Например, смеси растворителей этанол / вода дают константы скорости в 10 раз выше, чем сульфолан. Было показано, что трехвалентные алюмоорганические реагенты, такие как триметилалюминий, ускоряют эту реакцию.
Первая описанная перегруппировка Клайзена - это [3,3] -сигматропная перегруппировка аллил фенил эфира в промежуточное соединение 1, которое быстро таутомеризуется на орто-замещенный фенол.

Мета-замещение влияет на региоселективность этой перегруппировки. Например, электроноакцепторные группы (такие как бромид) в мета-положении направляют перегруппировку в орто-положение (71% орто-продукта), в то время как электронодонорные группы (такие как метокси) направляют перегруппировку в пара-положение (69 % пара продукта). Кроме того, присутствие орто-заместителей приводит исключительно к пара-замещенным продуктам перегруппировки (тандемная перегруппировка Клайзена и Коупа).
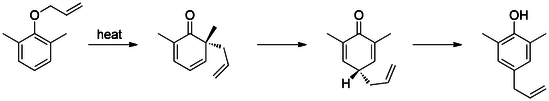
Если альдегид или карбоновая кислота занимает орто- или пара-положения, боковая аллильная цепь замещает группу, высвобождая ее в виде монооксида углерода или диоксида углерода соответственно.
The Bellus –Перегруппировка Клайзена представляет собой реакцию аллиловых простых эфиров, аминов и тиоэфиров с кетенами с образованием γ, δ-ненасыщенных сложных эфиров, амидов и тиоэфиров. Эта трансформация была случайно обнаружена Беллусом в 1979 году, когда они синтезировали ключевой промежуточный продукт инсектицида, пиретроид. Галогензамещенные кетены (R 1, R 2) часто используются в этой реакции из-за их высокой электрофильности. Разработаны многочисленные восстановительные методы для удаления образующихся α-галогенэфиров, амидов и тиоэфиров. Bellus-Claisen предлагает химикам-синтетикам уникальную возможность для стратегий расширения кольца.

Перегруппировка Эшенмозера-Клайзена протекает при нагревании аллиловых спиртов в присутствии N, N-диметилацетамида диметилацеталя с образованием γ, δ-ненасыщенного амида. Это было разработано Альбертом Эшенмозером в 1964 году. Перегруппировка Эшенмозера-Клайзена использовалась в качестве ключевого шага в полном синтезе морфина.
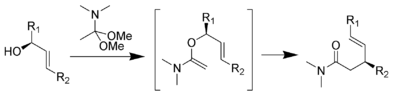
Механизм:

Перегруппировка Ирландии-Клейзена представляет собой реакцию аллильного карбоксилата с сильным основанием (таким как диизопропиламид лития ) с образованием γ, δ-ненасыщенного карбоновая кислота. Перегруппировка протекает через силилкетенацеталь, который образуется при захвате енолята лития хлортриметилсиланом. Подобно перегруппировке Беллуса-Клайзена (см. Выше), перегруппировка Ирландия-Клейзена может происходить при комнатной температуре и выше. Силилкетен-ацетали с E- и Z-конфигурацией приводят к анти- и син-перегруппированным продуктам соответственно. В литературе есть многочисленные примеры энантиоселективных перегруппировок Ирландии-Клейзена, которые включают хиральные борные реагенты и использование хиральных вспомогательных веществ.

Перегруппировка Джонсона-Клейзена является реакцией аллиловый спирт с сложным ортоэфиром с получением γ, δ-ненасыщенного сложного эфира. Слабые кислоты, такие как пропионовая кислота, использовались для катализатора этой реакции. Эта перестановка часто требует высоких температур (100–200 ° C) и может занять от 10 до 120 часов. Однако нагревание с помощью микроволн в присутствии KSF-глины или пропионовой кислоты продемонстрировало резкое увеличение скорости реакции и выхода.

Механизм:

Перегруппировка Клайзена ариловых эфиров может также может быть проведена в виде фотохимической реакции. В дополнение к традиционному орто-продукту, полученному в термических условиях (продукт перегруппировки [3,3]), фотохимическое изменение также дает пара-продукт (продукт [3,5]), альтернативные изомеры аллильной группы (например, [ 1,3] и [1,5] продукты) и простой потерей эфирной группы, и даже может перегруппировать алкиловые эфиры в дополнение к аллиловым эфирам. Фотохимическая реакция протекает в виде ступенчатого процесса радикального расщепления с последующим образованием связи, а не в виде согласованной перициклической реакции, что, таким образом, дает возможность для большего разнообразия возможных субстратов и изомеров продуктов. Результаты [1,3] и [1,5] фото-перегруппировки Клейзена аналогичны фото-перегруппировке Фриза ариловых эфиров и родственных ацильных соединений.
иминий может служить в качестве одного из пи-связанных фрагментов в перегруппировке.

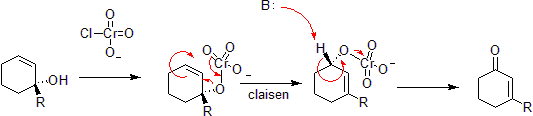
Хром может окисляют аллиловые спирты до α, β-ненасыщенных кетонов на противоположной стороне ненасыщенной связи от спирта. Это происходит через согласованную гетеро-реакцию Клайзена, хотя есть механистические различия, поскольку атом хрома имеет доступ к d-орбиталям, которые позволяют проводить реакцию в менее ограниченном наборе геометрий.
Реакция Чена-Маппа, также известная как [3,3] -фосфоримидатная перегруппировка или реакция Штаудингера-Клайзена, устанавливает фосфит вместо спирта и использует преимущество восстановления Штаудингера, чтобы преобразовать это в имин. Последующий процесс Клейзена обусловлен тем фактом, что двойная связь P = O более энергетически выгодна, чем двойная связь P = N.

Перегруппировка Овермана (названа в честь Ларри Оверман ) представляет собой перегруппировку Клейзена аллильных трихлорацетимидатов в аллильные трихлорацетамиды.

Перегруппировка Овермана применима к синтезу диаминосоединений вицинола из 1,2-вицинальных аллильных диолов.
В отличие от типичных перегруппировок Клейзена, требующих нагревания, цвиттерионная перегруппировка Клейзена имеют место при комнатной температуре или ниже. Ионы ацил аммония обладают высокой селективностью в отношении енолатов Z- в мягких условиях.

Фермент хоризматмутаза (EC 5.4.99.5) катализирует перегруппировку Клайзена хоризмата в префенат, ключевой промежуточный продукт в биосинтетическом пути синтеза фенилаланина и тирозин.
