 | |
 | |
| Имена | |
|---|---|
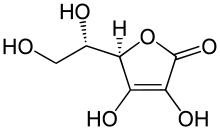
| Название ИЮПАК (5R) - [( 1S) -1,2-Дигидроксиэтил] -3,4-дигидроксифуран-2 (5H) -он | |
| Другие названия Витамин C | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| Номер EC |
|
| E номер | E300 (антиоксиданты,...) |
| IUPHAR / BPS | |
| KEGG | |
| PubChem CID | |
| UNII | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C6H8O6 |
| Молярная масса | 176,124 г · моль |
| Внешний вид | Белое или светло-желтое твердое вещество |
| Плотность | 1,65 г / см |
| Точка плавления | от 190 до 192 ° C (374 до 378 ° F; От 463 до 465 K) разлагается |
| Растворимость в воде | 330 г / л |
| Растворимость | Нерастворим в диэтиловом эфире, хлороформе, бензоле, петролейный эфир, масла, жиры |
| Растворимость в этаноле | 20 г / л |
| Растворимость в глицерине | 10 г / л |
| Растворимость в пропиленгликоле | 50 г / л |
| Кислотность (pK a) | 4,10 (первая), 11,6 (второй) |
| Фармакология | |
| Код АТС | A11GA01 (WHO ) G01AD03 (WHO ), S01XA15 (ВОЗ ) |
| Опасности | |
| Паспорт безопасности | JT Baker |
| NFPA 704 (огненный алмаз) |  1 1 0 1 1 0 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 11,9 г / кг (перорально, крыса) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Аскорбиновая кислота представляет собой органическое соединение с формулой C. 6H. 8O. 6, первоначально называлась гексуроновая кислота . Это белое твердое вещество, но загрязненные образцы могут иметь желтоватый оттенок. Хорошо растворяется в воде с образованием слабокислых растворов. Это мягкий восстанавливающий агент.
Аскорбиновая кислота существует в виде двух энантиомеров (зеркальное отображение изомеров ), обычно обозначаемых «l» (от «levo») и «d» (для «правого движения»). Изомер l является наиболее часто встречающимся: он встречается в природе во многих пищевых продуктах и является одной из форм («витамер ») витамина C, важного питательного вещества для человека. и многие животные. Дефицит витамина С вызывает цингу, которая раньше была основным заболеванием моряков в длительных морских путешествиях. Он используется как пищевая добавка и пищевая добавка из-за своих антиоксидантных свойств. Форма «d» может быть получена посредством химического синтеза, но не имеет значительной биологической роли.
антискорбутационные свойства некоторых пищевых продуктов были продемонстрированы в 18 веке Джеймсом Линдом. В 1907 году Аксель Холст и Теодор Фрёлих обнаружили, что антискорбутический фактор представляет собой водорастворимое химическое вещество, отличное от того, которое предотвращает авитаминоз. Между 1928 и 1932 годами Альберт Сент-Дьёрдьи выделил кандидата на это вещество, которое он назвал «гексуроновой кислотой», сначала из растений, а затем из надпочечников животных. В 1932 году Чарльз Глен Кинг подтвердил, что это действительно антискорбутический фактор.
В 1933 году сахарный химик Уолтер Норман Хаворт работал с образцами «гексуроновой кислоты», которую Сент-Дьерди выделил из паприки и отправил ему в предыдущем году, вывел правильную структуру и оптико-изомерную природу соединения, а в 1934 году сообщил о его первом синтезе. Что касается антискорбиновых свойств соединения, Хаворт и Сент-Дьёрдьи предложили переименовать его в «а-скорбиновую кислоту» для соединения, а позже конкретно в 1-аскорбиновую кислоту. За их работу в 1937 г. Нобелевские премии по химии и медицине были присуждены Хаворту и Сент-Дьерди соответственно.
Аскорбиновая кислота является виниловой кислотой и образует аскорбат анион при депротонировании на одном из гидроксилы. Это свойство характерно для редуктонов : ендиолов с карбонильной группой, смежной с ендиольной группой, а именно с группой –C (OH) = C (OH). –C (= O) -. Аскорбат-анион стабилизируется делокализацией электронов, которая возникает в результате резонанса между двумя формами:

По этой причине аскорбиновая кислота намного более кислая, чем можно было бы ожидать, если бы соединение содержало только изолированные гидроксильные группы.
Аскорбатный анион образует соли, такие как аскорбат натрия, аскорбат кальция и калий. аскорбат.
Аскорбиновая кислота также может реагировать с органическими кислотами в виде спирта с образованием сложных эфиров, таких как аскорбилпальмитат и аскорбилстеарат.
Нуклеофильная атака аскорбиновой кислоты на протон приводит к 1,3-дикетону:
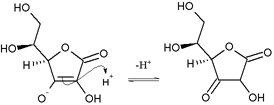
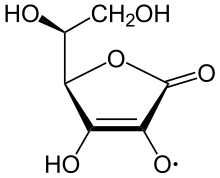 Полугидроаскорбатный остаток кислоты
Полугидроаскорбатный остаток кислоты 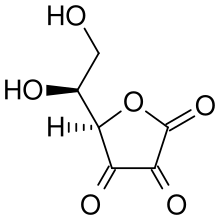 Дегидроаскорбиновая кислота
Дегидроаскорбиновая кислота Аскорбат ion является преобладающим видом при типичных биологических значениях pH. Это мягкий восстанавливающий агент и антиоксидант. Он окисляется с потерей одного электрона с образованием радикального катиона, а затем с потерей второго электрона с образованием дегидроаскорбиновой кислоты. Обычно он реагирует с окислителями активных форм кислорода, такими как гидроксильный радикал.
. Аскорбиновая кислота является особенной, потому что она может переносить один электрон благодаря своей собственной резонансно-стабилизированной природе. ион-радикал, называемый семидегидроаскорбат. Итоговая реакция:
Под воздействием кислорода аскорбиновая кислота подвергнется дальнейшему окислительному разложению с образованием различных продуктов, включая, ксилоновая кислота, треоновая кислота и щавелевая кислота.
Реактивные формы кислорода наносят вред животным и растениям на молекулярном уровне из-за их возможного взаимодействия с нуклеиновой кислотой. кислоты, белки и липиды. Иногда эти радикалы инициируют цепные реакции. Аскорбат может прекратить эти цепные радикальные реакции посредством переноса электрона. Окисленные формы аскорбата относительно инертны и не вызывают повреждения клеток.
Однако, будучи хорошим донором электронов, избыток аскорбата в присутствии свободных ионов металла может не только способствовать, но и инициировать реакции свободных радикалов, что делает его потенциально опасным прооксидантным соединением в определенных метаболических условиях.
Аскорбиновая кислота и ее соли натрия, калия и кальция обычно используются в качестве антиоксидантов пищевых добавок. Эти соединения водорастворимы и, таким образом, не могут защитить жиры от окисления: для этой цели жиро- растворимые сложные эфиры аскорбиновой кислоты с длинной цепью жирные кислоты (аскорбилпальмитат или аскорбилстеарат) могут использоваться в качестве пищевых антиоксидантов.
Создает летучие соединения при смешивании с глюкозой и аминокислотами при 90 ° C.
Это кофактор в окислении тирозина .
1-аскорбиновая кислота и ее соли используются в основном в качестве пищевых добавок, в основном для борьбы с окислением. Он одобрен для этой цели в ЕС под номером E E300, США, Австралия и Новая Зеландия)
Еще одно важное применение l -аскорбиновая кислота - это пищевая добавка.
Естественный биосинтез витамина C происходит во многих растениях и животных с помощью различных процессов.
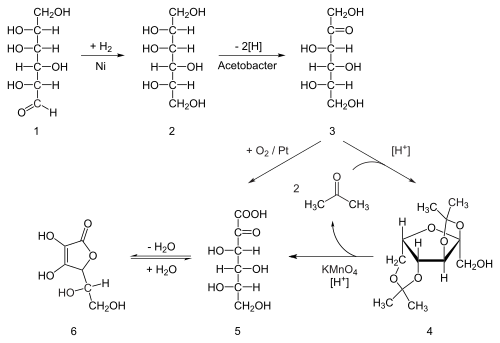 Устаревший, но исторически важный промышленный синтез аскорбиновой кислоты из глюкозы с помощью процесса Рейхштейна.
Устаревший, но исторически важный промышленный синтез аскорбиновой кислоты из глюкозы с помощью процесса Рейхштейна.Восемьдесят процентов мировых запасов аскорбиновой кислоты производится в Китае. В промышленности аскорбиновую кислоту получают из глюкозы способом, основанным на историческом процессе Райхштейна. В первом из пяти этапов глюкоза каталитически гидрируется до сорбита, который затем окисляется микроорганизмом <116.>От Acetobacter субоксидантов до сорбозы. Только одна из шести гидроксильных групп окисляется этой ферментативной реакцией. С этого момента доступны два маршрута. Обработка продукта ацетоном в присутствии кислотного катализатора превращает четыре из оставшихся гидроксильных групп в ацетали. Незащищенная гидроксильная группа окисляется до карбоновой кислоты в результате реакции с каталитическим окислителем TEMPO (регенерируется раствором гипохлорита натрия - отбеливающим раствором). Исторически сложилось так, что при промышленном производстве с помощью процесса Райхштейна в качестве отбеливающего раствора использовался перманганат калия. Катализируемый кислотой гидролиз этого продукта выполняет двойную функцию: удаление двух ацетальных групп и закрывающую цикл лактонизацию. На этом этапе образуется аскорбиновая кислота. Каждая из пяти стадий имеет выход более 90%.
Более биотехнологический процесс, впервые разработанный в Китае в 1960-х годах, но получивший дальнейшее развитие в 1990-х годах, позволяет обойтись без использования ацетон-защитных групп. Второй вид генетически модифицированных микробов, такой как мутант Erwinia, среди прочего, окисляет сорбозу до (2-KGA), который затем может подвергаться лактонизации с замыканием кольца посредством дегидратации. Этот метод используется в основном процессе производства аскорбиновой кислоты в Китае, который обеспечивает 80% мирового производства аскорбиновой кислоты. Американские и китайские исследователи соревнуются в создании мутанта, который может осуществлять ферментацию в одном горшке непосредственно из глюкозы в 2-KGA, минуя как необходимость второй ферментации, так и необходимость восстановления глюкозы до сорбита.
Существует d-аскорбиновая кислота, которая не встречается в природе, но может быть синтезирована искусственно. В частности, известно, что l-аскорбат участвует во многих специфических ферментативных реакциях, для которых требуется правильный энантиомер (l-аскорбат, а не d-аскорбат). l-аскорбиновая кислота имеет удельное вращение из [α]. D= + 23 °.
Традиционным способом анализа содержания аскорбиновой кислоты является процесс титрования с окислителем, и было разработано несколько процедур.
В популярном методе йодометрии используется йод в присутствии индикатора крахмала. Йод восстанавливается аскорбиновой кислотой, и, когда вся аскорбиновая кислота прореагировала, йод оказывается в избытке, образуя сине-черный комплекс с индикатором крахмала. Это указывает на конечную точку титрования.
В качестве альтернативы аскорбиновую кислоту можно обработать избытком йода с последующим обратным титрованием тиосульфатом натрия с использованием крахмала в качестве индикатора.
Этот йодометрический метод был пересмотрен, чтобы использовать реакцию аскорбиновой кислоты. кислоты с йодатом и йодидом в растворе кислоты. При электролизе раствора йодида калия образуется йод, который вступает в реакцию с аскорбиновой кислотой. Окончание процесса определяется потенциометрическим титрованием аналогично титрованию по Карлу Фишеру. Количество аскорбиновой кислоты можно рассчитать по закону Фарадея.
В другом альтернативном варианте используется N-бромсукцинимид (NBS) в качестве окислителя в присутствии йодида калия и крахмал. NBS сначала окисляет аскорбиновую кислоту; когда последний истощается, NBS высвобождает йод из йодида калия, который затем образует сине-черный комплекс с крахмалом.
| На Wikimedia Commons есть материалы, связанные с Химией аскорбиновой кислоты. |