| 5-HT 3 антагонист рецептора | |
|---|---|
| Класс препарата | |
 Формула скелета из ондансетрона, прототипа 5-HT 3 антагониста Формула скелета из ондансетрона, прототипа 5-HT 3 антагониста | |
| Идентификаторы класса | |
| Используйте | Тошнота и Рвота |
| Код ATC | A04AA |
| Биологическая мишень | 5-HT 3 рецептор |
| Клинические данные | |
| Drugs.com | Классы лекарств |
| Потребительские сообщения | Best Buy Drugs |
| Внешние ссылки | |
| MeSH | D058831 |
| В Викиданных | |
Антагонисты 5-HT 3, неофициально известные как «сетроны ", представляют собой класс лекарственных средств, которые действуют как антагонисты рецептора на 5-HT 3 рецептор, подтип рецептора серотонина , обнаруженный в терминалах блуждающего нерва и в некоторых областях мозга. За заметными исключениями алосетрон и циланзетрон, которые используются при лечении синдрома раздраженного кишечника, все антагонисты 5-HT 3 противорвотные, используемые для профилактики и лечения тошноты и рвоты. Они особенно эффективны при контроле тошноты и рвоты, вызываемых химиотерапией рака, и считаются золотым стандартом для этой цели.
Антагонисты 5-HT 3 могут быть обозначены суффиксом -setron и классифицируются под кодом A04AA в системе WHO анатомо-терапевтической химической классификации..
5-HT 3 антагонисты наиболее эффективны в профилактике и лечении тошноты и рвоты, вызванных химиотерапией (CINV), особенно вызванных высокой рвотные препараты, такие как цисплатин ; когда они используются для этой цели, их можно вводить отдельно или, чаще, с глюкокортикоидом, обычно дексаметазоном. Их обычно вводят внутривенно незадолго до введения химиотерапевтического агента, хотя некоторые авторы утверждали, что пероральное введение может быть предпочтительным. Одновременное введение антагониста рецептора NK1, такого как апрепитант, , значительно увеличивает эффективность антагонистов 5-HT 3 в предотвращении как острых и отложенный CINV.
Антагонисты 5-HT 3 также показаны для профилактики и лечения радиационно-индуцированной тошноты и рвоты (RINV), когда это необходимо, и послеоперационная тошнота и рвота (ПОТР). Хотя они более эффективны при контроле CINV (при котором они полностью устраняют симптомы у 70% людей и уменьшают их у оставшихся 30%), они столь же эффективны, как и другие агенты для PONV.
Текущие данные свидетельствуют о том, что антагонисты 5-HT 3 неэффективны в борьбе с укачиванием. рандомизированное плацебо-контролируемое исследование ондансетрона для лечения укачивания у персонала санитарной авиации показало субъективное улучшение, но оно не было статистически значимым.
Алосетрон и силанзетрон - последний был разработан Solvay но никогда не одобряются FDA - не являются противорвотными; вместо этого они показаны при лечении подмножества синдрома раздраженного кишечника, где диарея является доминирующим симптомом. Алосетрон был изъят с рынка США в 2000 году из-за неприемлемо частых серьезных побочных эффектов, включая ишемический колит, и доступен только в рамках ограничительной программы для пациентов, отвечающих определенным требованиям.
Определенные прокинетические препараты, такие как цизаприд, рензаприд и метоклопрамид, хотя и не являются собственно антагонистами 5-HT 3, обладают некоторыми слабый антагонистический эффект в отношении рецептора 5-HT 3. Галанолактон, дитерпеноид, обнаруженный в имбире, является антагонистом 5-HT 3 и, как полагают, по крайней мере частично опосредует анти- рвотная активность этого растения. Миртазапин представляет собой тетрациклический антидепрессант с эффектами антагониста 5-HT 2 и только очень умеренными эффектами антагониста 5-HT 3, который также обладает сильными противорвотные свойства, однако он также обладает сильным седативным действием. Исследования показывают, что миртазапин столь же эффективен при лечении тошноты и рвоты, связанных с химиотерапией, как и стандартные методы лечения; он также дешевле и имеет меньше побочных эффектов, чем обычные противорвотные средства, а его антидепрессивные свойства могут быть дополнительным преимуществом для больных раком. Миртазапин также использовался для лечения нарушения моторики гастропареза из-за его противорвотного действия. оланзапин, атипичный антипсихотик с аналогичными противорвотными свойствами по сравнению с миртазапином, также перспективен при лечении тошноты и рвоты, вызванных химиотерапией.
Есть несколько побочных эффектов, связанных с использованием 5-HT 3 антагонисты; наиболее частыми являются запор или диарея, головная боль и головокружение. В отличие от антигистаминных препаратов с противорвотными свойствами, таких как циклизин, антагонисты 5-HT 3 не вызывают седативного эффекта и не вызывают экстрапирамидные эффекты, как, например, фенотиазины (например, прохлорперазин ).
Все антагонисты 5-HT 3 были связаны с бессимптомными изменениями электрокардиограммы, такими как удлинение интервалов PT и QTc и некоторые аритмии. Клиническое значение этих побочных эффектов неизвестно.
Рецепторы 5-HT 3 присутствуют в нескольких критических участках, вовлеченных в рвоту, включая вагус афференты, ядро солитарного тракта (STN) и сама область postrema. Серотонин высвобождается энтерохромаффинными клетками тонкой кишки в ответ на химиотерапевтические агенты и может стимулировать вагус афференты (через рецепторы 5-HT 3), чтобы инициировать рвотный рефлекс. Антагонисты рецептора 5-HT 3 подавляют рвоту и тошноту путем ингибирования связывания серотонина с рецепторами 5-HT 3. Самая высокая концентрация 5-HT 3 рецепторов в центральной нервной системе (CNS ) обнаружена в STN и Триггерная зона хеморецепторов (CTZ) и антагонисты 5-HT 3 могут также подавлять рвоту и тошноту, воздействуя на эти участки. Антагонисты 5-HT 3 очень селективны и обладают небольшим сродством к другим рецепторам, таким как дофамин, гистамин и мускариновые рецепторы ацетилхолина.
Все антагонисты 5-HT 3 хорошо абсорбируются и эффективны после перорального приема, и все метаболизируются в печени различными изоферментами системы цитохрома P450. Однако они не ингибируют или индуцируют эти ферменты.
Несмотря на то, что 5-HT 3 антагонисты рецептора имеют общий механизм действия, они имеют разные химические структуры и проявляют различия в сродстве к рецептору, ответной реакции на дозу и продолжительности действия. Они также метаболизируются по-разному, то есть разные компоненты системы цитохрома P450 (CYP ) преобладают в метаболизме антагонисты.
Из-за этого пациенты, устойчивые к одному антагонисту, могут получить пользу от другого. Существует корреляция между количеством активных аллелей CYP 2D6 и количеством эпизодов рвоты у пациентов, получающих лечение цисплатином и ондансетроном или трописетроном. Пациенты с множественными аллелями, как правило, невосприимчивы к противорвотному препарату и наоборот.
| Лекарство | Химическое. природа | антагонисты рецепторов | T1/2 (h) | Метаболизм | Доза |
|---|---|---|---|---|---|
| Ондансетрон | Карбазол производное | 5- Антагонист рецептора HT 3 и слабый антагонист 5-HT 4 | 3,9 часа | CYP1A1 /2, CYP2D6, CYP 3A3 / 4 /5 | 0,15 мг / кг |
| гранисетрон | индазол | 5-HT 3 антагонист рецепторов | 9-11,6 часов | CYP3A3 / 4 /5 | 10 мкг / кг |
| Доласетрон | Индол | 5-HT 3 антагонист рецепторов | 7–9 часов | CYP 3A3 / 4 /5, CYP2D6 | 0,6 –3 мг / кг |
| палоносетрон | изохинолин | 5-HT 3 антагонист рецепторов; самое высокое сродство к рецептору 5-HT 3 в этом классе | 40 часов | CYP1A2, CYP2D6, CYP3A3 / 4 /5 | 0,25 мг x 1 доза |
| Рамозетрон | Производное бензимидазола | 5-HT 3 антагонист рецептора | 5,8 часа | 300 мкг / кг | |
| Трописетрон | Индол | 5-HT 3 антагонист рецептора | 5,6 часа | CYP 3A3 / 4 /5, CYP2D6 | 200 мкг / кг |
| Вортиоксетин (Тринтелликс) | Индол | 5-HT 3 антагонист рецепторов Антидепрессант | 66h | CYP 2D6 / / CYP2B6 /, CYP2C19 | 5 мг, 10 мг, 20 мг дозы |
История антагонистов рецепторов 5-HT 3 началась в 1957 году, когда Джон Гэддум и Зулейка П. Пикарелли из Эдинбургского университета предположили существование двух подтипов серотониновых рецепторов, рецепторов M и D (названных таким образом, потому что их функция может быть заблокирована морфином и дибензилин соответственно). Позже было обнаружено, что рецептор 5-HT 3 соответствует рецептору М. В 1970-х годах Джон Фозард обнаружил, что метоклопрамид и кокаин являются слабыми антагонистами рецептора 5-HT 3 (5-HT-M). Позднее Фозард и Морис Гиттос синтезировали MDL 72222, первый мощный и действительно селективный антагонист рецептора 5-HT 3. Было обнаружено, что противорвотные эффекты метоклопрамида частично связаны с его антагонизмом к серотонину.
Пока Фозард исследовал аналоги кокаина, исследователи из Sandoz идентифицировали мощный избирательный 5-HT 3 антагонист рецептора ICS 205-930, из которого были разработаны и одобрены в 1991 г. первые поступившие на рынок селективные антагонисты рецептора 5-HT 3 ондансетрон и гранисетрон. 1993 г. соответственно. Было синтезировано несколько соединений, связанных с MDL 72222, что в конечном итоге привело к одобрению трописетрона в 1994 году и доласетрона в 1997 году. Новый и улучшенный антагонист рецептора 5-HT 3, названный палоносетроном, был одобрен в 2003 году. селективные антагонисты рецептора 5-HT 3 значительно улучшили лечение тошноты и рвоты. Ондансетрон, гранисетрон, доласетрон и палоносетрон в настоящее время одобрены в США и составляют основу терапии для контроля острой рвоты химиотерапевтическими агентами с рвотным потенциалом от умеренного до высокого.
Антагонисты рецептора 5-HT 3 или антагонисты серотонина были впервые представлены в начале 1990-х годов, и они стали наиболее широко используемыми противорвотными препаратами в химиотерапии. Они также оказались безопасными и эффективными для лечения послеоперационной тошноты и рвоты. Серотонин (5-HT) широко распространен в кишечнике и центральной нервной системе. В кишечнике 5-HT обнаруживается в основном в слизистых энтерохромаффинных клетках. Энтерохромаффинные клетки представляют собой сенсорные преобразователи, которые высвобождают 5-HT для активации внутренних (через 5-HT1P и 5-HT 4 рецепторов) и внешних (через 5-HT 3 рецепторы) первичные афферентные нервы. Было обнаружено, что химиотерапевтические препараты для лечения злокачественных заболеваний, вызывающих рвоту, вызывают высвобождение большого количества серотонина из энтерохромаффинных клеток кишечника, серотонин действует на рецепторы 5-HT 3 в кишечнике и стволе мозга.
Эксперименты показали, что сайт связывания лиганда расположен на границе раздела двух соседних субъединиц. Сайт связывания лиганда образован тремя петлями (A-C) от основной субъединицы связывания лиганда (основная поверхность) и тремя β-цепями (D-F) от соседней субъединицы (комплементарная поверхность). Аминокислотный остаток E129 на петле A обращен в связывающий карман и образует критическую водородную связь с гидроксильной группой 5-HT. Петля B содержит W183, критический остаток связывания лиганда триптофана, который вносит вклад в катион-π-взаимодействие между pi электронной плотностью триптофана и первичным амином 5-HT. Остатки петли C рассматривались как кандидаты на различие фармакологии рецепторов грызунов и человека 5-HT 3 из-за их расхождения между виды. Наиболее важным ароматическим остатком внутри петли C, вероятно, является Y234, который расположен напротив петли B триптофана в кармане связывания лиганда и участвует в связывании лиганда. Петли D и F на самом деле являются β-нитями, а не петлями. W90 в петле D имеет решающее значение для связывания лиганда, и антагонисты могут напрямую связываться с R92. Азабициклическое кольцо конкурентного антагониста гранисетрона расположено близко к W183, образуя взаимодействие катион-pi. Остатки петли E Y143, G148, E149, V150, Q151, N152, Y153 и K154 могут быть важны для связывания гранисетрона. Структура петли F еще не выяснена, но W195 и D204, по-видимому, имеют решающее значение для связывания лиганда.
| 5-HT 3 антагонисты рецепторов | Аффинность связывания (K d, K i, K 50) | Species |
|---|---|---|
| Tropisetron | 11 нМ | Человек |
| Гранисетрон | 1,44 нМ | Человек |
| Ондансетрон | 4,9 нМ | Человек |
| Палоносетрон | 31,6 нМ | Кора головного мозга крысы, подвздошно-миентеральное сплетение кролика, подвздошное сплетение морской свинки |
| Доласетрон | 20,03 нМ | НГ 108-15 |
| Метоклопрамид (неселективный) | 355 нМ | Человек |
| Кокаин | 2,45-83 нМ | Крыса-кролик |
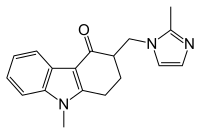 Рис. 1. Ондансетрон: антагонист рецептора 5-HT 3 первого поколения
Рис. 1. Ондансетрон: антагонист рецептора 5-HT 3 первого поколения  Рис 2. Палоносетрон: антагонист рецептора 5-HT 3 второго поколения
Рис 2. Палоносетрон: антагонист рецептора 5-HT 3 второго поколения Химические структуры Антагонист рецептора 5-HT 3 первого поколения может быть отнесен к трем категориям. в классах
первого поколения Антагонисты рецепторов 5-HT 3 (ондансетрон, доласетрон, гранисетрон и трописетрон ) были наиболее важными препаратами в противорвотной терапии для рвотной химиотерапии. Они особенно эффективны при лечении острой рвоты, возникающей в первые 24 часа после химиотерапии. Новый препарат палоносетрон является фармакологически отличным и высокоселективным антагонистом рецептора 5-HT 3 второго поколения. Палоносетрон имеет два стереогенных центра и существует в виде четырех стереоизомеров. Палоносетрон имеет более длительный период полужизни (40 часов) и большую аффинность связывания с рецептором (>30 раз по сравнению с антагонистами первого поколения).
 Рис. 3. 5-HT 3 фармакофор антагонистов рецептора (схема)
Рис. 3. 5-HT 3 фармакофор антагонистов рецептора (схема) фармакофор рецепторов 5-HT 3 состоит из трех компонентов: карбонилсодержащий связывающий фрагмент, ароматический / гетероароматическое кольцо и основной центр. Карбонильная группа компланарна ароматическому кольцу. Антагонисты рецептора 5-HT 3 с большей вероятностью связываются в своей протонированной форме. Пристыковка ряда антагонистов к модели гомологии сайта связывания 5-HT 3 рецептора показывает достаточно хорошее согласие с моделью фармакофора и подтверждает наблюдаемые различия между видами. Исследования гранисетрона в связывающем кармане показали, что ароматические кольца гранисетрона расположены между W183 и Y234, а азабициклическое кольцо - между W90 и F226. В этом исследовании было идентифицировано другое энергетически выгодное расположение гранисетрона, ближе к мембране, в положении, которое могло быть частью пути связывания / разрыва лиганда. Аналогично расположенный альтернативный сайт связывания для гранисетрона был впоследствии идентифицирован в другом исследовании рецептора 5-HT 3.
 Рис. 4. Основные фармакофорные элементы известные антагонисты 5-HT 3
Рис. 4. Основные фармакофорные элементы известные антагонисты 5-HT 3 5-HT 3 рецепторы имеют общий фармакофор. Ароматический фрагмент (предпочтительно индол), связывающая ацильная группа, способная к взаимодействиям водородной связи, и основной амин (азот ) могут рассматриваться как ключевые фармакофорных элементов известных антагонистов рецепторов 5-HT 3. Существуют стерические ограничения для сайта связывания ароматического, и хотя возможны два взаимодействия водородных связей на гетероциклической связывающей группе (оксадиазол, способный принимать две водородные связи), только одно является существенным для высокая близость. Оптимальная среда для основного азота - это когда он ограничен азабициклиновой системой с наивысшим сродством, наблюдаемым для систем с азотом в положении моста, а вторичные амины являются более сильными. Рецептор 5-HT3 может вмещать только небольшие заместители заряженного амина, оптимальная группа метил. Оптимальное расстояние между центром связывания ароматических соединений и основным амином составляет 8,4-8,9 Å, и лучше всего, если двухуглеродная связь разделяет оксадиазол и азот. Увеличивающееся замещение R увеличивает сродство. Наиболее сильные антагонисты 5-HT 3 рецепторов имеют 6-членное ароматическое кольцо и обычно имеют 6,5 гетероциклические кольца. Не было обнаружено корреляции между липофильностью соединений и сродством к рецептору 5-HT 3. Поскольку большинство известных антагонистов 5-HT3 представляют собой сложноэфирные или амидные производные, они потенциально подвержены гидролизу, чего можно избежать, включив акцепторы Н-связи в 5-членное гетероароматическое кольцо.
 Рис. 5. Важность C5 ( Замещение R1) и C7 (R2) изучено
Рис. 5. Важность C5 ( Замещение R1) и C7 (R2) изучено Взаимосвязь структура-активность (SAR) лигандов рецептора LGIC ценна для изучения их структуры и функции. антагонистическая -подобная молекула с низкой внутренней активностью (ia) снижает частоту открытия каналов и проницаемость для ионов. Небольшие липофильные заместители C5 (R1) (см. Фиг. 5) дают соединения с сильным антагонизмом, что указывает на то, что заместитель C5 может уместиться в узкой гидрофобной бороздке связывающей области в рецепторе. Кажется, что аминокислотные остатки, которые взаимодействуют с заместителями C7 (R2), имеют мало общего со связыванием лиганда, но играют большую роль в стробировании ионных каналов. Стерически объемные заместители демонстрируют большее взаимодействие с закрывающими аминокислотными остатками и способствуют открытой конформации ионного канала из-за стерического отталкивания.
 Рис. 6. Карбонильная группа полностью копланарна с соседним ароматическим кольцом.
Рис. 6. Карбонильная группа полностью копланарна с соседним ароматическим кольцом. Ондансетрон является рацематом, но стереохимия асимметричного углерода атома не является важным фактором в 5-HT 3 рецепторное взаимодействие. Аннелирование 1,7-положения индольного ядра ондансетрона приводит к увеличению сродства к рецептору.
. Метильная группа, по-видимому, функционально так же эффективна, как и хлор в положении R (см. Рис. 6).. Группа карбонила отвечает за сильное взаимодействие с рецептором и вносит значительный вклад в процесс связывания. Эта карбонильная группа полностью копланарна со смежным ароматическим кольцом, что указывает на то, что связанная с рецептором конформация соответствует одной из наиболее стабильных конформаций этой группы в гибких соединениях.
Небольшое открытое исследование, проведенное в 2000 году, показало, что ондансетрон полезен при лечении антипсихотических -индуцированных поздней дискинезии у людей с шизофренией. Пациенты исследования также показали значительное улучшение симптомов заболевания; более позднее двойное слепое, рандомизированное контролируемое исследование также обнаружило, что ондансетрон значительно улучшает симптомы шизофрении при использовании в качестве дополнения к галоперидолу, и люди, принимавшие оба препарата, испытывали меньше о побочных эффектах, обычно связанных с галоперидолом.