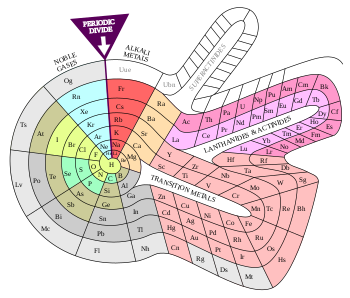
 Периодическая таблица Теодора Бенфея (1964)
Периодическая таблица Теодора Бенфея (1964) Альтернатива периодические таблицы представляют собой таблицы химических элементов, отличающиеся по своей организации от традиционного описания периодической системы.
Более тысячи было разработано, часто для дидактических целей Причина в том, что не все корреляции между химическими элементами эффективно фиксируются стандартной периодической таблицей.
Периодическая таблица с левым шагом Чарльза Джанет - наиболее широко используемая альтернатива традиционному изображению периодической системы. Он организует элементы в соответствии с идеализированным орбитальным заполнением (вместо валентности ). Например, элементы от Sc до Zn показаны в виде блока 3d, подразумевающего орбитальную занятость [Ar] 4s 3d, хотя теперь известно, что Cr на самом деле имеет орбитальную занятость [Ar] 4s 3d, а Cu имеет [Ar] 4s 3d.
| f | f | f | f | f | f | f | f | f | f | f | f | f | f | d | d | d | d | d | d | d | d | d | d | p | p | p | p | p | p | s | s | |
| 1s | H | He | ||||||||||||||||||||||||||||||
| 2s | Li | Be | ||||||||||||||||||||||||||||||
| 2p 3s | B | C | N | O | F | Ne | Na | Mg | ||||||||||||||||||||||||
| 3p 4s | Al | Si | P | S | Cl | Ar | K | Ca | ||||||||||||||||||||||||
| 3d 4p 5s | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | Rb | Sr | ||||||||||||||
| 4d 5p 6s | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | Cs | Ba | ||||||||||||||
| 4f 5d 6p 7s | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | Fr | Ra |
| 5f 6d 7p 8s | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | 119 | 120 |
| f-block | d-block | p-block | s-block | |||||||||||||||||||||||||||||
 Слева направо: s-, f-, d-, p-блок в общем представлении периодической таблицы; для достаточно высоких главных квантовых чисел эти блоки заполняются в порядке s, p, d и f. Периодическая таблица с левым шагом организована в соответствии с изменением этого порядка, так что истинный порядок поддерживается посредством правильного чтения.
Слева направо: s-, f-, d-, p-блок в общем представлении периодической таблицы; для достаточно высоких главных квантовых чисел эти блоки заполняются в порядке s, p, d и f. Периодическая таблица с левым шагом организована в соответствии с изменением этого порядка, так что истинный порядок поддерживается посредством правильного чтения. По сравнению с обычным расположением, таблица с левым шагом имеет следующие изменения:
В результате порядок по-прежнему соответствует атомному номеру (Z), 1–120.
В периодической таблице Теодора Бенфея элементы образуют двумерную спираль, начиная с водорода, и складывают свои вокруг двух полуостровов: переходные металлы и лантаноиды и актиниды. Остров суперактинида уже вставлен в него.
3-D периодическая таблица Поля Жигера состоит из четыре соединенных билборда с элементами, написанными на лицевой и оборотной сторонах. Первый рекламный щит имеет элементы группы 1 спереди и элементы группы 2 сзади, причем водород и гелий полностью исключены. Под углом 90 ° второй рекламный щит содержит группы с 13 по 18 спереди и сзади. Еще два рекламных щита, каждый с углами 90 °, содержат другие элементы.
Периодическая таблица физика Тимоти Стоу трехмерна с тремя осями, представляющими главное квантовое число, орбитальное квантовое число и орбитальное магнитное квантовое число. Гелий снова является элементом группы 2.
Рональд Л. Рич предложил периодическую таблицу, в которой элементы появляются более одного раза, когда это необходимо. Он отмечает, что водород разделяет свойства с элементами группы 1 на основе валентности, с элементами группы 17, потому что водород является неметаллом, но также и с группа углерода на основе сходства химической связи с переходными металлами и аналогичной электроотрицательности. В этом исполнении периодической таблицы углерод и кремний также входят в ту же группу, что и титан и цирконий.
 Периодическая таблица ADOMAH отражает электронные конфигурации атомов.
Периодическая таблица ADOMAH отражает электронные конфигурации атомов. Таблица ADOMAH является адаптацией левой ступенчатой таблицы. Каждый строго вертикальный столбец таблицы имеет одинаковое значение главного квантового числа n. Например, для Fe n = 3. Каждый блок элементов имеет одинаковое значение вторичного квантового числа l. Например, для Fe l = 2. Каждая запись элемента вместе со всеми предыдущими элементами соответствует электронной конфигурации этого элемента (за 20 исключениями из 118 известных элементов). Например, электронная конфигурация Fe определяется, начиная с H, равной 1 с, и считая в порядке атомных номеров. Это дает конфигурацию 1s 2s 2p 3s 3p 4s 3d или, вкратце, [Ar] 4s 3d.
Четыре блока таблицы Адома могут быть перегруппированы таким образом, чтобы они помещались на равном расстоянии внутри правильного тетраэдра. Последний, в свою очередь, умещается в куб.
Таблица химиков («Newlands Revisited») с альтернативным расположением водорода, гелия и лантаноидов была опубликована EG Marks и JA Marks в 2010 году.
Из исходной периодической таблицы Менделеева элементы были в основном расположены по валентности (группы в столбцы) и повторению в ней (точки в строках). С годами и с открытиями в атомной структуре эта схема была скорректирована и расширена, но не изменилась в принципе.
 Периодическая таблица Менделеева 1871 г. в VIII столбцах. В настоящее время, грубо говоря, пары Reihen отображаются как группы A, B (например : Reihen 4, 5 записываются как период 3, а группы (столбцы) IA – VIIIA, IB –VIIIB).
Периодическая таблица Менделеева 1871 г. в VIII столбцах. В настоящее время, грубо говоря, пары Reihen отображаются как группы A, B (например : Reihen 4, 5 записываются как период 3, а группы (столбцы) IA – VIIIA, IB –VIIIB). Самая старая таблица Менделеева - это сокращенная таблица (столбцы I – VIII) Дмитрия Менделеева, которая показывает вторичные химические родства. Например, щелочные металлы и металлы для чеканки (медь, серебро, золото) находятся в одном столбце, поскольку обе группы имеют валентность, равную единице. Этот формат до сих пор используется многими, как показано в этой современной русской сокращенной таблице, которая включает все элементы и имена элементов до roentgenium.
H. Г. Деминг использовал так называемую длинную периодическую таблицу (18 столбцов) в своем учебнике «Общая химия», который впервые появился в США в 1923 г. (Wiley), и первым обозначил первые две и последние пять основных групп обозначены буквой «А», а промежуточные переходные группы обозначены буквой «В».
Нумерация была выбрана таким образом, чтобы характеристические оксиды групп В соответствовали оксидам групп А. Группы железа, кобальта и никеля не были обозначены ни A, ни B. Группа благородных газов первоначально была прикреплена (Демингом) к левой стороне периодической таблицы. Позже группа была переведена на правую сторону и обычно обозначена как группа VIIIA.
В расширенной таблице Менделеева, предложенной Гленном Т. Сиборгом в 1969 г., пока неизвестные элементы включены до атомного номера 168. Теоретические периоды сверх обычного периода 7 добавляются.
В области исследований суператомов кластеры атомов обладают свойствами отдельных атомов другого элемента. Предлагается расширить периодическую таблицу за счет второго слоя, который будет занят этими кластерными соединениями. Последним дополнением к этой многоярусной таблице является кластерный ион алюминия Al. 7, который ведет себя как многовалентный атом германия.
Спираль Таблица Менделеева (Роберт В. Харрисон)

Кольцо Периодических Элементов (TROPE)

Периодическая таблица Менделеева (JF Hyde)
Круглая периодическая таблица
Альтернативная круговая периодическая таблица

Спиральная периодическая таблица (Янв Scholten)

Цветок Менделеева (Цветочная таблица Менделеева)

Таблица Менделеева с двоичными электронными оболочками

Таблица Менделеева "Стоу"

Таблица Менделеева и Бейли

Таблица Менделеева (В. Циммерман)

Новый взгляд на Ньюлендс
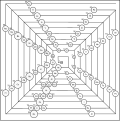
Пирамидальная таблица Менделеева
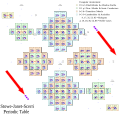
Стоу – Джанет – Скерри с трехмерными электронными орбиталями
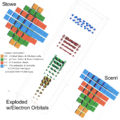
4D Периодическая таблица Стоу – Джанет – Скерри