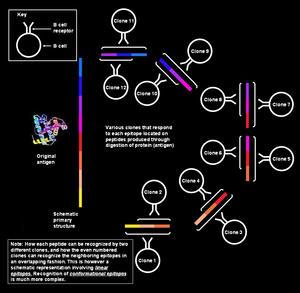
 Поликлональный ответ В-клеток против линейных эпитопов
Поликлональный ответ В-клеток против линейных эпитопов  Примеры веществ, признанных чужеродными (чужеродными)
Примеры веществ, признанных чужеродными (чужеродными) Поликлональный B-клеточный ответ представляет собой естественный тип иммунного ответа, проявляемый адаптивной иммунной системой млекопитающих. Он гарантирует, что один антиген распознается и атакуется через его перекрывающиеся части, называемые эпитопами, множеством клонов B-клетки.
в При нормальном иммунном ответе части патогенов (например, бактерии ) распознаются иммунной системой как чужеродные (чужеродные) и устраняются или эффективно нейтрализуются, чтобы уменьшить их потенциальный ущерб. Такое узнаваемое вещество называется антигеном. Иммунная система может по-разному реагировать на антиген; Ключевой особенностью этого ответа является продукция антител B-клетками (или B-лимфоцитами) с участием одного из звеньев иммунной системы, известного как гуморальный иммунитет. Антитела растворимы и не требуют прямого межклеточного контакта между патогеном и B-клеткой для функционирования.
Антигены могут быть крупными и сложными веществами, и любое отдельное антитело может связываться только с небольшой специфической областью антигена. Следовательно, эффективный иммунный ответ часто включает выработку множества различных антител множеством различных В-клеток против одного и того же антигена. Отсюда термин «поликлональный», который происходит от слов поли, означающих много, и клоны («Klon» = греч. Росток или веточка); клон - это группа клеток, происходящая из общей «материнской» клетки. Антитела, полученные таким образом в результате поликлонального ответа, известны как поликлональные антитела. гетерогенные поликлональные антитела отличаются от молекул моноклональных антител, которые идентичны и реагируют только против одного эпитопа, т.е. являются более специфичными.
Хотя поликлональный ответ дает преимущества иммунной системе, в частности, большую вероятность реакции против патогенов, он также увеличивает шансы развития определенных аутоиммунных заболеваний, возникающих в результате реакции иммунной системы на нативные молекулы, продуцируемые внутри организма. хост.
Заболевания, которые могут передаваться от одного организма к другому, известны как инфекционные болезни, а их причинный биологический агент известен как патоген. Процесс, посредством которого патоген попадает в организм, известен как инокуляция, а организм, на который он влияет, известен как биологический хозяин. Когда патоген закрепляется на этапе, известном как колонизация, он может привести к инфекции, в результате чего хозяин напрямую или через вредные вещества, называемые токсинами, причинит вред хозяину. может производить. Это приводит к появлению различных симптомов и признаков, характерных для инфекционного заболевания, такого как пневмония или дифтерия.
Противодействие различным инфекционным заболеваниям очень важно для выживаемость восприимчивого организма, в частности, и видов в целом. Это достигается хозяином, устраняя патоген и его токсины или делая их нефункциональными. Набор различных клеток, тканей и органов, который специализируется на защите организма от инфекций, известен как иммунная система. Иммунная система достигает этого посредством прямого контакта определенных белых кровяных телец с вторгающимся патогеном, вовлекающим часть иммунной системы, известную как клеточно-опосредованный иммунитет, или путем производства веществ, которые движутся к участкам, удаленным от места их производства, «ищут» болезнетворные клетки и токсины, специфически связываясь с ними, и нейтрализуют их в процессе, известном как гуморальное плечо иммунной системы. Такие вещества известны как растворимые антитела и выполняют важные функции в борьбе с инфекциями.
 Схематическая диаграмма для объяснения механизмов клональной селекции В-клеток
Схематическая диаграмма для объяснения механизмов клональной селекции В-клеток Антитела выполняют различные функции по защите хозяина от патогена. Их растворимые формы, которые выполняют эти функции, продуцируются В-клетками плазмы, типом белых кровяных телец. Это производство строго регулируется и требует активации В-клеток активированными Т-клетками (другой тип белых кровяных телец), что является последовательной процедурой. Основные этапы:
 Этапы производства антител В-клетками: 1.Антиген распознается и поглощается В-клеткой 2. Процессируется антиген 3. Процессированный антиген представлен на поверхности В-клетки 4. В-клетка и Т-клетка взаимно активируют друг друга 5. В-клетки дифференцируются в плазматические клетки с образованием растворимых антител
Этапы производства антител В-клетками: 1.Антиген распознается и поглощается В-клеткой 2. Процессируется антиген 3. Процессированный антиген представлен на поверхности В-клетки 4. В-клетка и Т-клетка взаимно активируют друг друга 5. В-клетки дифференцируются в плазматические клетки с образованием растворимых антител Патогены синтезируют белки, которые могут служить «узнаваемыми » антигены; они могут экспрессировать молекулы на своей поверхности или выпускать их в окружающую среду (жидкости организма). Что делает эти вещества узнаваемыми, так это то, что они очень специфично и несколько прочно связываются с определенными белками хозяина, называемыми антителами. Те же антитела могут быть заякорены на поверхности клеток иммунной системы, и в этом случае они служат рецепторами, или они могут секретироваться в кровь, что известно как растворимые антитела. В молекулярном масштабе белки относительно большие, поэтому их нельзя распознать целиком; вместо этого могут быть распознаны их сегменты, называемые эпитопами. Эпитоп контактирует с очень маленькой областью (из 15–22 аминокислот) молекулы антитела; эта область известна как паратоп. В иммунной системе мембраносвязанные антитела представляют собой рецептор B-клеток (BCR). Кроме того, хотя Т-клеточный рецептор не классифицируется биохимически как антитело, он выполняет аналогичную функцию, поскольку он специфически связывается с эпитопами, образующими комплекс с молекулами главного комплекса гистосовместимости (MHC). Связывание между паратопом и соответствующим ему антигеном очень специфично из-за его структуры и регулируется различными нековалентными связями, в отличие от спаривания других типов лигандов (любой атом, ион или молекула, которая связывается с любым рецептором, по крайней мере, с некоторой степенью специфичности и силы). Специфичность связывания не возникает из-за жесткого типа взаимодействия «замок и ключ», а скорее требует, чтобы паратоп и эпитоп претерпевали небольшие конформационные изменения в присутствии друг друга.
 Распознавание конформационных эпитопов В-клетками. Сегменты, широко разделенные в первичной структуре, вступили в контакт в трехмерной третичной структуре, образующей часть одного и того же эпитопа
Распознавание конформационных эпитопов В-клетками. Сегменты, широко разделенные в первичной структуре, вступили в контакт в трехмерной третичной структуре, образующей часть одного и того же эпитопа На рисунке слева показано, что различные сегменты, образующие эпитоп, непрерывно коллинеарны, что означает, что они показаны как последовательные; однако для обсуждаемой здесь ситуации (то есть распознавания антигена В-клеткой) это объяснение слишком упрощенно. Такие эпитопы известны как последовательные или линейные эпитопы, поскольку все аминокислоты в них находятся в одной последовательности (линии). Этот способ распознавания возможен только в том случае, если пептид имеет небольшой размер (примерно от шести до восьми аминокислот) и используется Т-клетками (Т-лимфоцитами).
Однако B-клетки памяти / наивные клетки распознают интактные белки, присутствующие на поверхности патогена. В этой ситуации белок в его третичной структуре настолько сильно свернут, что некоторые петли аминокислот оказываются внутри белка, а сегменты, фланкирующие их, могут лежать на поверхности. Паратоп на рецепторе В-клеток контактирует только с теми аминокислотами, которые лежат на поверхности белка. Поверхностные аминокислоты на самом деле могут быть прерывистыми в первичной структуре белка, но могут быть соседними из-за сложных паттернов сворачивания белка (как на соседнем рисунке). Такие эпитопы известны как конформационные эпитопы и имеют тенденцию быть длиннее (15–22 аминокислотных остатка), чем линейные эпитопы. Аналогичным образом, антитела, продуцируемые плазматическими клетками, принадлежащими к одному и тому же клону, будут связываться с одними и теми же конформационными эпитопами на патогенных белках.
Связывание специфического антигена с соответствующими молекулами BCR приводит к увеличению продукции MHC- II молекулы. Это имеет значение, поскольку того же не происходит, когда один и тот же антиген интернализуется в результате относительно неспецифического процесса, называемого пиноцитоз, при котором антиген с окружающей жидкостью «поглощается» В-клеткой в виде небольшого пузырька.. Следовательно, такой антиген известен как неспецифический антиген и не приводит к активации В-клетки или последующему образованию антител против нее.
Макрофаги и родственные клетки используют другой механизм для распознавания патогена. Их рецепторы распознают определенные мотивы, присутствующие на вторгающемся патогене, которые вряд ли будут присутствовать в клетке-хозяине. Такие повторяющиеся мотивы распознаются рецепторами распознавания образов (PRR), такими как toll-подобные рецепторы (TLR), экспрессируемые макрофагами. Поскольку один и тот же рецептор может связываться с данным мотивом, присутствующим на поверхностях сильно различающихся микроорганизмов, этот способ распознавания является относительно неспецифическим и представляет собой врожденный иммунный ответ.
 Этапы макрофага, поглощающего патоген
Этапы макрофага, поглощающего патоген После распознавания антигена антигенпрезентирующая клетка, такая как макрофаг или B-лимфоцит, полностью поглощает его в результате процесса, называемого фагоцитоз. Поглощенная частица вместе с некоторым окружающим ее материалом образует эндоцитарную везикулу (фагосому ), которая сливается с лизосомами. Внутри лизосомы антиген расщепляется на более мелкие части, называемые пептидами, с помощью протеаз (ферментов, разрушающих более крупные белки). Затем отдельные пептиды образуют комплекс с молекулами главного комплекса гистосовместимости класса II (MHC класса II ), расположенными в лизосоме - этот метод «обработки» антигена известен как экзогенный или эндоцитарный путь антигена. процессинг в отличие от эндогенного или цитозольного пути, который объединяет аномальные белки, продуцируемые внутри клетки (например, под влиянием вирусной инфекции или в опухолевой клетке) с MHC класса I молекулы.
Также был продемонстрирован альтернативный путь эндоцитарного процессинга, при котором определенные белки, такие как фибриноген и миоглобин, могут связываться в целом с молекулами MHC-II после того, как они денатурированный и их дисульфидные связи являются восстановленными (разрыв связи путем добавления атомов водорода атомов поперек него). Затем протеазы разрушают экспонированные области комплекса белок-MHC II.
После того, как процессированный антиген (пептид) образует комплекс с молекулой MHC, они оба вместе мигрируют в клеточная мембрана, где они проявляются (разрабатываются) в виде комплекса, который может распознаваться CD 4+ (Т-хелперные клетки) - типом белых кровяных телец. Это известно как презентация антигена. Однако эпитопы (конформационные эпитопы), которые распознаются В-клеткой до их переваривания, могут отличаться от эпитопов, представленных Т-хелперной клетке. Кроме того, В-клетка может представлять различные пептиды в комплексе с различными молекулами MHC-II.
Клетки CD 4+ через их Т-клеточный рецептор - CD3 комплекс распознает связанные с эпитопом молекулы MHC II на поверхности антигенпрезентирующих клеток и получает «активированный». После этой активации эти Т-клетки пролиферируют и дифференцируются в Tdiv class="ht" клетки. Это заставляет их производить растворимые химические сигналы, способствующие их собственному выживанию. Однако другой важной функцией, которую они выполняют, является стимуляция В-клеток путем установления прямого физического контакта с ними.
Полная стимуляция Т Для вспомогательных клеток требуется, чтобы молекула B7, присутствующая на антигенпрезентирующей клетке, связывалась с молекулой CD28, присутствующей на поверхности Т-клетки (в непосредственной близости с рецептором Т-клетки). Аналогичным образом, также необходимо второе взаимодействие между лигандом CD40 или CD154 (CD40L ), присутствующим на поверхности Т-клеток, и CD40, присутствующим на поверхности В-клеток. Те же взаимодействия, которые стимулируют Т-хелперные клетки, также стимулируют В-клетки, отсюда и термин костимуляция. Весь механизм гарантирует, что активированная Т-клетка стимулирует только В-клетку, которая распознает антиген, содержащий тот же эпитоп, который распознается Т-клеточным рецептором «костимулирующей» Т-хелперной клетки. В-клетка стимулируется, помимо прямой костимуляции, некоторыми факторами роста, а именно интерлейкинами 2, 4, 5 и 6, по паракринной манере. Эти факторы обычно производятся вновь активированными Т-хелперами. Однако эта активация происходит только после того, как рецептор B-клетки, присутствующий в memory или наивной B-клетке, сам связался бы с соответствующим эпитопом, без чего инициирующие этапы фагоцитоза и антигена обработка не произошла бы.
Наивная (или неопытная) B-клетка - это та, которая принадлежит клону, который никогда не встречал эпитоп, к которому она специфична. Напротив, B-клетка памяти - это та, которая происходит от активированной наивной B-клетки или B-клетки памяти. Активация наивной B-клетки или B-клетки памяти сопровождается множественной пролиферацией этой конкретной B-клетки, большая часть потомства которой окончательно дифференцируется в плазматические B-клетки ; остальные выживают как В-клетки памяти. Итак, когда наивные клетки, принадлежащие к определенному клону, сталкиваются со своим специфическим антигеном, чтобы дать начало плазматическим клеткам, а также оставляют несколько клеток памяти, это называется первичным иммунным ответом. В ходе пролиферации этого клона гены В-клеточного рецептора могут претерпевать частые (одно из каждых двух делений клетки) мутации в генах, кодирующих паратопы антител. Эти частые мутации называются соматической гипермутацией. Каждая такая мутация незначительно изменяет способность паратопа связываться с эпитопом, создавая при этом новые клоны В-клеток. Некоторые из вновь созданных паратопов сильнее связываются с одним и тем же эпитопом (что приводит к отбору клонов, обладающих ими), что известно как созревание аффинности. Другие паратопы лучше связываются с эпитопами, которые немного отличаются от исходного эпитопа, который стимулировал пролиферацию. Вариации в структуре эпитопа также обычно вызываются мутациями в генах патогена, кодирующего их антиген. Таким образом, соматическая гипермутация делает рецепторы В-клеток и растворимые антитела при последующих встречах с антигенами более инклюзивными в их способности распознавания антигенов измененными эпитопами, помимо придания большей специфичности антигену, который в первую очередь индуцировал пролиферацию. Когда антиген стимулирует клетки памяти производить плазматические клетки (точно так же, как в случае первичного ответа клона) и при этом оставляет еще больше клеток памяти, это называется вторичным иммунным ответом, что означает в большее количество плазматических клеток и более высокую скорость производства антител в течение более длительных периодов. В-клетки памяти, продуцируемые как часть вторичного ответа, быстрее распознают соответствующий антиген и более прочно связываются с ним (т.е. с большей аффинностью связывания) благодаря созреванию аффинности. Растворимые антитела, продуцируемые клоном, демонстрируют аналогичное усиление связывания антигена.
Ответы являются поликлональными по природе, поскольку каждый клон в некоторой степени специализируется на продукции антител против данного эпитопа, и потому что, каждый антиген содержит несколько эпитопов, каждый из которых, в свою очередь, может распознаваться более чем одним клоном В-клеток. Чтобы иметь возможность реагировать на бесчисленные антигены, а также на несколько составляющих эпитопов, иммунная система требует способности распознавать очень большое количество эпитопов в целом, то есть должно быть большое разнообразие клонов В-клеток.
Память и наивные В-клетки обычно существуют в относительно небольших количествах. Поскольку организму необходимо иметь возможность реагировать на большое количество потенциальных патогенов, он поддерживает пул B-клеток с широким спектром специфичности. Следовательно, хотя почти всегда есть по крайней мере одна В (наивная или память) клетка, способная реагировать на любой данный эпитоп (из всего, против чего может реагировать иммунная система), существует очень мало точных дубликатов. Однако, когда одна В-клетка встречает антиген, с которым она может связываться, она может очень быстро пролиферировать. Такая группа клеток с идентичной специфичностью по отношению к эпитопу известна как клон и происходит от общей «материнской» клетки. Все «дочерние» В-клетки соответствуют исходной «материнской» клетке по своей эпитопной специфичности и секретируют антитела с идентичнымипаратопами. Эти антитела представляют собой моноклон антителами, поскольку они происходят из клонов одной и той же родительской клетки. Поликлональный ответ - это ответ, при котором клоны нескольких В-клеток реагируют на один и тот же антиген.
 Слепые монахи, исследующие слона : аллегория для поликлонального ответа: каждый клон или антитело распознает разные части одного более крупного антигена
Слепые монахи, исследующие слона : аллегория для поликлонального ответа: каждый клон или антитело распознает разные части одного более крупного антигена Один антиген можно рассматривать как последовательность нескольких перекрывающихся эпитопов. Многие уникальные клоны В-клеток могут связываться с отдельными эпитопами. Это придает еще большую множественность общему отклику. Все эти В-клетки могут активироваться и образовывать большие колонии клонов плазматических клеток, каждую из которых может секретировать до 1000 антител против каждого эпитопа в секунду.
Дополнение к, что разные В-клетки реагируют на разные эпитопы одного и того же антигена, В-клетки, принадлежащие к разным клонам, также могут быть способны реагировать на один и тот же эпитоп. Говорят, что эпитоп, который может атаковать множество различных В-клеток, является высокоиммуногенным. В этих случаях аффинности связывания для соответствующих пар эпитоп-паратоп различают: одни клоны В-клеток продуцируют антитела, которые сильно связываются с эпитопом, а другие продуцируют антитела, которые связываются слабо.
Клоны, которые связываются с конкретным эпитопом с большей силой, с большей вероятностью будут отобраны для дальнейшей пролиферации в зародышевых центрах фолликулов в различных лимфоидных тканях, таких как лимфа узлы. Это мало чем отличается от естественного отбора : клоны отбираются по их способности атаковать эпитопы (сила связывания) на встреченном патогене. Что делает аналогию еще более сильной, так это то, что В-лимфоциты должны конкурировать друг с другом за сигналы, которые способствуют их выживанию в зародышевых центрах.
Хотя многие из которых постоянно мутируют, удивительно, что большинство людей остаются свободными от инфекций. Таким образом, для поддержания здоровья организм должен распознавать все возможные патогены (антигены, которые они включают или вырабатывают). Это достигается за счет поддержания пула больших (около 10) клонов В-клеток, которые реагируют на определенный эпитопа, распознавая и продуцируя антитела против него. Однако в любой момент времени очень немногие клоны остаются восприимчивыми к своему специфическому эпитопу. Таким образом, все вместе взятые клоны В-клетки могут распознавать 10 различных эпитопов. Более того, в течение жизни человеку обычно требуется выработка антител против очень небольшого количества антигенов по сравнению с ним, который организм может распознать и отреагировать на него.
Если антиген может быть распознан более чем одним компонентом его структуры, вероятность того, что он будет «пропущен» иммунной системой, снижается. Мутация патогенных организмов может привести к модификации структуры антигена и, следовательно, эпитопа. Если иммунная система «помнит», как выглядят другие эпитопы, антиген и организм все равно будут распознаваться и подвергаться иммунному ответу организма. Таким образом, поликлональный ответ расширяет диапазон патогенов, которые могут быть распознаны.
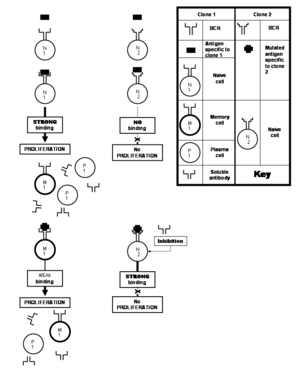 Клон 1, который стимулирует первым антигеном, также стимулирует вторым антигеном, который лучше всего связывается с наивной клеткой клона 2. Однако антитела, продуцируемые плазматическими клетками клона 1, ингибируют пролиферацию клона 2.
Клон 1, который стимулирует первым антигеном, также стимулирует вторым антигеном, который лучше всего связывается с наивной клеткой клона 2. Однако антитела, продуцируемые плазматическими клетками клона 1, ингибируют пролиферацию клона 2. Многие вирусы подвергаются частым мутациям, которые приводят к изменению аминокислотного состава их важные белки. Эпитопы, расположенные на белке, также претерпевать изменения в этом процессе. Такой измененный эпитоп прочно связывается с антителами, специфичными к неизменному эпитопу, стимулированию иммунной системы. Это прискорбно, потому что соматическая гипермутация действительно дает клоны, способные продуцировать растворимые антитела, которые связывали бы измененный эпитоп достаточно активно, чтобы нейтрализовать его. Эти клоны будут состоять из наивных клеток, которые не позволяют пролиферировать слабо связывающиеся антитела, продуцируемые ранее стимулированным клоном. Эта доктрина известна как первоначальный антигенный грех. Этот феномен проявляется, в частности, в иммунных ответах против вирусов гриппа, денге и ВИЧ. Это ограничение, однако, вызвано не явлением поликлонального ответа, а скорее иммунным ответом, который смещен в пользу опытных клеток памяти против "новичков" наивных клеток.
При аутоиммунности иммунная система ошибочно распознает функцию нативные молекулы в организме как чужеродные (аутоантиген) и вырабатывает иммунный ответ против их. Как эти нативные молекулы, как нормальные части тела, естественным образом всегда существуют в организме, против них со временем усиливаются (аналогично вторичному иммунному ответу). Более того, многие организмы проявляют молекулярную мимикрию, которая включает отображение на своей поверхности тех антигенов, которые антигенно подобны белкам-хозяевам. Это имеет два последствия: во-первых, либо организм будет сохранен как аутоантиген; Или, во-вторых, антитела, продуцируемые против него, также будут связываться с имитируемыми нативными белками. Антитела будут атаковать аутоантигены и ткани, вызывающие активацию различных механизмов, таких как активация комплемента и антителозависимая клеточно-опосредованная цитотоксичность. Следовательно, чем шире диапазон специфичности антител, тем выше вероятность того, что или иной будет реагировать против аутоантигенов (нативных молекул организма).
Моноклональные антитела представляют собой структурно идентичные молекулы иммуноглобулинов с идентичной эпитоп-специфичностью (все они связаны с одним и тем же эпитопом с одинаковой аффинностью) по сравнению с их поликлональными аналогами, которые имеют различное сродство к одному и тому же эпитопу. Обычно они не используются при естественном иммунномном ответе, а только при болезненных состояниях, таких как множественная миелома, или с помощью лабораторных методов. Из-за своей специфичности моноклональные антитела используются в определенных функциях обнаружения или обнаружения веществ (как антиген для моноклональных антител) и для нацеливания на отдельные клетки (например, раковые клетки). Моноклональные диагностические методы находят применение в различных методах (см. вестерн-блот и иммунофлуоресценция ) и терапии, особенно рака и заболеваний с аутоиммунным компонентом. Практически все механизмы в природе представляют собой существующие моноклональные антитела менее простого.
Первое свидетельство нейтрализующего вещества в крови, которое может противодействовать инфекциям. пришел, когда Эмиль фон Беринг вместе с Китасато Шибасабуром в 1890 году разработали эффективную сыворотку против дифтерии. Они сделали это, передаем сыворотку, полученную от животных, иммунизированных против дифтерии, животным, страдающим от нее. Таким образом, перенос сыворотки может вылечить инфицированных животных. Беринг был удостоен Нобелевской премии за эту работу в 1901 году.
В то время, хотя химическая природа того, что именно в крови дает эту защиту, не была известна. Через несколько десятилетий было показано, что защитная сыворотка может нейтрализовать и осаждать токсины и скапливать бактерии. Все эти функции приписывались различным веществам в сыворотке и назывались соответственно антитоксином, преципитином и агглютинином. То, что все три вещества представляет собой одно целое (гамма-глобулины ), былоано Элвином А. Кабатом в 1939 году. В прошлом году Кабат применил гетерогенность антител с помощью ультрарифугирования. исследования сывороток лошадей.
До этого момента клеточно-опосредованный иммунитет и гуморальный иммунитет считались конкурирующими теориями, объясняющими эффективный иммунный ответ, но первые отставали из-за отсутствия передовых методов. Клеточный иммунитет получил импульс в своем признании и изучении, когда в 1942 году Меррил Чейз успешно передал иммунитет против туберкулеза между свиньями, передав лейкоциты.
Позже в 1948 году Астрид Фагрей в своей докторской диссертации показала, что плазматические B-клетки специфически участвуют в производстве антител. Роль лимфоцитов в опосредовании как клеточно-опосредованных, так и гуморальных условий была Джеймсом Гоуэнсом в 1959 году.
Чтобы учесть широкий спектр антигенов, которые могут распознавать иммунная система, Пауль Эрлих в 1900 г. Это взаимодействие побуждает клетки, демонстрирующие рецептор, размножаться и повторять больше копий того же рецептора. Эта теория, называемая селективной теорией, не была доказана в течение следующих пятидесятилетия и была поставлена сомнение в использовании учебных теориями, которые основывались на представлении о, что антитело примет свою эффективную структуру, свернувшись вокруг антигена. Однако в конце 1950-х годов работы трех ученых - Джерна, Талмейджа и Бернета (которые в степени изменили теорию) - дали начало теории клонального отбора, которая доказала все элементы гипотезы Эрлиха, за исключением того, что специфические рецепторы, которые вызывают нейтрализовать агент, были растворимы и не связаны с мембраной.
Теория клонального отбора оказалась верной, когда Сэр Густав Носсал показал, что каждая В-клетка всегда продуцирует только одно антитело.
В 1974 году роль MHC в презентации антигена была установлена Рольфом Цинкернагелем и Питером С.. Доэрти.