| Эозинофил | |
|---|---|
 3D визуализация эозинофилов 3D визуализация эозинофилов | |
 эозинофилов под микроскопом (400 ×) из мазка периферической крови. Эритроциты окружают эозинофил, два тромбоцита в верхнем левом углу. эозинофилов под микроскопом (400 ×) из мазка периферической крови. Эритроциты окружают эозинофил, два тромбоцита в верхнем левом углу. | |
| Подробности | |
| Произношение | ) |
| Система | Иммунная система |
| Идентификаторы | |
| MeSH | D004804 |
| TH | H2.00.04.1.02017 |
| FMA | 62861 |
| Анатомические термины микроанатомии. [редактировать в Викиданных ] | |
Эозинофилы, иногда так называемые эозинофилы или, реже, ацидофилы, представляют собой разновидность белых кровяных телец и один из компонентов иммунной системы, ответственных за борьбу с многоклеточные паразиты и некоторые инфекции у позвоночных. Наряду с тучными клетками и базофилами они также контролируют механизмы, связанные с аллергией и астмой. Это гранулоциты, которые развиваются во время гемопоэза в костном мозге перед миграцией в кровь, после чего они окончательно дифференцируются и не размножаются.
Эти клетки являются эозинофильными или «кислотно -любивыми» из-за их больших ацидофильных цитоплазматических гранул, которые проявляют свое сродство к кислотам благодаря сродству к каменноугольные красители : Обычно прозрачные, именно это сродство заставляет их казаться кирпично-красными после окрашивания эозином, красным краситель, используя метод Романовского. Окрашивание концентрируется в небольших гранулах в клеточной цитоплазме, которые содержат множество химических медиаторов, таких как пероксидаза эозинофилов, рибонуклеаза (РНКаза), дезоксирибонуклеазы (ДНКаза), липаза, плазминоген и основной основной белок. Эти медиаторы высвобождаются в процессе, называемом дегрануляцией, после активации эозинофила, и являются токсичными как для тканей паразита, так и для тканей хозяина.
У нормальных людей эозинофилы составляют около 1–3% лейкоцитов и имеют размер около 12–17 микрометров с двулопастными ядрами. В то время как они попадают в кровоток в виде нейтрофилов, эозинофилы находятся в тканях. Они находятся в мозговом веществе и на стыке коры и продолговатого мозга вилочковой железы, а также в нижнем желудочно-кишечном тракте, яичники, матка, селезенка и лимфатические узлы, но не в легких, коже, пищевод или некоторые другие внутренние органы в нормальных условиях. Присутствие эозинофилов в последних органах связано с заболеванием. Например, пациенты с эозинофильной астмой имеют высокий уровень эозинофилов, что приводит к воспалению и повреждению тканей, что затрудняет дыхание пациентам. Эозинофилы сохраняются в кровотоке в течение 8–12 часов и могут выжить в тканях еще 8–12 дней в отсутствие стимуляции. Новаторская работа в 1980-х годах выяснила, что эозинофилы представляют собой уникальные гранулоциты, обладающие способностью выживать в течение продолжительных периодов времени после их созревания, что продемонстрировано экспериментами по культуре ex-vivo.
 Клетки линии крови
Клетки линии крови и ILC2 оба экспрессируют фактор транскрипции GATA-3, который способствует выработке цитокинов TH2, включая интерлейкины (IL). IL- 5 контролирует развитие эозинофилов в костном мозге, поскольку они дифференцируются от миелоидных клеток-предшественников. Судьба их клонов определяется факторами транскрипции, включая GATA и C / EBP. Эозинофилы продуцируют и хранят множество вторичных гранулярных белков до их выхода из костного мозга. После созревания эозинофилы циркулируют в крови и мигрируют к участкам воспаления в тканях или к участкам заражения гельминтами в ответ на хемокины, такие как CCL11 (эотаксин-1), CCL24 (эотаксин-2), CCL5 (RANTES ), 5-гидроксикозатетраеновая кислота и 5-оксо-эйкозатетраеновая кислота, а также некоторые лейкотриены как лейкотриен B4 (LTB4) и MCP1 / 4. Интерлейкин-13, другой цитокин TH2, стимулирует выход эозинофилов из костного мозга, выстилая стенки сосудов молекулами адгезии, такими как VCAM-1 и ICAM-1. Когда эозинофилы активируются, они подвергаются цитолизу, при котором при разрыве клетки высвобождаются эозинофильные гранулы, обнаруженные во внеклеточных ловушках ДНК. Известно, что высокие концентрации этих ДНК-ловушек вызывают повреждение клеток, поскольку содержащиеся в них гранулы ответственны за индуцированную лигандом секрецию эозинофильных токсинов, вызывающих структурные повреждения. Имеются данные, позволяющие предположить, что экспрессия белка гранул эозинофилов регулируется некодирующей РНК EGOT.
 Гистология эозинофила в эпителии, характеризующаяся двулопастным ядром, хотя эозинофильная цитоплазма.
Гистология эозинофила в эпителии, характеризующаяся двулопастным ядром, хотя эозинофильная цитоплазма. После активации эффекторные функции эозинофилов включают выработку следующего:
Там также являются эозинофилами, которые играют роль в борьбе с вирусными инфекциями, о чем свидетельствует обилие РНКаз, которые они содержат в своих гранулах, и удаление фибрина во время воспаления. Эозинофилы, наряду с базофилами и тучными клетками, являются важными медиаторами аллергических реакций и астмы патогенеза и являются связанные с тяжестью заболевания. Они также борются с колонизацией гельминтами (червями) и могут незначительно увеличиваться в присутствии некоторых паразитов. Эозинофилы также участвуют во многих других биологических процессах, включая постпубертатное развитие молочной железы, цикл эструса, отторжение аллотрансплантата и неоплазию. Они также участвуют в презентации антигена в Т-клетках.
. Эозинофилы ответственны за повреждение тканей и воспаление при многих заболеваниях, включая астму. Было обнаружено, что высокие уровни интерлейкина-5 усиливают экспрессию молекул адгезии, которые затем способствуют адгезии эозинофилов к эндотелиальным клеткам, вызывая воспаление и повреждение тканей.
Накопление эозинофилов в слизистая оболочка носа считается основным диагностическим критерием аллергического ринита (аллергии носа).
После активации иммунным стимулом эозинофилы дегранулируют с высвобождением массива цитотоксических гранулярных катионных белков, которые способны вызывать повреждение и дисфункцию тканей. К ним относятся:
Основной основной белок, пероксидаза эозинофилов и катионный белок эозинофилов токсичны для многих тканей. Катионный белок эозинофилов и нейротоксин, происходящий от эозинофилов, представляют собой рибонуклеазы с противовирусной активностью. Главный основной белок индуцирует дегрануляцию тучных клеток и базофилов и участвует в ремоделировании периферического нерва. Катионный белок эозинофилов создает токсичные поры в мембранах клеток-мишеней, позволяя проникать в клетку другим цитотоксическим молекулам, может ингибировать пролиферацию Т-клеток, подавлять антитело продуцирование В-клетками, индуцирует дегрануляцию тучными клетками и стимулирует фибробласты к секреции слизи и гликозаминогликана. Эозинофильная пероксидаза образует активные формы кислорода, которые способствуют окислительному стрессу в мишени, вызывая гибель клеток в результате апоптоза и некроза.
Увеличение количества эозинофилов, т.е. присутствие более 500 эозинофилов на микролитр крови, называется эозинофилией и обычно наблюдается у людей с паразитарной инвазией. кишечника ; аутоиммунное и коллагенососудистое заболевание (такое как ревматоидный артрит ) и системная красная волчанка ; злокачественные заболевания, такие как эозинофильный лейкоз, клональная гиперэозинофилия и болезнь Ходжкина ; лимфоцитарная гиперэозинофилия ; обширные кожные заболевания (такие как эксфолиативный дерматит ); болезнь Аддисона и другие причины низкой продукции кортикостероидов (кортикостероиды подавляют уровень эозинофилов в крови); рефлюкс-эзофагит (при котором эозинофилы обнаруживаются в плоском эпителии пищевода) и эозинофильный эзофагит ; и с использованием некоторых лекарств, таких как пенициллин. Но, пожалуй, наиболее частой причиной эозинофилии является аллергическое состояние, такое как астма. В 1989 году зараженные добавки L-триптофана вызвали смертельную форму эозинофилии, известную как синдром эозинофилии-миалгии, которая напоминала синдром токсического масла в Испании в 1981.
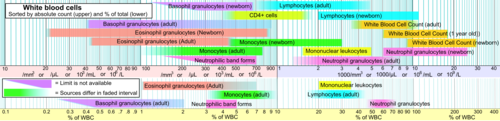 Референсные диапазоны для анализов крови лейкоцитов, сравнение количества эозинофильных гранулоцитов (показано светло-красным) с другими клетками
Референсные диапазоны для анализов крови лейкоцитов, сравнение количества эозинофильных гранулоцитов (показано светло-красным) с другими клетками Эозинофилы играют важную роль при астме, поскольку количество накопленных эозинофилов соответствует выраженность астматической реакции. Показано, что эозинофилия на моделях мышей связана с высокими уровнями интерлейкина-5. Кроме того, биопсия слизистой оболочки бронхов, проведенная у пациентов с такими заболеваниями, как астма, показала более высокие уровни интерлейкина-5, что ведет к более высоким уровням эозинофилов. Инфильтрация эозинофилов при таких высоких концентрациях вызывает воспалительную реакцию. В конечном итоге это приводит к ремоделированию дыхательных путей и затруднению дыхания.
Эозинофилы также могут вызывать повреждение тканей в легких у пациентов с астмой. Высокие концентрации основного основного белка эозинофилов и нейротоксина, происходящего от эозинофилов, которые приближаются к цитотоксическим уровням, наблюдаются в местах дегрануляции в легких, а также в астматической мокроте.
Лечение, используемое для борьбы с аутоиммунными заболеваниями. заболевания и состояния, вызываемые эозинофилами, включают:
Моноклональные антитела, такие как дупилумаб и лебрикизумаб нацеленный на IL-13 и его рецептор, который снижает эозинофильное воспаление у пациентов с астмой за счет снижения количества молекул адгезии, с которыми связываются эозинофилы, тем самым уменьшая воспаление. Меполизумаб и бенрализумаб - это другие варианты лечения, которые нацелены на альфа-субъединицу рецептора IL-5, тем самым подавляя его функцию и уменьшая количество развивающихся эозинофилов, а также количество эозинофилов, ведущих к воспалению через антитело-зависимые клетки, опосредованные цитотоксичность и эозинофильный апоптоз.
В жировой (жировой ) ткани CCR2 дефицитных мышей имеется повышенное количество эозинофилов, большая альтернатива макрофагам активации и склонность к экспрессии цитокина типа 2 . Кроме того, этот эффект был преувеличен, когда мыши стали ожирением из-за диеты с высоким содержанием жиров. Мышиные модели эозинофилии от мышей, инфицированных T. canis показал увеличение мРНК IL-5 в селезенке мышей. Мышиные модели астмы из OVA показывают более высокий ответ TH2. Когда мышам вводят IL-12 для индукции ответа TH1, ответ TH2 становится подавленным, что показывает, что у мышей без цитокинов TH2 значительно реже проявляются симптомы астмы.