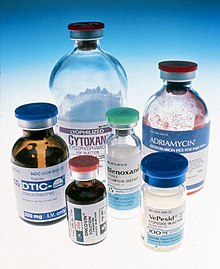
 Шесть флаконов с химиотерапевтическими средствами для инъекций, продаваемых в США c. 1993. По часовой стрелке от центра: блеомицин, противоопухолевый антибиотик ; винкристин, веретенообразный яд ; дакарбазин, алкилирующий агент ; циклофосфамид, азотистый иприт ; доксорубицин, антрациклин ; и этопозид, ингибитор топоизомеразы.
Шесть флаконов с химиотерапевтическими средствами для инъекций, продаваемых в США c. 1993. По часовой стрелке от центра: блеомицин, противоопухолевый антибиотик ; винкристин, веретенообразный яд ; дакарбазин, алкилирующий агент ; циклофосфамид, азотистый иприт ; доксорубицин, антрациклин ; и этопозид, ингибитор топоизомеразы.Эра рака химиотерапия началась в 1940-х годах с первого использования азотистых ипритов и препараты-антагонисты фолиевой кислоты. Революция таргетной терапии произошла, но многие принципы и ограничения химиотерапии, открытые ранними исследователями, все еще применимы.
Начало современной эры химиотерапии рака можно проследить непосредственно до внедрения Германией химического оружия во время Первой мировой войны. использовались химические вещества, иприт был особенно разрушительным. Хотя это и было запрещено Женевским протоколом в 1925 году, начало Второй мировой войны вызвало опасения по поводу возможного повторного применения химического оружия. Такие опасения привели к открытию азотного иприта, боевого химического агента, в качестве эффективного средства лечения рака. Два фармаколога из Йельской школы медицины, Луис С. Гудман и Альфред Гилман были наняты Министерством США. Министерства обороны для исследования потенциальных терапевтических применений агентов химической войны. Гудман и Гилман заметили, что иприт слишком летучий агент, чтобы быть подходящим для лабораторных экспериментов. Они заменили молекулу азота на серу и получили более стабильное соединение в азотном иприте. Через год после начала их исследования немецкий воздушный налет в Бари, Италия привел к тому, что более 1000 человек подверглись воздействию секретного груза СС Джона Харви, состоящего из горчичный газ бомбы. Доктор Стюарт Фрэнсис Александр, подполковник, который был экспертом в области химического оружия, был впоследствии направлен для расследования последствий. Вскрытие жертв показало, что после воздействия имело место глубокое лимфоидное и миелоидное подавление. В своем отчете д-р Александер предположил, что, поскольку горчичный газ практически прекратил деление определенных типов соматических клеток, природа которых заключалась в быстром делении, он также потенциально может быть использован для помощи в подавлении деления. определенных типов раковых клеток.
Используя эту информацию, Гудман и Гилман пришли к выводу, что этот агент может быть использован для лечения лимфомы, опухоли из лимфоидных клеток. Сначала они создали модель на животных, установив лимфомы у мышей и продемонстрировали, что могут лечить их горчичными препаратами. Затем, в сотрудничестве с торакальным хирургом Густавом Линдскогом, они ввели родственный агент, мустин (прототип азотистого иприта противораковый химиотерапевтический препарат) пациенту с неходжкинская лимфома. Они наблюдали резкое уменьшение массы опухоли пациента. Хотя эффект длился всего несколько недель, и пациенту пришлось вернуться для прохождения еще одного курса лечения, это был первый шаг к осознанию того, что рак можно лечить фармакологическими средствами. Публикация первых клинических испытаний была опубликована в 1946 году в New York Times.
 Работа Фарбера сыграла важную роль в демонстрации возможности эффективного фармакологического лечения рака, и по сей день он считается лучшим лекарством от рака. отец современной химиотерапии.
Работа Фарбера сыграла важную роль в демонстрации возможности эффективного фармакологического лечения рака, и по сей день он считается лучшим лекарством от рака. отец современной химиотерапии.Вскоре после Второй мировой войны начался второй подход к лекарственной терапии рака. Сидни Фарбер, патолог из Гарвардской медицинской школы, изучал влияние фолиевой кислоты на больных лейкемией. Фолиевая кислота, витамин, имеющий решающее значение для метаболизма ДНК (в то время он не знал значения ДНК ), была обнаружена Люси Уиллс, когда она работал в Индии в 1937 году. Казалось, что он стимулировал пролиферацию клеток острого лимфобластного лейкоза (ALL) при введении детям с этим раком. В одном из первых примеров рационального дизайна лекарств (а не случайного открытия) Фарбер использовал аналоги фолиевой кислоты, синтезированные Харриет Килти и Йеллапрагада Суббаров из Lederle Laboratories. Эти аналоги - сначала аминоптерин, а затем аметоптерин (теперь метотрексат) были антагонистами фолиевой кислоты и блокировали функцию ферментов, требующих фолиевой кислоты. При введении детям с ОЛЛ в 1948 году эти агенты стали первыми лекарствами, вызывавшими ремиссию у детей с ОЛЛ. Ремиссия была короткой, но принцип был ясен - антифолаты могут подавлять пролиферацию злокачественных клеток и тем самым восстанавливать нормальную функцию костного мозга. Фарбер столкнулся с сопротивлением к проведению своих исследований в то время, когда в медицине считалось, что лейкемия неизлечима и что детям следует позволить умереть спокойно. Впоследствии отчет Фарбера 1948 года в Медицинском журнале Новой Англии был встречен с недоверием и насмешками.
В 1947 году Высшая лига бейсбола Зал славы Бэйб Рут, который боролся с раком носоглотки, стал одним из первых людей, получивших лечение птероилтриглутаматом (также известный под его торговой маркой «Тероптерин» и аналогичный аминоптерину). Доктор Ричард Льюисон из больницы Маунт Синай в Нью-Йорке ввел препарат, и в течение нескольких месяцев состояние Рут начало улучшаться. Однако в следующем году Рут умерла.
В 1951 году Джейн С. Райт продемонстрировала использование метотрексата при солидных опухолях, продемонстрировав ремиссию. при раке груди. Группа Райта была первой, кто продемонстрировал применение препарата при солидных опухолях в отличие от лейкозов, которые представляют собой рак костного мозга. Несколько лет спустя в Национальном институте рака и Мин Чиу Ли затем продемонстрировали полную ремиссию у женщин с хориокарциномой и хориоаденомой в 1956 г. открытие того, что только метотрексат может вылечить хориокарциному (1958), злокачественное новообразование зародышевых клеток, которое возникает в трофобластических клетках плаценты. В 1960 г. Райт и др. вызвал ремиссию грибовидного микоза.
Джозеф Бурченал в Мемориальном онкологическом центре Слоуна-Кеттеринга в Нью-Йорке, с помощью Фарбера начал свое собственное исследование метотрексата и обнаружил такие же эффекты. Затем он решил попытаться разработать антиметаболиты так же, как Фарбер, путем внесения небольших изменений в метаболит, необходимый клетке для деления. С помощью Джорджа Хитчингса и Гертруды Элион, двух химиков-фармацевтов, которые работали в Burroughs Wellcome Co. в Tuckahoe, многие Были протестированы аналоги пурина, в результате чего был открыт 6-меркаптопурин (6-MP), который, как впоследствии было показано, является высокоактивным противолейкозным лекарственным средством.
Группа натуральных продуктов Eli Lilly обнаружила, что алкалоиды из мадагаскарского барвинка (Vinca rosea), первоначально обнаруженный при проверке антидиабетических препаратов, блокировал пролиферацию опухолевых клеток. Позже было показано, что противоопухолевый эффект алкалоидов барвинка (например, винкристин ) обусловлен их способностью ингибировать щелочи полимеризации микротрубочек и, следовательно, деление клеток.
NCI, возглавляемый доктором Джоном Р. Хеллером-младшим, лоббировал Конгресс США в отношении финансовых поддержка исследований химиотерапии второго поколения. В ответ Конгресс создал (NCCSC) в NCI в 1955 году. Это была первая федеральная программа по содействию открытию лекарств от рака - в отличие от нынешнего, большинство фармацевтических компаний еще не были заинтересованы в разработке противоопухолевых препаратов. NCCSC разработал методологии и важные инструменты (например, клеточные линии и животные модели ) для разработки химиотерапевтических средств.
В 1965 году произошел крупный прорыв в лечении рака. Джеймс Ф. Холланд, Эмиль Фрейрих и Эмиль Фрей выдвинули гипотезу, что химиотерапия рака должна следовать стратегии антибактериальной терапии туберкулеза с комбинациями лекарств, каждый из которых разный механизм действия. Раковые клетки предположительно могут мутировать, чтобы стать устойчивыми к одному агенту, но при одновременном применении разных лекарств для опухоли будет труднее развить устойчивость к комбинации. Холланд, Фрейрих и Фрей одновременно вводили метотрексат (антифолат), винкристин (алкалоид барвинка), 6- меркаптопурин (6-MP) и преднизон - вместе именуемые режимом POMP - и вызывал длительную ремиссию у детей с острым лимфобластным лейкозом (ALL). С постепенным уточнением оригинальных схем с использованием рандомизированных клинических исследований St. Детская исследовательская больница Джуд, Совет медицинских исследований в Великобритании (протоколы UKALL) и в Германии Берлин - Франкфурт - Мюнстер В группе клинических испытаний (протоколы ALL-BFM) ОЛЛ у детей стала в значительной степени излечимой болезнью.
Этот подход был распространен на лимфомы в 1963 году Винсентом Т. ДеВита и Джорджем Канеллосом из NCI, которые окончательно доказали в конце 1960-х годов, что азотный иприт, винкристин, прокарбазин и преднизон - известные как режим MOPP - могут вылечить пациентов с лимфомой Ходжкина и неходжкинской лимфомой.
В настоящее время почти все успешные режимы химиотерапии рака используют эту парадигму одновременного приема нескольких препаратов, называемую комбинированной химиотерапией или полихимиотерапией .
Согласно исследованиям на животных моделях, лекарства были наиболее эффективны при использовании у пациентов с опухолями меньшего объема. Из этого была разработана еще одна важная стратегия - если бы опухолевую нагрузку можно было сначала уменьшить с помощью хирургического вмешательства, то химиотерапия могла бы удалить любые оставшиеся злокачественные клетки, даже если бы она не была достаточно мощной, чтобы полностью уничтожить опухоль. Этот подход получил название «адъювантная терапия».
Эмиль Фрей впервые продемонстрировал этот эффект - высокие дозы метотрексата предотвратили рецидив остеосаркомы после хирургического удаления первичной опухоли. Позже было показано, что 5-фторурацил, который ингибирует тимидилатсинтазу, улучшает выживаемость при использовании в качестве адъюванта к хирургическим вмешательствам при лечении пациентов с раком толстой кишки. Точно так же знаковые испытания Бернарда Фишера, председателя Национального проекта хирургической адъювантной терапии груди и кишечника, и работающего в Италии, доказали, что адъювантная химиотерапия После полной хирургической резекции опухоли груди значительно увеличилась выживаемость, особенно при более запущенных формах рака.
В 1956 году К. Гордон Зуброд, который ранее руководил разработкой противомалярийных препаратов для армии США, возглавил Отдел лечения рака NCI и руководил разработкой новых лекарств. В течение двух десятилетий, последовавших за созданием NCCSC, под эгидой NCI возникла большая сеть совместных клинических групп для тестирования противоопухолевых агентов. Зуброд проявлял особый интерес к натуральным продуктам и разработал широкую программу сбора и тестирования растительных и морских источников, противоречивую программу, которая привела к открытию таксанов (в 1964 году) и камптотецинов (в 1966 году). Оба класса лекарственных средств были выделены и охарактеризованы лабораторией Монро Уолл в Research Triangle Institute.
Паклитаксел (Таксол) был новым антимитотическим агентом, который способствовал развитию сборка микротрубочек. Этот агент оказалось сложно синтезировать, и его можно было получить только из коры тихоокеанского тиса, что вынудило NCI заняться дорогостоящим бизнесом по сбору значительных количеств тиса на государственных землях. После 4 лет клинических испытаний на солидных опухолях в 1987 г. (через 23 года после первоначального открытия) было обнаружено, что он эффективен при терапии рака яичников. Примечательно, что этот агент, хотя и был разработан NCI в партнерстве с Bristol-Myers Squibb, продавался исключительно компанией BMS (которая использовала синтетическую методологию, разработанную Робертом Холтоном в Университете штата Флорида), которая продолжала производить Таксол принес прибыль более миллиарда долларов.
Другим классом наркотиков, разработанным Национальным институтом клинических исследований, были камптотецины. Камптотецин, полученный из китайского декоративного дерева, ингибирует топоизомеразу I, фермент, который позволяет раскручивать ДНК. Несмотря на обнадеживающие результаты в доклинических исследованиях, в ранних клинических испытаниях препарат проявлял небольшую противоопухолевую активность, а дозировка была ограничена токсичностью для почек : его лактоновое кольцо нестабильно при нейтральном pH, поэтому в кислой среде почек он становится активным, повреждая почечные канальцы. В 1996 году более стабильный аналог, иринотекан, получил одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для лечения рака толстой кишки. Позже этот агент также будет использоваться для лечения рака легких и яичников.
Цисплатин, соединение на основе платины, было обнаружено исследователем Мичиганского государственного университета, Барнеттом Розенбергом, работает по контракту NCI. Это было еще одним случайным открытием: Розенберг изначально хотел исследовать возможные эффекты электрического поля на рост бактерий. Он заметил, что бактерии неожиданно перестали делиться, когда их помещали в электрическое поле. Взволнованный, он провел месяцы испытаний, пытаясь объяснить это явление. Он был разочарован, обнаружив, что причиной был экспериментальный артефакт - ингибирование бактериального деления было связано с продуктом электролиза платинового электрода, а не с электрическим поле. Это случайное открытие, однако, вскоре положило начало серии исследований влияния соединений платины на деление клеток, что привело к синтезу цисплатина. Этот препарат сыграл ключевую роль в лечении рака яичек. Впоследствии и другие сотрудники Института исследований рака в Соединенном Королевстве расширили клиническую ценность соединений платины, разработав карбоплатин, производное цисплатина с широкой противоопухолевой активностью и сравнительно меньшей нефротоксичность.
Вторая группа с контрактом NCI во главе с Джоном Монтгомери из Южного исследовательского института синтезировала нитрозомочевины, и алкилирующий агент, сшивающий ДНК. Флударабин фосфат, аналог пурина, который стал основой лечения пациентов с хроническим лимфолейкозом, был еще одной аналогичной разработкой Montgomery.
Другие эффективные молекулы также поступили из промышленности в период с 1970 по 1990 год, включая антрациклины и эпиподофиллотоксины - оба из которых ингибировал действие топоизомеразы II, фермента, имеющего решающее значение для синтеза ДНК.
Как очевидно из их происхождения, вышеупомянутые химиотерапевтические методы лечения рака по существу являются ядами. Пациенты, получавшие эти агенты, испытали серьезные побочные эффекты, которые ограничивали вводимые дозы и, следовательно, ограничивали полезные эффекты. Клинические исследователи поняли, что способность управлять этими токсическими эффектами имеет решающее значение для успеха химиотерапии рака.
Следует отметить несколько примеров. Многие химиотерапевтические агенты вызывают сильное угнетение костного мозга. Это обратимо, но для восстановления требуется время. Поддержка тромбоцитами и переливаниями эритроцитов, а также антибиотиками широкого спектра действия в случае инфекции в этот период имеет решающее значение для выздоровления пациента.
Также стоит упомянуть несколько практических факторов. Большинство этих агентов вызывало очень сильную тошноту (в литературе называемую тошнотой и рвотой (CINV), вызванной химиотерапией), которая, хотя и не вызывала непосредственной смерти пациентов, была невыносимой при более высоких дозах. Разработка новых препаратов для предотвращения тошноты (прототипом которых был ондансетрон ) имела большое практическое применение, как и конструкция постоянных внутривенных катетеров (например, линии Хикмана и Линии PICC ), что позволило безопасно назначать химиотерапию, а также поддерживающую терапию.
Одним из важных достижений этого периода было открытие средства, которое позволяло вводить ранее смертельные дозы химиотерапии. Сначала был взят костный мозг пациента, проведена химиотерапия, а затем собранный костный мозг вернулся пациенту через несколько дней. Этот подход, названный аутологичной трансплантацией костного мозга, первоначально считался полезным для широкой группы пациентов, включая пациентов с распространенным раком груди. Однако тщательные исследования не подтвердили это преимущество, и аутотрансплантация больше не широко используется при солидных опухолях. Доказанные лечебные преимущества высоких доз химиотерапии, обеспечиваемые аутологичным спасением костного мозга, ограничены как пациентами с лимфомой Ходжкина, так и некоторыми пациентами с неходжкинской лимфомой, которые не прошли терапию традиционной комбинированной химиотерапией. Аутологичная трансплантация продолжает использоваться в качестве компонента терапии ряда других гематологических злокачественных новообразований.
За это время был признан гормональный вклад в несколько категорий подтипов рака груди, что привело к разработка фармакологических модуляторов (например, эстрогена ), таких как тамоксифен.
 bcr-abl киназа, которая вызывает CML, ингибируемая иматинибом (small молекула).
bcr-abl киназа, которая вызывает CML, ингибируемая иматинибом (small молекула). Молекулярная генетика обнаружила сигнальные сети, которые регулируют клеточную активность, такую как пролиферация и выживание. При конкретном раке такая сеть может быть радикально изменена из-за случайной соматической мутации. Таргетная терапия подавляет метаболический путь, лежащий в основе этого типа деления раковых клеток.
Классическим примером направленной разработки является мезилат иматиниба (Gleevec), небольшая молекула, которая ингибирует сигнальную молекулу киназа. Долгое время было известно, что генетическая аномалия, вызывающая хронический миелогенный лейкоз (ХМЛ), представляет собой хромосомную транслокацию, создающую аномальный гибридный белок, киназу BCR-ABL, который сигнализирует аномально, ведущий к неконтролируемому разрастанию лейкозных клеток. Иматиниб точно ингибирует эту киназу. В отличие от многих других противораковых средств, это лекарство не было случайностью. Брайан Друкер, работающий в Орегонском университете здравоохранения и науки, тщательно исследовал аномальную ферментную киназу при ХМЛ. Он рассудил, что именно ингибирование этой киназы лекарством будет контролировать болезнь и мало повлияет на нормальные клетки. Друкер сотрудничал с Novartis химиком Николасом Лайдоном, который разработал несколько кандидатов в ингибиторы. Из них было обнаружено, что иматиниб является наиболее перспективным для лабораторных экспериментов. Сначала Druker, а затем другие группы по всему миру продемонстрировали, что при использовании этой небольшой молекулы для лечения пациентов с хронической фазой CML 90% достигают полной гематологической ремиссии. Есть надежда, что молекулярное нацеливание на подобные дефекты при других формах рака будет иметь такой же эффект.
Еще одним направлением таргетной терапии является растущее использование моноклональных антител в терапии рака. Хотя моноклональные антитела (иммунные белки, которые могут быть выбраны для точного связывания практически с любой мишенью) существуют уже несколько десятилетий, они были получены от мышей и не очень хорошо функционировали при введении людям, вызывая аллергические реакции и быстро удаляемые из кровотока. "" этих антител (генетически трансформируя их, чтобы они были максимально похожи на человеческие антитела) позволили создать новое семейство высокоэффективных гуманизированных моноклональных антител. Трастузумаб, препарат, используемый для лечения рака груди, является ярким примером.
Открытие того, что определенные токсичные химические вещества, вводимые в комбинации, могут вылечить определенные виды рака, считается одним из величайших в современной медицине. Детство ВСЕ, рак яичек и болезнь Ходжкина, ранее повсеместно фатальная, теперь обычно излечимы. Обычная цитотоксическая химиотерапия показала способность излечивать некоторые виды рака, включая рак яичек, болезнь Ходжкина, неходжкинскую лимфому и некоторые лейкемии. Он также оказался эффективным при использовании адъюванта для снижения риска рецидива после операции по поводу рака груди высокого риска, рака толстой кишки и рака легких, среди прочего.
Общее влияние химиотерапии на выживаемость при раке может быть трудно оценить, поскольку улучшение скрининга, профилактики (например, кампании по борьбе с курением) и выявления рака влияют на статистику заболеваемости и смертности от рака. В Соединенных Штатах общий уровень заболеваемости раком был стабильным с 1995 по 1999 год, в то время как уровень смертности от рака неуклонно снижался с 1993 по 1999 год. Опять же, это, вероятно, отражает совокупное влияние улучшенного скрининга, профилактики и лечения. Тем не менее, рак остается основной причиной болезней и смерти, и обычная цитотоксическая химиотерапия оказалась неспособной вылечить большинство видов рака после метастазирования.