 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Camptosar, Campto, Onivyde и другие |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a608043 |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы. введения | Внутривенное |
| Код АТС | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | NA |
| Метаболизм | Печень глюкуронизация |
| Период полувыведения | от 6 до 12 часов |
| Выведение | Билиарный и почка |
| Идентификаторы | |
Название IUPAC
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| CompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.219.260 |
| Химические и физические данные | |
| Формула | C33H38N4O6 |
| Молярная масса | 586,689 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
| (что это?) | |
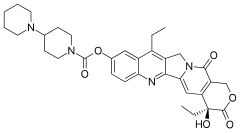
Иринотекан, продается под торговой маркой Camptosar среди прочих ers, представляет собой лекарство, используемое для лечения рака толстой кишки и мелкоклеточного рака легкого. При раке толстой кишки его применяют отдельно или с фторурацилом. При мелкоклеточном раке легкого он используется с цисплатином. Его вводят путем медленной инъекции в вену..
Общие побочные эффекты включают диарею, рвоту, подавление костного мозга, выпадение волос, короткое замыкание. дыхание и жар. Другие серьезные побочные эффекты включают сгустки крови, воспаление толстой кишки и аллергические реакции. Те, у кого есть две копии варианта гена UGT1A1 * 28, подвержены более высокому риску побочных эффектов. Использование во время беременности может нанести вред ребенку. Иринотекан относится к семейству препаратов ингибиторов топоизомеразы. Он действует путем блокирования топоизомеразы 1, что приводит к повреждению ДНК и гибели клеток.
Иринотекан был одобрен для медицинского применения в США в 1996 году. 200>Список основных лекарственных средств Всемирной организации здравоохранения. Он сделан из природного соединения камптотецина, которое содержится в китайском декоративном дереве Camptotheca acuminata.
Его основное применение - рак толстой кишки, в частности, в сочетании с другими химиотерапевтическими агентами. Это включает схему FOLFIRI, которая состоит из инфузионного 5-фторурацила, лейковорина и иринотекана. Схема XELIRI состоит из капецитабина и иринотекана.
Он также может использоваться вместе с фторурацилом и фолиевой кислотой для рака поджелудочной железы после неудачного первоначального лечения.
К наиболее значительным побочным эффектам иринотекана относятся диарея, тошнота и рвота, нейтропения и лихорадка, инфекции крови или легких (сепсис, пневмония), шок, обезвоживание, почечная недостаточность и тромбоцитопения (низкая
Диарея, связанная с иринотеканом, является тяжелой и клинически значимой, иногда приводящей к тяжелому обезвоживанию, требующему госпитализации или приема в отделение интенсивной терапии. Этот побочный эффект купируется агрессивным применением противодиарейных средств, таких как лоперамид или ко-фенотроп при первом жидком дефекации.
Иринотекан отрицательно влияет на иммунную систему. Это отражается в резко сниженном количестве лейкоцитов в крови, в частности нейтрофилов. Пациент может испытывать период нейтропении (клинически значимое снижение нейтрофилов в крови), в то время как костный мозг увеличивает выработку лейкоцитов для компенсации.
Камптотецин, одна из четырех основных структурных классификаций противораковых соединений растительного происхождения, представляет собой цитотоксический алкалоид, который состоит из пентациклической кольцевой структуры, содержащей пиррол (3, 4 β) хинолиновый фрагмент, лактоновая форма S-конфигурации и карбоксилатная форма. Иринотекан активируется гидролизом до SN-38, ингибитора топоизомеразы I. Затем он инактивируется глюкуронидированием уридиндифосфатглюкуронозилтрансферазой 1A1 (UGT1A1 ). Ингибирование топоизомеразы I активным метаболитом SN-38 в конечном итоге приводит к ингибированию как репликации ДНК, так и транскрипции.
Молекулярное действие иринотекана происходит путем улавливания подмножества топоизомеразы -1- Комплексы расщепления ДНК, содержащие гуанин +1 в последовательности ДНК. Одна молекула иринотекана накладывается на пары оснований, фланкирующие сайт расщепления, индуцированного топоизомеразой, и отравляет (инактивирует) фермент топоизомераза 1.
Щелкните гены, белки и метаболиты ниже для ссылки на соответствующие статьи.
[[File: [[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]]
[[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]] | {{bSize}}} px | alt = Irinotecan Pathway edit ]] Irinotecan Pathway edit
| {{bSize}}} px | alt = Irinotecan Pathway edit ]] Irinotecan Pathway edit Иринотекан преобразован ферментом в его активный метаболит SN-38, который, в свою очередь, инактивируется ферментом UGT1A1 путем глюкуронизации.
Люди с вариантами UGT1A1, называемыми TA 7, также известными как «вариант * 28», экспрессируют меньше ферментов UGT1A1 в печени и часто имеют синдром Гилберта. Во время химиотерапии они эффективно получают более высокую дозу, чем ожидалось, потому что их организм не может выводить иринотекан так быстро, как другие. В исследованиях это соответствует более высокой частоте тяжелой нейтропении и диареи.
В 2004 году было проведено клиническое исследование, которое проспективно подтвердило связь варианта * 28 с большей токсичностью, а также способность генетического тестирования предсказать это. токсичность до введения химиотерапии.
В 2005 году FDA внесло изменения в маркировку иринотекана, добавив рекомендации по фармакогеномике, чтобы реципиенты иринотекана с гомозиготностью (оба из (две копии гена) в гене UGT1A1, а именно вариант * 28, следует учитывать при снижении доз лекарства. Иринотекан - один из первых широко используемых химиотерапевтических агентов, дозировка которого зависит от генотипа реципиента.
Иринотекан получил ускоренное одобрение в США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в 1996 г. и полное одобрение в 1998 г.
Во время разработки он был известен как CPT-11.
Инкапсулированная в липосомы версия иринотекана, продаваемая как Onivyde компанией Merrimack Pharmaceuticals, была одобрена FDA в октябре 2015 года для лечения метастатического рака поджелудочной железы. Он был одобрен для медицинского использования в Европейском Союзе в октябре 2016 года.