| тимидилатсинтаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер EC | 2.1.1.45 | ||||||||
| Номер CAS | 9031 -61-2 | ||||||||
| Базы данных | |||||||||
| IntEnz | Представление IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Представление NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология гена | AmiGO / QuickGO | ||||||||
| |||||||||
| тимидилатсинтаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Thymidylat_synt | ||||||||
| Pfam | PF00303 | ||||||||
| InterPro | IPR000398 | ||||||||
| PROSITE | PDOC00086 | ||||||||
| SCOPe | 1tys / SUPFAM | ||||||||
| |||||||||
Тимидилатсинтаза (TS) (EC 2.1.1.45 ) - это фермент, который катализирует превращение дезоксиуридинмонофосфат (dUMP) на дезокситимидинмонофосфат (dTMP). Тимидин является одним из нуклеотидов ДНК. При ингибировании TS возникает дисбаланс дезоксинуклеотидов и повышенные уровни dUMP. Оба вызывают повреждение ДНК.
Следующая реакция катализируется тимидилатсинтазой:
 дигидрофолат + dTMP
дигидрофолат + dTMPПосредством восстановительного метилирования, дезоксиуридинмонофосфат (dUMP) и N5, N10-метилентетрагидрофолат вместе используются для образования dTMP, давая дигидрофолат в качестве вторичного продукта.
Это обеспечивает единственный de novo путь производства dTMP и единственный фермент метаболизма фолиевой кислоты, в котором 5,10-метилентетрагидрофолат окисляется во время одноуглеродного переноса. Фермент необходим для регулирования сбалансированного поступления 4-х предшественников ДНК при нормальной репликации ДНК: дефекты активности фермента, влияющие на процесс регуляции, вызывают различные биологические и генетические аномалии, такие как смерть без тимина. Фермент является важной мишенью для некоторых химиотерапевтических препаратов. Тимидилатсинтаза представляет собой фермент с примерно 30-35 k Da у большинства видов, за исключением простейших и растений, где он существует в виде бифункционального фермента, который включает домен дигидрофолатредуктазы. Остаток цистеина участвует в каталитическом механизме (он ковалентно связывает промежуточное соединение 5,6-дигидро-dUMP). Последовательность вокруг активного сайта этого фермента сохраняется от фагов до позвоночных.
Тимидилатсинтаза индуцируется фактором транскрипции LSF / TFCP2, а LSF представляет собой онкоген в гепатоцеллюлярной карциноме. LSF и тимидилатсинтаза играют важную роль в пролиферации и прогрессировании рака печени и устойчивости к лекарствам.
Тимидилатсинтаза (TS) играет решающую роль на ранних стадиях ДНК биосинтез. Повреждение или делеция ДНК происходят ежедневно в результате как эндогенных факторов, так и факторов окружающей среды. К таким факторам окружающей среды относятся ультрафиолетовое повреждение и сигаретный дым, который содержит множество канцерогенов. Следовательно, синтез и внедрение здоровой ДНК жизненно важны для нормального функционирования организма и предотвращения раковой активности. Кроме того, важно подавление синтеза важных нуклеотидов, необходимых для роста клеток. По этой причине TS стал важной мишенью для лечения рака с помощью химиотерапии. Чувствительность TS к подавлению ингибиторов TS является ключевым фактором его успеха в лечении рака толстой кишки, поджелудочной железы, яичников, желудка и груди.
Использование ингибиторов TS стало основным направлением использования TS в качестве мишени для лекарств. Наиболее широко используемым ингибитором является 5-фторурацил (5-FU), который действует как антиметаболит, который необратимо ингибирует TS путем конкурентного связывания. Однако из-за низкого уровня 5-ФУ, обнаруженного у многих пациентов, было обнаружено, что в комбинации с лейковорином (LV) 5-ФУ имеет больший успех в подавлении механизмов прогрессирования опухоли и повышении иммунитета. активность системы.
Экспериментально было показано, что низкие уровни экспрессии TS приводят к лучшему ответу на 5-FU и более высокому уровню успешности и выживаемости пациентов с раком толстой кишки и печени. Однако дополнительные эксперименты просто заявили, что уровни TS могут быть связаны со стадией заболевания, пролиферацией клеток и дифференцировкой опухоли у пациентов с аденокарциномой легких, но с низкими уровнями не обязательно являются показателями высокого успеха. Уровни экспрессии TS мРНК могут быть полезны в прогнозировании злокачественного потенциала некоторых раковых клеток, таким образом улучшая цели лечения рака и обеспечивая более высокие показатели выживаемости среди онкологических больных [Хашимото].
Связь TS с клеточным циклом также способствует его использованию в лечении рака. Некоторые зависимые от клеточного цикла киназы и факторы транскрипции влияют на уровни TS в клеточном цикле, которые увеличивают его активность во время фазы S, но снижают его активность, в то время как клетки отсутствуют дольше размножается. Саморегулирующим образом TS контролирует не только свою собственную трансляцию, но и трансляцию других белков, таких как р53, который посредством мутации является корнем большого роста опухоли. Благодаря своей трансляции TS по-разному экспрессируется в раковых клетках и опухолях, что приводит к ранней гибели клеток.
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.
[[File: [[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]]
[[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]] | {{bSize}}} px | alt = Фторурацил (5-ФУ) Активность редактировать ]] Фторурацил (5-ФУ) Активность редактировать
| {{bSize}}} px | alt = Фторурацил (5-ФУ) Активность редактировать ]] Фторурацил (5-ФУ) Активность редактировать 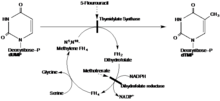 Это показывает общий путь, по которому тимидилатсинтаза и ее промежуточные соединения принимают
Это показывает общий путь, по которому тимидилатсинтаза и ее промежуточные соединения принимают В предложенном механизме TS образует ковалентную связь с субстратом dUMP посредством 1,4-присоединения с участием цистеинового нуклеофила. Тетрагидрофолат субстрата отдает метильную группу альфа-углероду, одновременно восстанавливая новый метил на dUMP с образованием dTMP.
 Это показывает сложные взаимодействия UMP в активном центре тимидилатсинтазы.
Это показывает сложные взаимодействия UMP в активном центре тимидилатсинтазы. Было доказано, что имин, образующийся в результате реакции с ТГФ и dUMP, является промежуточным звеном в реакции с dUMP через мутации в структуре TS, которые препятствуют завершению механизма. V316Am TS, мутант с делецией С-концевых валинов из обеих субъединиц, позволяет катализировать дегалогенирование BrdUMP, предшествующее механизму, описанному выше, и ковалентной связи с THF и dUMP. Мутантный TS неспособен выполнить C-концевое конформационное изменение, необходимое для разрыва ковалентных связей с образованием dTMP, таким образом показывая, что предложенный механизм верен. Структура была выведена с помощью рентгеновской кристаллографии V316Am TS, чтобы проиллюстрировать полную гомодимерную структуру TS (рис. 1). Кроме того, он показал возможные взаимодействия 175Arg и 174Arg между димерами. Считается, что эти аргинины стабилизируют структуры UMP в активных центрах, создавая водородные связи с фосфатной группой (рис. 2). [Страуд и Файнер-Мур] 5-ФУ является ингибитором TS. При попадании в клетку 5-фторурацил (5-FU) внутриклеточно превращается во множество активных метаболитов. Одним из таких метаболитов является FdUMP, который отличается от dUMP фтором вместо водорода на альфа-углероде. FdUMP способен ингибировать TS путем связывания с сайтом связывания нуклеотидов dUMP. Это конкурентное связывание подавляет нормальную функцию синтеза dTMP из dUMP [Longley]. Таким образом, dUMP не может пройти реакцию элиминирования и завершить отложение метила из ТГФ.
 Тимидилатсинтаза как гомодимер
Тимидилатсинтаза как гомодимер Фиг.1. На этом рисунке изображен гомодимер, которым является TS. Как вы можете видеть, оранжевая и бирюзовая основы никогда не соединяются и не переплетаются, но между димерами существуют взаимодействия боковых цепей. На оранжевом белке вы можете визуально обнаружить две длинные боковые цепи, которые входят в белок бирюзового цвета (они расположены внутри желтого круга). Остальные бежевые части представляют собой боковые цепи, которые взаимодействуют внутри активного сайта. Чуть ниже желтого круга вы можете увидеть тот же образец боковых цепей и конфигурации.
 Активный сайт тимидилатсинтазы
Активный сайт тимидилатсинтазы Рис. 2. На этом рисунке показаны возможные взаимодействия водородной связи между аргининами и UMP в активном центре тимидилатсинтазы. Это видно по слабым линиям между синими и красными наконечниками. Эти аргинины используются для удержания положения молекулы UMP, чтобы взаимодействие могло происходить правильно. Два аргинина в правом верхнем углу, которые расположены рядом друг с другом на позвоночнике, на самом деле происходят из другого белка этого димерного фермента. Это взаимодействие является одной из многих межмолекулярных сил, которые удерживают вместе эти две третичные структуры. Желтая полоса в верхней средней области показывает серную связь, которая образуется между боковой цепью цистеина и UMP. Это ковалентно удерживает UMP в активном сайте до тех пор, пока он не прореагирует с образованием TMP.