 Еноляционные резонансные структуры, схематическое изображение форм (см. Текст о молекулярных орбиталях ); слева карбанионная форма, справа енолят; Ex. это 2-бутанон, также менее стабилизировалась енольная.
Еноляционные резонансные структуры, схематическое изображение форм (см. Текст о молекулярных орбиталях ); слева карбанионная форма, справа енолят; Ex. это 2-бутанон, также менее стабилизировалась енольная.  Таутомеризация кетонов, кетоформа слева, енол справа. Ex. представляет собой 2,4-пентандион, енол, стабилизированный водородной связью (---).
Таутомеризация кетонов, кетоформа слева, енол справа. Ex. представляет собой 2,4-пентандион, енол, стабилизированный водородной связью (---). Енолы или, более формально, алкенолы, представляют собой тип реакционноспособной структуры или промежуточного продукта в органической химии, который представлен как алкен ( олефин ) с гидроксильной группой, присоединенной к одному концу двойной связи алкена. Термины енольные и alkenol являются чемоданами, вытекающими из «-» / «алкена» и «-ол» суффикса, указывающий гидроксильной группу из спиртов, сбросив терминал «-e» первого член. Образование енолов часто включает удаление водорода, соседнего ( α -) с карбонильной группой, то есть депротонирование, его удаление в виде протона, H +. Когда этот протон не возвращается в конце пошагового процесса, результатом является анион, называемый енолятом (см. Изображения справа). Показанные енолятные структуры схематичны; более современное представление рассматривает молекулярные орбитали, которые образуются и заняты электронами в еноляте. Точно так же образование енола часто сопровождается «захватом» или маскированием гидроксигруппы в виде простого эфира, такого как простой силиленольный эфир.
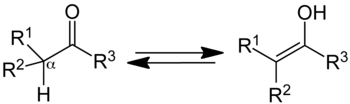 Кето-енольная таутомерия. Кето-форма (слева); форма енола (справа).
Кето-енольная таутомерия. Кето-форма (слева); форма енола (справа). В органической химии, кето-енольная таутомерия относится к химическому равновесию между кето формой (в кетоне или альдегид ) и энолом (An спирта ). Кето и енольные формы называются таутомерами друг друга. Взаимопревращение двух форм включает движение альфа-атома водорода и реорганизацию связывающих электронов ; следовательно, изомерия квалифицируется как таутомерия.
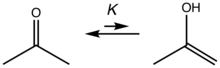 Кето-енольное равновесие для ацетона.
Кето-енольное равновесие для ацетона. | карбонил | энол | К енолизация |
|---|---|---|
| CH 3 CHO | CH 2 = CHOH | 5,8 х 10-7 |
| СН 3 С (О) СН 3 | СН 3 С (ОН) = СН 2 | 5,12 х 10-7 |
| CH 3 CO 2 CH 3 | СН 2 = СН (ОН) ОСН 3 | 4х10 -20 |
| С 6 Н 5 С (О) СН 3 | С 6 Н 5 С (ОН) = СН 2 | 1 х 10-8 |
| СН 3 С (О) СН 2 С (О) СН 3 | СН 3 С (О) СН = С (ОН) СН 3 | 0,27 |
Органические сложные эфиры, кетоны и альдегиды с α-водородом (связь CH, смежная с карбонильной группой ) часто образуют енолы. Реакция включает миграцию протона от углерода к кислороду:
В случае кетонов преобразование называется кето-енольной таутомерией, хотя это название часто применяется ко всем таким таутомеризациям. Обычно константа равновесия настолько мала, что енол не может быть обнаружен спектроскопически.
В некоторых соединениях с двумя (или более) карбонилами енольная форма становится доминирующей. Поведение 2,4-пентандиона иллюстрирует этот эффект:

Енолы представляют собой производные винилового спирта с связностью C = C-OH. Депротонирование органических карбонилов дает енолят-анион, который является сильным нуклеофилом. Классический пример предпочтения кето-формы можно увидеть в равновесии между виниловым спиртом и ацетальдегидом (K = [енол] / [кето] ≈ 3 × 10 -7). В 1,3-дикетонах, таких как ацетилацетон (2,4-пентандион), предпочтение отдается енольной форме.
Катализируемое кислотой превращение енола в кетоформу происходит за счет переноса протона от O к углероду. Процесс не происходит внутримолекулярно, но требует участия растворителя или других медиаторов.
Если R 1 и R 2 (обратите внимание на уравнение вверху страницы) являются разными заместителями, то при преобразовании енола в свою кетоформу в альфа-положении образуется новый стереоцентр. В зависимости от природы трех R-групп получающиеся продукты в этой ситуации будут диастереомерами или энантиомерами.
Эндиолы представляют собой алкены с гидроксильной группой на каждом атоме углерода двойной связи C = C. Обычно такие соединения являются нежелательными компонентами в равновесии с ацилоинами. Одним из особых случаев является катехол, в котором субъединица C = C является частью ароматического кольца. Однако в некоторых других случаях ендиолы стабилизируются фланкированием карбонильных групп. Эти стабилизированные ендиолы называются редуктонами. Такие виды важны в гликохимии, например, в преобразовании Лобри де Брюн-ван Экенштейна.
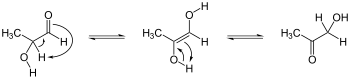 Кето-ендиоловые таутомеризации. Энедиол в центре; изомеры ацилоина слева и справа. Ex. представляет собой гидроксиацетон, показанный справа.
Кето-ендиоловые таутомеризации. Энедиол в центре; изомеры ацилоина слева и справа. Ex. представляет собой гидроксиацетон, показанный справа.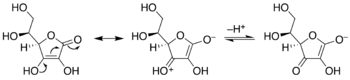 Превращение аскорбиновой кислоты (витамина С) в енолят. Эндиол слева, енолят справа, демонстрируя движение электронных пар, приводящее к депротонированию стабильного исходного эндиола. Отдельная, более сложная химическая система, проявляющая характеристики винилогии.
Превращение аскорбиновой кислоты (витамина С) в енолят. Эндиол слева, енолят справа, демонстрируя движение электронных пар, приводящее к депротонированию стабильного исходного эндиола. Отдельная, более сложная химическая система, проявляющая характеристики винилогии. Фенолы представляют собой разновидность енола. Для некоторых фенолов и родственных соединений важную роль играет кето-таутомер. Например, во многих реакциях резорцина участвует кето-таутомер. Нафталин-1,4-диол существует в наблюдаемом равновесии с дикетонтетрагидронафталин-1,4-дионом.
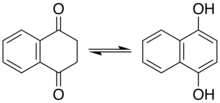
Кето-енольная таутомерия важна в нескольких областях биохимии.
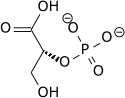
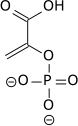
Высокий потенциал переноса фосфата фосфоенолпирувата является результатом того факта, что фосфорилированное соединение «улавливается» в менее термодинамически благоприятной енольной форме, тогда как после дефосфорилирования оно может принимать кето-форму.
Фермент енолаз катализирует дегидратацию 2-фосфоглицериновой кислоты до енольного эфира фосфорной кислоты. Метаболизм PEP до пировиноградной кислоты с помощью пируваткиназы (ПК) генерирует аденозинтрифосфат (АТФ) через субстрат уровня фосфорилирования.
 |  |  | ||||
| H 2 O | ADP | АТФ | ||||
 |  | |||||
| H 2 O | ||||||
Конец двойной связи в енолах нуклеофильный. Его реакции с электрофильными органическими соединениями лежат в основе огромного значения промежуточных продуктов на основе енолов в широком спектре важных жизненных процессов (например, в биохимии в качестве промежуточных продуктов в реакциях, катализируемых ферментами ), а также занимают центральное место в современной синтетической органической химии (например,, в приложениях альдольных и родственных реакций).
Депротонирование енолизируемых кетонов, альдегидов и сложных эфиров дает еноляты. В случае сильных оснований депротонирование носит количественный характер. Обычно еноляты получают с использованием диизопропиламида лития (LDA). Часто, как в обычных конденсациях Клайзена, реакциях Манниха и альдольных конденсациях, еноляты образуются в низких концентрациях с алкоксидными основаниями. В таких условиях они существуют в низких концентрациях, но все же вступают в реакции с электрофилами. Многие факторы влияют на поведение енолятов, особенно растворитель, добавки (например, диамины) и противокатион (Li + против Na + и т. Д.). Для несимметричных кетонов существуют методы контроля региохимии депротонирования.
Енолаты также могут улавливаться ацилированием и силилированием, которые происходят по кислороду. Силиловые эфиры енола являются обычными реагентами в органическом синтезе, что проиллюстрировано альдольной реакцией Мукаямы :

Винилацетат - это сложный эфир енола, который производится в промышленных масштабах. Еноляты лития имеют агрегированные структуры, аналогичные другим алкоксидам лития.
Еноляты электронно связаны с аллильными анионами. Анионный заряд делокализован по кислороду и двум центрам углерода.
