 | |
 | |
| Имена | |
|---|---|
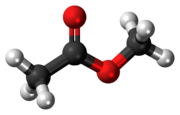
| Предпочтительное название IUPAC Метилацетат | |
| Систематическое название ИЮПАК Метил этаноат | |
| Другие названия Метиловый эфир уксусной кислоты | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.001.078 |
| КЕГГ | |
| PubChem CID | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | С 3 Н 6 О 2 |
| Молярная масса | 74,079 г моль -1 |
| Появление | Бесцветная жидкость |
| Запах | Ароматный, фруктовый |
| Плотность | 0,932 г см −3 |
| Температура плавления | -98 ° С (-144 ° F, 175 К) |
| Точка кипения | 56,9 ° С (134,4 ° F, 330,0 К) |
| Растворимость в воде | ~ 25% (20 ° С) |
| Давление газа | 173 мм рт. Ст. (20 ° С) |
| Магнитная восприимчивость (χ) | -42,60 10 −6 см 3 / моль |
| Показатель преломления ( n D) | 1,361 |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| NFPA 704 (огненный алмаз) |  2 3 2 3 |
| точка возгорания | −10 ° С; 14 ° F; 263 К |
| Пределы взрываемости | 3,1% -16% |
| Смертельная доза или концентрация (LD, LC): | |
| LD 50 ( средняя доза ) | 3700 мг / кг (перорально, кролик) |
| LC Lo ( самый низкий опубликованный ) | 11039 ppm (мышь, 4 часа) 21753 ppm (кошка, 1 час) 32000 ppm (крыса, 4 часа) |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 200 частей на миллион (610 мг / м 3) |
| REL (рекомендуется) | TWA 200 частей на миллион (610 мг / м 3) ST 250 частей на миллион (760 мг / м 3) |
| IDLH (Непосредственная опасность) | 3100 частей на миллион |
| Родственные соединения | |
| Связанные эфиры | Метилформиат Этилацетат Этилформиат Метилфторацетат |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Метилацетат, также известный как MeOAc, метиловый эфир уксусной кислоты или метилэтаноат, представляет собой сложный эфир карбоксилата с формулой CH 3 COOCH 3. Это легковоспламеняющаяся жидкость с характерным приятным запахом, напоминающим некоторые клеи и жидкости для снятия лака. Метилацетат иногда используется в качестве растворителя, поскольку он является слабополярным и липофильным, но его близкий родственник этилацетат является более распространенным растворителем, менее токсичным и менее растворимым в воде. Метилацетат имеет растворимость в воде 25% при комнатной температуре. При повышенной температуре его растворимость в воде намного выше. Метилацетат нестабилен в присутствии сильных водных оснований или водных кислот. Метилацетат не считается ЛОС в США.
Метилацетат получают промышленно с помощью карбонилирования из метанола в качестве побочного продукта при производстве уксусной кислоты. Метилацетат также образуется при этерификации уксусной кислоты метанолом в присутствии сильных кислот, таких как серная кислота ; Этот производственный процесс известен тем, что Eastman Kodak интенсивно использует реактивную дистилляцию.
В присутствии сильных оснований, таких как гидроксид натрия, или сильных кислот, таких как соляная кислота или серная кислота, он гидролизуется обратно в метанол и уксусную кислоту, особенно при повышенной температуре. Превращение метилацетата обратно в его компоненты кислотой является реакцией первого порядка по отношению к сложному эфиру. Реакция метилацетата и основания, например гидроксида натрия, является реакцией второго порядка по отношению к обоим реагентам.
Метилацетат - это основание Льюиса, которое образует аддукты 1: 1 с различными кислотами Льюиса. Он классифицируется как жесткая база и является базой в модели ECW с E B = 1,63 и C B = 0,95.
В основном метилацетат используется в качестве летучего малотоксичного растворителя в клеях, красках и жидкостях для снятия лака.
Уксусный ангидрид получают карбонилированием метилацетата в процессе, вдохновленном синтезом уксусной кислоты Monsanto.