| Вирус гриппа A | |
|---|---|
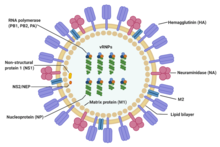 | |
| Структура вируса гриппа A | |
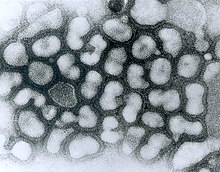 | |
| TEM микрофотография вирусы гриппа A | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Orthornavirae |
| Тип: | Negarnaviricota |
| Класс : | Insthoviricetes |
| Порядок: | Articulavirales |
| Семейство: | Orthomyxoviridae |
| Род: | Alphainfluenzavirus |
| Виды: | Вирус гриппа A |
| Подтипы | |
См. Текст | |
Вирус гриппа A вызывает грипп у птиц и некоторых млекопитающих и является единственным видом из рода Alphainfluenzavirus семейства вирусов Orthomyxoviridae. Штаммы всех подтипов вируса гриппа A были изолированы от диких птиц, хотя заболевание встречается редко. Некоторые изоляты вируса гриппа A вызывают тяжелые заболевания как у домашней птицы, так и, в редких случаях, у человека. Иногда вирусы передаются от диких водных птиц домашней птице, и это может вызвать вспышку или вызвать человеческий грипп пандемии.
Вирусы гриппа A негативного смысла, одноцепочечные, сегментированные РНК-вирусы. Несколько подтипов помечены в соответствии с номером H (для типа гемагглютинина ) и номером N (для типа нейраминидазы ). Существует 18 различных известных антигенов H (от H1 до H18) и 11 различных известных антигенов N (от N1 до N11). H17N10 был выделен от летучих мышей в 2012 году. H18N11 был обнаружен у перуанских летучих мышей в 2013 году.
Каждый подтип вируса мутировал в различные штаммы с разными патогенные профили; некоторые из них являются патогенными для одного вида, но не являются патогенными для других, некоторые - для нескольких видов.
Была разработана фильтрованная и очищенная вакцина против гриппа А для людей, и многие страны накопили ее для быстрого введения населению в случае птичьего гриппа пандемии. Птичий грипп иногда называют птичьим гриппом, а в просторечии - птичьим гриппом. В 2011 году исследователи сообщили об открытии антитела, эффективного против всех типов вируса гриппа А.
 Схема номенклатуры гриппа
Схема номенклатуры гриппа Вирусы гриппа типа A - это РНК-вирусы, разделенные на подтипы по типу двух белки на поверхности вирусной оболочки:
Гемагглютинин - это центральное значение для распознавания вируса и связывания с клетками-мишенями, а также t o затем он заражает клетку своей РНК. С другой стороны, нейраминидаза имеет решающее значение для последующего высвобождения дочерних вирусных частиц, созданных внутри инфицированной клетки, чтобы они могли распространяться на другие клетки.
Различные вирусы гриппа кодируют разные белки гемагглютинина и нейраминидазы. Например, вирус H5N1 обозначает подтип гриппа A, который имеет белок гемагглютинин (H) типа 5 и белок нейраминидазы (N) типа 1. Существует 18 известных типов гемагглютинина и 11 известных типов нейраминидазы, поэтому теоретически возможны 198 различных комбинаций этих белков.
Некоторые варианты идентифицированы и названы в соответствии с изолятом, на который они похожи, таким образом, предполагается делиться родословной (пример гриппа Фуцзянь похожего на вирус); в соответствии с их типичным хозяином (пример вирус человеческого гриппа ); по подтипу (пример H3N2); и по их смертоносности (например, LP, низкопатогенный). Таким образом, грипп, вызванный вирусом, подобным изоляту A / Fujian / 411/2002 (H3N2), называется гриппом Фуцзянь, человеческим гриппом и гриппом H3N2.
Варианты иногда называют в зависимости от вида (хозяина), для которого штамм является эндемичным или к которому он адаптирован. Основными вариантами, названными с использованием этого соглашения, являются:
Варианты также иногда называют в соответствии с их летальностью для домашней птицы, особенно куры:
Большинство известных штаммов - это вымершие штаммы. Например, подтип ежегодного гриппа H3N2 больше не содержит штамм, вызвавший Гонконгский грипп.
Ежегодный грипп (также называемый «сезонным гриппом» или «человеческим гриппом») Соединенные штаты. «ежегодно уносит около 36 000 смертей и более 200 000 госпитализаций. В дополнение к человеческим жертвам, грипп ежегодно вызывает в США более 10 миллиардов долларов». В глобальном масштабе количество случаев смерти от вируса гриппа оценивается в 290 000–645 000 смертей ежегодно, что превышает предыдущие оценки.
Ежегодно обновляемая трехвалентная вакцина против гриппа состоит из гемагглютинина (HA) поверхностные гликопротеиновые компоненты вирусов гриппа H3N2, H1N1 и B.
Измеренная устойчивость к стандартным противовирусным препаратам амантадин и римантадин в H3N2 увеличился с 1% в 1994 г. до 12% в 2003 г. до 91% в 2005 г.
«Современные вирусы гриппа H3N2 человека в настоящее время эндемичны у свиней в южном Китае и может повторно сортировать с птичьим вирусом H5N1 в этом промежуточном хозяине ».
FI6, антитело, нацеленное на белок гемагглютинин, было обнаружено в 2011 году. FI6 - единственное известное антитело, эффективное против всех 16 подтипов вируса гриппа А.
 Электронная микрофотография ( ТЕА) реконструированной пандемической инф вирус люензы. Нижняя структура представляет собой обломки мембран клеток, используемых для амплификации вируса. На фото изображены «эллиптические» частицы, представляющие мельчайшие частицы, производимые вирусом гриппа. Методы очистки часто деформируют частицы без надлежащих протоколов фиксации, что приводит к их «сферическому» виду. Нитевидные частицы или частицы среднего размера просто проходят вдоль длинной оси на противоположной стороне сегментов генома.
Электронная микрофотография ( ТЕА) реконструированной пандемической инф вирус люензы. Нижняя структура представляет собой обломки мембран клеток, используемых для амплификации вируса. На фото изображены «эллиптические» частицы, представляющие мельчайшие частицы, производимые вирусом гриппа. Методы очистки часто деформируют частицы без надлежащих протоколов фиксации, что приводит к их «сферическому» виду. Нитевидные частицы или частицы среднего размера просто проходят вдоль длинной оси на противоположной стороне сегментов генома. Вирусы гриппа типа A очень похожи по структуре на вирусы гриппа типов B, C и D. Вирусная частица (также называемая вирион) составляет 80–120 нанометров в диаметре, так что самые маленькие вирионы принимают эллиптическую форму. Длина каждой частицы значительно различается из-за того, что грипп является плеоморфным и может превышать многие десятки микрометров, образуя нитчатые вирионы. Путаница в отношении природы плеоморфии вируса гриппа проистекает из наблюдения, что лабораторно адаптированные штаммы обычно теряют способность образовывать филаменты, и что эти лабораторно адаптированные штаммы были первыми, которые были визуализированы с помощью электронной микроскопии. Несмотря на эти различные формы, вирионы всех вирусов гриппа типа А похожи по составу. Все они состоят из вирусной оболочки, содержащей два основных типа белков, обернутых вокруг центрального ядра.
Два больших белка, обнаруженных снаружи вирусных частиц, - это гемагглютинин (HA) и нейраминидаза (NA). НА - это белок, который опосредует связывание вириона с клетками-мишенями и проникновение вирусного генома в клетку-мишень. NA участвует в высвобождении из множества непродуктивных участков прикрепления, присутствующих в слизи, а также в высвобождении вирионов потомства из инфицированных клеток. Эти белки обычно являются мишенями для противовирусных препаратов. Кроме того, они также являются белками-антигенами, с которыми могут связываться антитела хозяина и запускать иммунный ответ. Вирусы гриппа типа A подразделяются на подтипы в зависимости от типа этих двух белков на поверхности вирусной оболочки. Известно 16 подтипов HA и 9 подтипов NA, но у людей обычно встречаются только H 1, 2 и 3, а также N 1 и 2.
Центральное ядро вириона содержит вирусный геном и другие вирусные белки, которые упаковывают и защищают генетический материал. В отличие от геномов большинства организмов (включая людей, животных, растения и бактерии), которые состоят из двухцепочечной ДНК, многие вирусные геномы состоят из другой однонитевой нуклеиновой кислоты, называемой РНК. Однако, что необычно для вируса, геном вируса гриппа типа А не представляет собой единого фрагмента РНК; вместо этого он состоит из сегментированных фрагментов РНК с отрицательным смыслом, каждый из которых содержит один или два гена, которые кодируют продукт гена (белок). Термин РНК с отрицательным смыслом просто означает, что геном РНК не может быть транслирован в белок напрямую; он должен быть сначала транскрибирован в РНК с положительным смыслом, прежде чем он может быть переведен в белковые продукты. Сегментированный характер генома позволяет обмениваться целыми генами между различными вирусными штаммами.
 Структура вируса гриппа A
Структура вируса гриппа A Полный геном вируса гриппа A имеет длину 13 588 оснований и содержится в восьми сегментах РНК, которые кодируют как минимум 10, но до 14 белков, в зависимости от штамма. Релевантность или присутствие альтернативных генных продуктов может варьироваться:
 Репликация вируса гриппа А. цикл
Репликация вируса гриппа А. цикл Сегменты РНК вирусного генома имеют комплементарные последовательности оснований на концевых концах, что позволяет им связываться друг с другом водородными связями. Транскрипция вирусного (-) смыслового генома (вРНК) может продолжаться только после того, как белок PB2 свяжется с РНК, кэпированной хозяином, что позволяет субъединице PA отщеплять несколько нуклеотидов после кэпа. Этот полученный от хозяина кэп и сопровождающие его нуклеотиды служат праймером для инициации вирусной транскрипции. Транскрипция продолжается вдоль вРНК до тех пор, пока не будет достигнут участок из нескольких оснований урацила, инициируя «заикание», в результате чего возникающая вирусная мРНК полиаденилируется, производя зрелый транскрипт для экспорта в ядро и трансляции механизмами хозяина.
Синтез РНК происходит в ядре клетки, а синтез белков - в цитоплазме. После того как вирусные белки собраны в вирионы, собранные вирионы покидают ядро и мигрируют к клеточной мембране. Мембрана клетки-хозяина имеет участки вирусных трансмембранных белков (HA, NA и M2) и нижележащий слой белка M1, который помогает собранным вирионам проходить через мембрану, высвобождая готовые вирусы в оболочке во внеклеточную жидкость.
Вирус гриппа может подвергаться реактивации множественности после инактивации УФ-излучением или ионизирующим излучением. Если какая-либо из восьми цепей РНК, составляющих геном, содержит повреждение, препятствующее репликации или экспрессии важного гена, вирус становится нежизнеспособным, когда он один заражает клетку (единичная инфекция). Однако, когда два или более поврежденных вируса заражают одну и ту же клетку (множественная инфекция), могут быть получены жизнеспособные потомки вирусов при условии, что каждый из восьми геномных сегментов присутствует по крайней мере в одной неповрежденной копии. То есть может произойти повторная активация множественности.
При инфицировании вирус гриппа вызывает ответную реакцию хозяина, включающую повышенное производство активных форм кислорода, и это может повредить геном вируса. Если в естественных условиях выживаемость вируса обычно уязвима для проблемы окислительного повреждения, то реактивация множественности, вероятно, является селективно выгодной как своего рода процесс репарации генома. Было высказано предположение, что реактивация множественности с участием сегментированных геномов РНК может быть похожей на самую раннюю развитую форму сексуального взаимодействия в мире РНК, которая, вероятно, предшествовала миру ДНК. (См. Также Гипотеза мира РНК.)
 Хронология пандемий гриппа и эпидемий, вызванных вирусом гриппа A
Хронология пандемий гриппа и эпидемий, вызванных вирусом гриппа A «Вирус гриппа человека» обычно относится к этим подтипам которые широко распространились среди людей. H1N1, H1N2 и H3N2 - единственные известные подтипы вируса гриппа A, циркулирующие в настоящее время среди людей.
Генетические факторы, позволяющие различать «вирусы гриппа человека» и «вирусы птичьего гриппа», включают:
Симптомы человеческого гриппа обычно включают лихорадку, кашель, боль в горле, мышечные боли, конъюнктивит и, в тяжелых случаях, проблемы с дыханием и пневмония, которая может быть фатальной. Тяжесть инфекции будет в значительной степени зависеть от состояния иммунной системы инфицированного человека и от того, подвергалась ли жертва воздействию штамма раньше и, следовательно, частично обладает иммунитетом. Последующие исследования влияния статинов на репликацию вируса гриппа показывают, что предварительная обработка клеток аторвастатином подавляет рост вируса в культуре.
Высокопатогенный птичий грипп H5N1 у человека протекает гораздо хуже, убивая 50% люди, которые его поймают. В одном случае мальчик с H5N1 испытал диарею, за которой быстро последовала кома без развития респираторных или гриппоподобных симптомов.
Подтипы вируса гриппа A, подтвержденные у людей, упорядочены число известных случаев смерти людей от пандемии составляет:
 Случаи заболевания людей и летальные исходы, вызванные различными подтипами вируса гриппа A H1N1 в настоящее время находится в пандемии ic в популяциях людей и свиней. Вариант H1N1 был ответственен за пандемию испанского гриппа, в результате которой примерно за год в 1918 и 1919 годах погибло от 50 до 100 миллионов человек во всем мире. Другой вариант был назван угрозой пандемии во время пандемии гриппа 2009 года. Споры возникли в октябре 2005 г., после того как в журнале Science был опубликован геном H1N1 из-за опасений, что эта информация может быть использована для биотерроризма.
Случаи заболевания людей и летальные исходы, вызванные различными подтипами вируса гриппа A H1N1 в настоящее время находится в пандемии ic в популяциях людей и свиней. Вариант H1N1 был ответственен за пандемию испанского гриппа, в результате которой примерно за год в 1918 и 1919 годах погибло от 50 до 100 миллионов человек во всем мире. Другой вариант был назван угрозой пандемии во время пандемии гриппа 2009 года. Споры возникли в октябре 2005 г., после того как в журнале Science был опубликован геном H1N1 из-за опасений, что эта информация может быть использована для биотерроризма.H5N1 представляет собой главную угрозу пандемии гриппа в мире.
 Генетическая эволюция вирусов гриппа человека и свиней, 1918–2009 гг.
Генетическая эволюция вирусов гриппа человека и свиней, 1918–2009 гг. Согласно Джеффри Таубенбергеру :
Исследователи из Национальных институтов of Health использовали данные Проекта секвенирования генома гриппа и пришли к выводу, что в течение исследуемого десятилетнего периода большую часть времени ген гемагглютинина в H3N2 не обнаруживал значительного избытка мутаций в антигенных областях, в то время как ан накапливается все большее разнообразие штаммов. Это привело к тому, что один из вариантов в конечном итоге достиг более высокой приспособленности, стал доминирующим и в течение короткого периода быстрой эволюции быстро охватил популяцию и устранил большинство других вариантов.
Вкратце Исследование, проведенное в 2006 году, показало, что ключевыми факторами являются случайные или случайные процессы. Эволюция антигена НА вируса гриппа А, по-видимому, характеризуется скорее прерывистыми, спорадическими скачками, чем постоянной скоростью изменения антигена. Используя филогенетический анализ 413 полных геномов вирусов гриппа А человека, собранных по всему штату Нью-Йорк, авторы Nelson et al. В 2006 году удалось показать, что генетическое разнообразие, а не дрейф антигенов, сформировало краткосрочную эволюцию гриппа А посредством случайной миграции и реассортировки. В эволюции этих вирусов преобладает случайный импорт генетически различных вирусных штаммов из других географических регионов, а не естественный отбор. В течение данного сезона адаптивная эволюция происходит нечасто и оказывает в целом слабый эффект, о чем свидетельствуют данные, собранные для 413 геномов. Филогенетический анализ показал, что различные штаммы были получены из недавно импортированного генетического материала, в отличие от изолятов, циркулировавших в Нью-Йорке в предыдущие сезоны. Следовательно, поток генов в эту популяцию и из нее, а не естественный отбор, был более важен в краткосрочной перспективе.
птицы действуют как естественные бессимптомные переносчики вирусов гриппа А. До нынешней эпизоотии H5N1 было продемонстрировано, что штаммы вируса гриппа A передаются от диких птиц только птицам, свиньям, лошадям, тюленям, китам и людям; и только между людьми и свиньями и между людьми и домашней птицей; а не другими путями, такими как от домашней птицы к лошади.
Дикие водные птицы являются естественными хозяевами для большого разнообразия вирусов гриппа А. Иногда вирусы передаются от этих птиц другим видам и затем могут вызывать разрушительные вспышки среди домашних птиц или вызывать пандемии гриппа человека.
Было показано, что H5N1 передается тиграм, леопардам и домашним кошкам, которые кормили сырых домашних птиц (цыплят) с вирусом. H3N8 Вирусы лошадей пересеклись и вызвали вспышки среди собак. Лабораторные мыши были успешно инфицированы различными генотипами птичьего гриппа.
Вирусы гриппа A распространяются в воздухе и навозе и дольше выживают в холодную погоду. Они также могут передаваться через зараженный корм, воду, оборудование и одежду; однако нет никаких доказательств того, что вирус может выжить в хорошо приготовленном мясе. Симптомы у животных различны, но вирулентные штаммы могут вызвать смерть в течение нескольких дней. Вирусы птичьего гриппа, которые Всемирная организация здравоохранения и другие тестируют для борьбы с болезнями домашних птиц, включают H5N1, H7N2, H1N7, H7N3, H13N6, H5N9, H11N6, H3N8, H9N2, H5N2, H4N8, H10N7, H2N2, H8N4, H14N5, H6N5 и H12N5.
| Год | Район | Затронутые | Подтип |
|---|---|---|---|
| 1959 | Шотландия | Курица | H5N1 |
| 1963 | Англия | Турция | H7N3 |
| 1966 | Онтарио (Канада) | Турция | H5N9 |
| 1976 | Виктория (Австралия) | Курица | H7N7 |
| 1979 | Германия | Курица | H7N7 |
| 1979 | Англия | Турция | H7N7 |
| 1983 | Пенсильвания (США) * | Цыпленок, индейка | H5N2 |
| 1983 | Ирландия | Турция | H5N8 |
| 1985 | Виктория (Австралия) | Курица | H7N7 |
| 1991 | Англия | Турция | H5N1 |
| 1992 | Виктория (Австралия) | Цыпленок | H7N3 |
| 1994 | Квинсленд (Австралия) | Цыпленок | H7N3 |
| 1994 | Мексика * | Цыпленок | H5N2 |
| 1994 | Пакистан * | Цыпленок | H7N3 |
| 1997 | Новый Южный Уэльс (Австралия) | Цыпленок | H7N4 |
| 1997 | Гонконг (Китай) * | Цыпленок | H5N1 |
| 1997 | Италия | Курица | H5N2 |
| 1999 | Италия * | Турция | H7N1 |
| 2002 | Гонконг (Китай) | Цыпленок | H5N1 |
| 2002 | Чили | Цыпленок | H7N3 |
| 2003 | Нидерланды * | Курица | H7N7 |
* Вспышки со значительным распространением на многочисленные фермы, приводящие к большим экономическим потерям. Большинство других вспышек были связаны с незначительным распространением или отсутствием распространения от первоначально зараженных ферм.
В период с декабря 1979 года по октябрь 1980 года в Новой Англии было зарегистрировано более 400 случаев смерти морских тюленей от острой пневмонии, вызванной вирусом гриппа A / Seal / Mass / 1/180 (H7N7).
Вирус гриппа A имеет следующие подтипы:
Высокопатогенный вирус птичьего гриппа входит в каждую десятку списка потенциальных агентов сельскохозяйственного биологического оружия.