 Димер дифенилкупрата лития из кристаллической структуры
Димер дифенилкупрата лития из кристаллической структуры 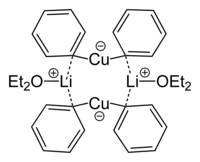 Скелетная формула димера дифенилкупрата лития.
Скелетная формула димера дифенилкупрата лития. Медноорганические соединения в металлоорганической химии содержат химические связи углерода с меди . Химия медьорганических соединений - это наука о медьорганических соединениях, описывающая их физические свойства, синтез и реакции. Они являются реагентами в органической химии.
Первое медноорганическое соединение, взрывчатый ацетилид меди (I) Cu2C2(Cu-C≡C-Cu), был синтезирован Рудольфом Кристианом Бёттгером в 1859 г., пропуская газ ацетилен через раствор хлорида меди (I) :
Медноорганические соединения разнообразны по структуре и реакционной способности, но медноорганические соединения в значительной степени ограничены в степень окисления s на медь (I), иногда обозначаемую как Cu. Как d-металлический центр, он связан с Ni (0), но из-за его более высокой степени окисления он участвует в меньшем количестве пи-обратных связей. Органические производные Cu (II) и Cu (III) упоминаются как промежуточные соединения, но редко выделяются или даже наблюдаются. С точки зрения геометрии, медь (I) имеет симметричную структуру в соответствии с ее сферической электронной оболочкой. Обычно принимается одна из трех координационных геометрий: линейная 2-координатная, тригональная 3-координатная и тетраэдрическая 4-координатная. Медноорганические соединения образуют комплексы с разнообразными мягкими лигандами, такими как алкилфосфины (R3P), тиоэфиры (R 2 S) и цианид ( CN).
Соли меди (I) давно известны тем, что связывают CO, хотя и слабо. Типичный комплекс - это полимер CuCl (CO). В отличие от классических карбонилов металлов, в этих соединениях пи-обратная связь не является сильной.
 Часть каркаса CuCl (CO). В этом координационном полимере центры Cu тетраэдрически связаны тройными мостиковыми хлоридными лигандами.
Часть каркаса CuCl (CO). В этом координационном полимере центры Cu тетраэдрически связаны тройными мостиковыми хлоридными лигандами. Алкены связываются с медью (I), хотя опять же, как правило, слабо. Связывание этилена с Cu в белках настолько важно в биологии растений, что этилен классифицируется как гормон растения. Его присутствие, обнаруживаемое с помощью Cu-белка, влияет на созревание и многие другие процессы.
Хотя медь не образует металлоцен, могут образовываться полусэндвич-комплексы. Одним из таких производных является (η-циклопентадиенилтриэтилфосфин) медь.
Галогениды меди реагируют с литийорганические реагенты с получением медноорганических соединений. Первым в этой области был Генри Гилман, который сообщил о метилмеди в 1936 году. Таким образом, фенилмедь получают реакцией фениллития с бромидом меди (I) в диэтиловый эфир. Реагенты Гриньяра могут использоваться вместо литийорганических соединений. Гилман также исследовал диалкилкупраты. Их получают путем объединения двух эквивалентов RLi с солями Cu (I). Альтернативно, эти купраты получают из олигомерных нейтральных медноорганических соединений путем обработки одним эквивалентом литийорганического реагента.
Соединения типа [CuR n ] реакционноспособны по отношению к кислороду и воде, образу оксид меди (I). Они также имеют тенденцию быть термически нестабильными, что может быть полезно в определенных реакциях сочетания. Несмотря на эти трудности или из-за них, медьорганические реагенты часто генерируются и потребляются in situ без попытки их изолировать. Они используются в органическом синтезе в качестве алкилирующих реагентов, потому что они проявляют большую устойчивость к функциональным группам, чем соответствующие реактивы Гриньяра и литийорганические реагенты. электроотрицательность меди намного выше, чем у ее ближайшего соседа в группе 12 элементов, цинка, что предполагает пониженную нуклеофильность для ее углеродные лиганды.
Соли меди реагируют с концевыми алкинами с образованием ацетилидов.
. Алкилгалогениды реагируют с медноорганическими соединениями с изменением конфигурации. С другой стороны, реакции медноорганического соединения с алкенилгалогенидами протекают с сохранением конфигурации субтрата.
Медноорганические соединения соединяются с арилгалогенидами:

Алкильные и арильные комплексы меди как в кристаллической форме, так и в виде агрегатов. Агрегация особенно очевидна для медноорганических соединений с нейтральным зарядом. фунтов, то есть виды с эмпирической формулой (RCu), которые принимают циклические структуры. Поскольку для каждого медного центра требуется по меньшей мере два лиганда, органическая группа представляет собой мостиковый лиганд . Этот эффект иллюстрируется структурой мезитилмеди, которая является пентамером. Циклическая структура также видна для CuCH 2 SiMe 3, первого медноорганического соединения 1: 1, подлежащего анализу с помощью рентгеновской кристаллографии (Lappert, 1972). Это соединение относительно стабильно, поскольку объемные триметилсилильные группы обеспечивают стерическую защиту. Это тетрамер, образующий 8-членное кольцо с чередующимися связями Cu-C. Кроме того, четыре атома меди образуют плоское кольцо Cu 4 на основе трехцентровых двухэлектронных связей. Длина связи меди составляет 242 пм по сравнению с 256 пм в объемной меди. В пентамеситилпентакоппере образуется 5-членное медное кольцо, подобное (2,4,6-триметилфенил) золоту, а пентафторфенилмедь представляет собой тетрамер.

Диметилкупрат лития представляет собой димер в диэтиловом эфире, образующий 8-членное кольцо с двумя атомами лития, связывающими две метильные группы. Точно так же дифенилкупрат лития образует димерный эфир, [{Li (OEt 2)} (CuPh 2)]2, в твердом состоянии.
Участие редко встречающейся в других отношениях степени окисления Cu (III) было продемонстрировано в добавлении конъюгата реагента Гилмана к енону : в эксперименте с так называемой быстрой инъекцией ЯМР при -100 ° C реагент Гилмана Me 2 CuLi (стабилизированный иодидом лития ) был введен до циклогексенон (1), позволяющий обнаруживать комплекс медь-алкен pi 2. При последующем добавлении триметилсилилцианида образуются частицы Cu (III) 3 (неопределенно стабильные при этой температуре) и при повышении температуры до -80 ° C продукт присоединения конъюгата 4 . Согласно сопутствующим экспериментам in silico промежуточное соединение Cu (III) имеет плоскую квадратную молекулярную геометрию с циано группой в цис-ориентации по отношению к циклогексенил метиновой группе и антипараллельно метиновому протону. С другими лигандами, кроме цианогруппы, это исследование предсказывает стабильные при комнатной температуре соединения Cu (III).
![Промежуточное соединение Cu (III), характеризуемое ЯМР. [11]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/ed/CopperIII_intermediate_by_RI_NMR.png/300px-CopperIII_intermediate_by_RI_NMR.png)
До разработки катализируемых палладием катализируемых реакций перекрестного сочетания, меди был предпочтительным катализатором в течение почти столетия. Палладий обеспечивает более быструю и селективную реакцию. Однако в последние годы медь снова стала синтетически полезным металлом из-за ее более низкой стоимости и потому, что это экологически чистый металл.
Реакции R 2 CuLi с алкилгалогениды R'-X образуют продукт сочетания:
механизм реакции включает окислительное присоединение (OA) алкилгалогенида до Cu (I) с образованием планарного промежуточного соединения Cu (III) с последующим восстановительным элиминированием (RE). Нуклеофильная атака является определяющим этапом. При замещении иодида предлагается одноэлектронный механизм переноса (см. Рисунок).
![{\displaystyle [{\ce {R}}{-}{\color {Blue}{\ce {Cu}}}{\ce {-R}}]^{-}{\ce {Li+}}\ {\xrightarrow {\color {Red}{\ce {R'-X}}}}\ \left[{\ce {R}}{-}{\overset {{\displaystyle \color {Red}{\ce {R}}'} \atop |}{\underset {| \atop {\displaystyle \color {Red}{\ce {X}}}}{\color {Blue}{\ce {Cu}}}}}{\ce {-R}}\right]^{-}{\ce {Li+}}{\ce {->R}} {-} {\ color {Синий} {\ ce {Cu}}} + {\ ce {R}} {-} {\ color {Red} {\ ce {R '}}} + {\ ce {Li}} {-} {\ цвет {Красный} {\ ce {X}}}}]( https://wikimedia.org/api/rest_v1/media/math/render/svg/ 9d7db6776d965a97de00837677a94c6fd3d1df2a )
Многие электрофилы участвуют в этой реакции. Примерный порядок реакционной способности, начиная с наиболее реакционноспособного, следующий: хлорангидриды >альдегиды >тозилаты ~ эпоксиды >иодиды >бромиды >хлориды >кетоны >сложные эфиры >нитрилы >>алкены
Обычно механизм OA-RE аналогичен катализируемым палладием реакциям кросс-сочетания. Одно различие между медью и палладием заключается в том, что медь может подвергаться o процессы одноэлектронного переноса.
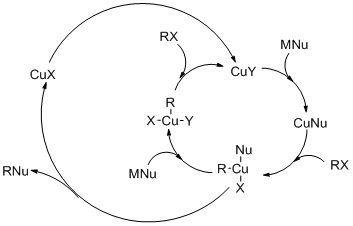
Окислительное связывание - это связывание ацетилидов меди с сопряженными алкинами в взаимодействии Глейзера (например, в синтез циклооктадеканонаена ) или до арилгалогенидов в взаимодействии Кастро-Стефенса.
Восстановительное связывание - это реакция связывания арилгалогенидов со стехиометрическим эквивалентом металлической меди, которая происходит в реакции Ульмана. В примере современной реакции перекрестного сочетания, называемой декарбоксилатным сочетанием, каталитическое количество Cu (I) замещает карбоксильную группу, образующую арилмедь (ArCu) промежуточный. Одновременно палладиевый катализатор превращает арилбромид в палладиевый промежуточный продукт (Ar'PdBr), и при трансметаллировании биарил образуется из ArPdAr '.

Нейтральное окислительно-восстановительное сочетание представляет собой сочетание концевых алкинов с галогеном. -алкины с солью меди (I) в сочетании Кадио-Ходкевича. Также возможно термическое соединение двух медноорганических соединений.
Карбокупрация - это нуклеофильное добавление медьорганических реагентов (R-Cu) к ацетилену или концевым алкинам, в результате чего в соединении алкенилмеди (RC = C-Cu). Это частный случай карбометализации, также называемый нормантной реакцией .
. Рисунок: Каталитический цикл карбокупрации для синтеза альдола, продукты типа Бейлиса-Хиллмана

.
Гидриды меди - это специализированные реагенты, которые иногда используются в качестве восстановителя. Наиболее известный гидрид меди называется реагент Страйкера, кластерное соединение с формулой [(PPh 3) CuH] 6. Он восстанавливает алкеновые α, β-ненасыщенные карбонильные соединения.
Реакция Бухвальда представляет собой асимметричное восстановление активированных алкенов, катализируемое медью. Реагент генерируется in situ из комплекса меди (I) NHC. Эквиваленты гидридов обеспечиваются силаном.

Синтезом изостер Z-фторалкен-дипептида. Другие попытки сделать эту реакцию более селективной, включают использование окислительно-восстановительных условий для реакции. Фторид действует как уходящая группа и повышает региоселективность превращения Z-фторалкена.
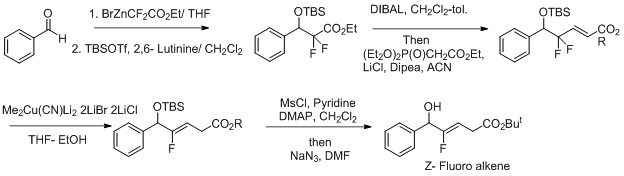
Обычно реакция алкилирования медьорганических реагентов протекает через гамма-алкилирование. Цис-гамма-атака лучше проявляется в циклогексилкарбамате из-за стерических факторов. Сообщается, что реакция протекает в эфирных растворителях. Доказано, что этот метод очень эффективен для окислительного сочетания аминов и алкила, включая трет-бутил, и арилгалогенидов.
функционализации вицинала с использованием последовательности реакции карбокупрации-альдола Мукаямы
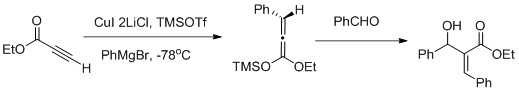
Мюллер и соавторы сообщили о вицинальной функционализации α, β-ацетиленовых эфиров с использованием последовательности реакций карбокупрация / альдол Мукаямы (как показано на фиг. Выше). Карбокупрация способствует образованию зальдола.