Окислительное добавление и восстановительное отщепление - два важных и связанных класса реакций в металлоорганической химии. Окислительное добавление - это процесс, который увеличивает степень окисления и координационное число металлического центра. Окислительное добавление часто является стадией каталитических циклов в сочетании с его обратной реакцией, восстановительным отщеплением.
Для переходных металлов, окислительные реакции приводят к уменьшению д п к конфигурации с меньшим количеством электронов, часто 2e меньше. Окислительная добавка предпочтительна для металлов, которые (i) являются основными и / или (ii) легко окисляются. Металлы с относительно низкой степенью окисления часто удовлетворяют одному из этих требований, но даже металлы с высокой степенью окисления подвергаются окислительному присоединению, как показано окислением Pt (II) хлором:
В классической металлоорганической химии формальная степень окисления металла и количество электронов в комплексе увеличиваются на два. Также возможны одноэлектронные изменения, и на самом деле некоторые реакции окислительного присоединения протекают через серию изменений 1e. Хотя окислительные добавки могут происходить при внедрении металла во многие различные субстраты, окислительные добавки чаще всего наблюдаются со связями H – H, H – X и C – X, поскольку эти субстраты наиболее актуальны для коммерческого применения.
Окислительное добавление требует, чтобы комплекс металла имел свободный координационный центр. По этой причине окислительные добавки обычны для четырех- и пятикоординированных комплексов.
Восстановительное удаление является обратным окислительному добавлению. Восстановительное устранение благоприятно, когда вновь образованная связь X – Y прочная. Для того, чтобы произошло восстановительное отщепление, две группы (X и Y) должны быть смежными друг с другом на координационной сфере металла. Восстановительное отщепление является ключевым этапом высвобождения продукта в нескольких реакциях, которые образуют связи C – H и C – C.
Окислительные добавки происходят по многим путям, которые зависят от металлического центра и субстратов.
Окислительные добавки неполярных субстратов, таких как водород и углеводороды, по-видимому, происходят согласованными путями. В таких субстратах отсутствуют π-связи, следовательно, активируется трехцентровый σ-комплекс с последующим разрывом внутримолекулярной лигандной связи лиганда (вероятно, путем передачи электронной пары на сигма-орбиталь межлигандной связи) с образованием окисленного комплекса. Полученные лиганды будут взаимно цис-образными, хотя может происходить последующая изомеризация.
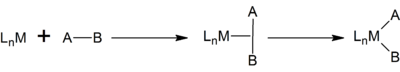
Этот механизм применяется к добавлению гомоядерных двухатомных молекул, таких как H 2. Многие реакции активации C – H также следуют согласованному механизму через образование агостического комплекса M– (C – H).
Типичным примером является реакция водорода с комплексом Васьки, транс- IrCl (CO) [P (C 6 H 5) 3 ] 2. В этом превращении иридий меняет свою формальную степень окисления с +1 на +3. Продукт формально связан с тремя анионами: одним хлоридным и двумя гидридными лигандами. Как показано ниже, исходный металлический комплекс имеет 16 валентных электронов и координационное число четыре, тогда как продукт представляет собой шестикоординированный 18-электронный комплекс.

Образование тригонально-бипирамидного дигидроген-интермедиата сопровождается разрывом связи H – H из-за обратной передачи электронов в H – H σ * -орбиталь, то есть в сигма-комплекс. Эта система также находится в химическом равновесии с обратной реакцией, протекающей путем удаления газообразного водорода с одновременным восстановлением металлического центра.
Обратное донорство электронов на H – H σ * -орбиталь для разрыва связи H – H заставляет богатые электронами металлы поддерживать эту реакцию. Согласованный механизм производит цис- дигидрид, в то время как стереохимия других путей окислительного присоединения обычно не дает цис- аддуктов.
Некоторые окислительные добавки протекают аналогично хорошо известным реакциям бимолекулярного нуклеофильного замещения в органической химии. Нуклеофильная атака металлическим центром на менее электроотрицательный атом в субстрате приводит к разрыву связи R – X с образованием частиц [M – R] +. Эта стадия сопровождается быстрой координацией аниона с катионным металлическим центром. Например, реакция плоско-квадратного комплекса с йодистым метилом :
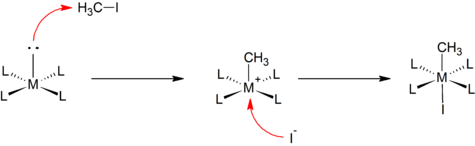
Этот механизм часто предполагается при добавлении полярных и электрофильных субстратов, таких как алкилгалогениды и галогены.
Ионный механизм окислительного присоединения аналогичен типу S N 2 в том, что он включает ступенчатое добавление двух отдельных фрагментов лиганда. Ключевое отличие состоит в том, что ионные механизмы включают субстраты, которые диссоциируют в растворе до любых взаимодействий с металлическим центром. Примером ионного окислительного присоединения является добавление соляной кислоты.
Помимо прохождения реакций типа S N 2, алкилгалогениды и подобные субстраты могут присоединяться к металлическому центру посредством радикального механизма, хотя некоторые детали остаются спорными. Однако известны реакции, которые, как принято считать, протекают по радикальному механизму. Один пример был предложен Леднором и сотрудниками.
Окислительное добавление и восстановительное отщепление используются во многих каталитических процессах как при гомогенном катализе (т. Е. В растворе), таких как процесс Monsanto, так и гидрирование алкена с использованием катализатора Уилкинсона. Часто предполагается, что реакции, подобные окислительному присоединению, также участвуют в механизмах гетерогенного катализа, например, гидрирование, катализируемое металлической платиной. Однако металлы характеризуются полосовой структурой, поэтому степень окисления не имеет значения. Окислительное добавление также необходимо для того, чтобы произошло нуклеофильное присоединение алкильной группы. Окислительный вставки также является важным шагом во многих кросс-сочетания реакций, таких как реакции сочетания Сузуки, Негиши муфты, и муфты Соногашира.