ДНК-гликозилазы представляют собой семейство ферментов, участвующих в эксцизионная репарация основания, классифицируется под номером ЕС EC 3.2.2. эксцизионная репарация оснований - это механизм, с помощью которого поврежденные основания в ДНК удаляются и заменяются. ДНК-гликозилазы катализируют первую стадию этого процесса. Они удаляют поврежденное азотистое основание, оставляя сахарно-фосфатный остов нетронутым, создавая апуриновый / апиримидиновый сайт, обычно называемый AP-сайтом. Это достигается путем переворота поврежденного основания из двойной спирали с последующим разрывом N- гликозидной связи..
Гликозилазы были впервые обнаружены у бактерий, и с тех пор были обнаружены во всех царствах жизнь. Помимо своей роли в эксцизионной репарации оснований, ферменты ДНК-гликозилазы участвуют в репрессии сайленсинга генов у A. thaliana, N. tabacum и других растений за счет активного деметилирования. Остатки 5-метилцитозина вырезаются и заменяются неметилированными цитозинами, обеспечивая доступ к структуре хроматина ферментов и белков, необходимых для транскрипции и последующей трансляции.
Существует два основных класса гликозилаз: монофункциональные и бифункциональные. Монофункциональные гликозилазы обладают только гликозилазной активностью, тогда как бифункциональные гликозилазы также обладают активностью AP лиазы, которая позволяет им разрезать фосфодиэфирную связь ДНК, создавая однонитевой разрыв без необходимости AP эндонуклеаза. β-Удаление АР-сайта гликозилазой-лиазой дает 3 'α, β-ненасыщенный альдегид, соседний с 5' фосфатом, который отличается от продукта расщепления АР-эндонуклеазой. Некоторые гликозилазы-лиазы могут дополнительно выполнять -элиминирование, которое превращает 3'-альдегид в 3'-фосфат.
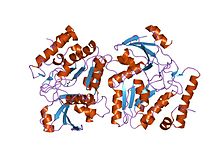
Первая кристаллическая структура ДНК-гликозилазы была получена для E. coli Nth. Эта структура показала, что фермент переворачивает поврежденное основание из двойной спирали в карман активного сайта, чтобы вырезать его. С тех пор было обнаружено, что другие гликозилазы следуют той же общей парадигме, включая человеческий UNG, изображенный ниже. Чтобы расщепить N-гликозидную связь, монофункциональные гликозилазы используют активированную молекулу воды для атаки на углерод 1 субстрата. Вместо этого бифункциональные гликозилазы используют остаток амина в качестве нуклеофила для атаки на тот же углерод, проходя через промежуточное соединение основание Шиффа.
Решены кристаллические структуры многих гликозилаз. На основании структурного сходства гликозилазы разделены на четыре суперсемейства. Семейства UDG и AAG содержат небольшие компактные гликозилазы, тогда как семейства MutM / Fpg и HhH-GPD содержат более крупные ферменты с множеством
Широкий спектр гликозилаз эволюционировал для распознавания различных поврежденных оснований. В таблице ниже суммированы свойства известных гликозилаз в обычно изучаемых модельных организмах.
| E. coli | B. cereus | Дрожжи (S. cerevisiae) | Человек | Тип | Субстраты |
|---|---|---|---|---|---|
| AlkA | AlkE | Mag1 | MPG (N-метилпурин ДНК-гликозилаза) | монофункциональная | 3-meA (3-алкиладенин), гипоксантин |
| UDG | Ung1 | UNG | монофункциональный | урацил | |
| Fpg | hOGG1 | бифункциональный | 8-oxoG (8-оксогуанин), FapyG | ||
| Nth | Ntg1 | h | бифункциональный | Tg, hoU, hoC, мочевина, FapyG (2,6-диамино-4-гидрокси-5-формамидопиримидин) | |
| Ntg2 | |||||
| Nei | Не присутствует | hNEIL1 | бифункциональный | Tg, hoU, hoC, мочевина, FapyG, FapyA (4,6-диамино-5-формамидопиримидин) | |
| hNEIL2 | AP сайт, hoU | ||||
| hNEIL3 | неизвестно | ||||
| MutY | Отсутствует | hMYH | монофункциональный | A: 8-oxoG | |
| Нет присутствует | Отсутствует | hSMUG1 | монофункциональный | U, hoU (5-гидроксиурацил), hmU (5-гидроксиметилурацил), fU (5-формилурацил) | |
| Нет | Нет | TDG | монофункциональный | T: G несоответствующая пара | |
| Отсутствует | Отсутствует | MBD4 | монофункциональный | T: G неправильное соединение | |
| AlkC | AlkC | Отсутствует | Отсутствует | монофункциональный | Алкилпурин |
| AlkD | AlkD | Отсутствует | Отсутствует | монофункциональные | Алкилпурин |
ДНК-гликозилазы могут быть сгруппированы в следующие категории в зависимости от их субстрата (субстратов):
 Структура фермента эксцизионной репарации урацил-ДНК-гликозилаза. Остаток урацила показан желтым.
Структура фермента эксцизионной репарации урацил-ДНК-гликозилаза. Остаток урацила показан желтым. В молекулярной биологии, семейство белков, урацил-ДНК-гликозилаза (UDG) представляет собой фермент, который возвращает мутации в ДНК. Наиболее распространенной мутацией является дезаминирование цитозина в урацил. UDG исправляет эти мутации. UDG имеет решающее значение в репарации ДНК, без него эти мутации могут привести к раку.
Эта запись представляет различные урацил-ДНК-гликозилазы и родственные ДНК-гликозилазы (EC ), например как урацил-ДНК-гликозилаза, термофильная урацил-ДНК-гликозилаза, G: T / U-специфическая ДНК-гликозилаза (Mug) и одноцепочечная селективная монофункциональная урацил-ДНК-гликозилаза (SMUG1).
Урацил-ДНК-гликозилазы удаляют урацил из ДНК, что может возникнуть либо в результате спонтанного дезаминирования цитозина, либо в результате неправильного включения dU напротив dA во время репликации ДНК. Прототипом этого семейства является UDG E. coli, который был одной из первых обнаруженных гликозилаз. В клетках млекопитающих идентифицированы четыре различных активности урацил-ДНК-гликозилазы, включая UNG, SMUG1, TDG и MBD4. Они различаются по субстратной специфичности и субклеточной локализации. SMUG1 предпочитает одноцепочечную ДНК в качестве субстрата, но также удаляет U из двухцепочечной ДНК. Помимо немодифицированного урацила, SMUG1 может вырезать 5-гидроксиурацил, 5-гидроксиметилурацил и 5-формилурацил, несущие окисленную группу в кольце C5. TDG и MBD4 строго специфичны для двухцепочечной ДНК. TDG может удалять тимингликоль, когда присутствует напротив гуанина, а также производные U с модификациями у углерода 5. Текущие данные свидетельствуют о том, что в клетках человека TDG и SMUG1 являются основными ферментами, ответственными за восстановление неправильных пар U: G, вызванных спонтанное дезаминирование цитозина, тогда как с урацилом, возникающим в ДНК из-за неправильного включения dU, в основном занимается UNG. Считается, что MBD4 корректирует несовпадения T: G, которые возникают в результате дезаминирования 5-метилцитозина до тимина в сайтах CpG. Мыши с мутантами MBD4 развиваются нормально и не проявляют повышенной восприимчивости к раку или снижения выживаемости. Но они приобретают больше CT-мутаций в последовательностях CpG в эпителиальных клетках тонкой кишки.
Структура UNG человека в комплексе с ДНК показала, что, как и другие гликозилазы, он переворачивает целевой нуклеотид из двойной спирали и в карман активного сайта. UDG претерпевает конформационные изменения из "открытого" несвязанного состояния в "закрытое" состояние с ДНК.
| UDG | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 урацил-ДНК-гликозилаза вируса Эпштейна-Барра в комплексе с ugi из pbs-2 урацил-ДНК-гликозилаза вируса Эпштейна-Барра в комплексе с ugi из pbs-2 | |||||||||
| Идентификаторы | |||||||||
| Символ | UDG | ||||||||
| Pfam | PF03167 | ||||||||
| InterPro | IPR005122 | ||||||||
| PROSITE | PDOC00121 | ||||||||
| SCOPe | 1udg / SUPFAM | ||||||||
| CDD | cd09593 | ||||||||
| |||||||||
Линдал был первым, кто наблюдал восстановление урацила в ДНК. UDG был очищен от Escherichia coli, и он гидролизовал N- гликозидную связь, соединяющую основание с дезоксирибозным сахаром основной цепи ДНК.
Функция UDG состоит в том, чтобы удалить мутации в ДНК, а точнее удалить урацил.
Эти белки имеют трехслойную альфа / бета / альфа структуру. Топология полипептида UDG соответствует классическому альфа / бета-белку. Структура состоит в основном из центрального четырехцепочечного, полностью параллельного бета-листа, окруженного с обеих сторон в общей сложности восемью альфа-спиралями, и называется параллельным бета-листом с двойной намоткой.
Урацил-ДНК-гликозилазы представляют собой ферменты репарации ДНК , которые вырезают урацил остатки из ДНК, расщепляя N-гликозидную связь, инициируя эксцизионную репарацию оснований путь. Урацил в ДНК может возникать либо в результате дезаминирования цитозина с образованием мутагенных U: G-пар, либо в результате включения dUMP ДНК полимеразой с образованием пар U: A . Эти аберрантные остатки урацила являются генотоксичными.
В эукариотических клетках активность UNG обнаруживается как в ядре, так и в митохондриях.. Человеческий белок UNG1 транспортируется как в митохондрии, так и в ядро .
последовательность урацил-ДНК-гликозилазы чрезвычайно хорошо консервативен в бактериях и эукариот, а также в вирусах герпеса. Более отдаленные родственные урацил-ДНК-гликозилазы также обнаружены в поксвирусах. N-концевые 77 аминокислот UNG1, по-видимому, необходимы для митохондриальной локализации, но присутствие митохондриального транзитного пептида имеет прямо не продемонстрировано. Наиболее N-концевой консервативный участок содержит остаток аспарагиновой кислоты , который был предложен на основании структур X-ray действует как общее основание в каталитическом механизме.
Существует два семейства UDG, названных Семейство 1 и Семейство 2. Семейство 1 активно против урацил в оцДНК и дцДНК. Семейство 2 вырезает урацил из несовпадений с гуанином.
 8-oxoG (syn) в паре оснований Хугстина с dA (анти)
8-oxoG (syn) в паре оснований Хугстина с dA (анти) Разнообразные гликозилазы эволюционировали, чтобы распознавать окисленные основания, которые обычно образуются из активных форм кислорода, образующихся в процессе клеточного метаболизма. Наиболее частыми повреждениями, образованными на остатках гуанина, являются 2,6-диамино-4-гидрокси-5-формамидопиримидин (FapyG) и 8-оксогуанин. Из-за неправильного спаривания с аденином во время репликации 8-oxoG обладает сильным мутагенным действием, что приводит к трансверсиям G в T. Восстановление этого повреждения инициируется бифункциональной ДНК-гликозилазой OGG1, которая распознает 8-oxoG в паре с C. hOGG1 представляет собой бифункциональную гликозилазу, которая принадлежит к семейству спираль-шпилька-спираль (HhH). MYH распознает аденин, несвязанный с 8-oxoG, но удаляет A, оставляя 8-oxoG нетронутым. Мыши с нокаутом OGG1 не демонстрируют увеличения заболеваемости опухолями, но с возрастом накапливают 8-oxoG в печени. Аналогичный фенотип наблюдается при инактивации MYH, но одновременная инактивация как MYH, так и OGG1 вызывает накопление 8-oxoG во многих тканях, включая легкие и тонкий кишечник. У людей мутации MYH связаны с повышенным риском развития полипов толстой кишки и рака толстой кишки. Помимо OGG1 и MYH, клетки человека содержат три дополнительных ДНК-гликозилазы: NEIL1, NEIL2 и NEIL3. Они гомологичны бактериальному Nei, и их присутствие, вероятно, объясняет умеренные фенотипы мышей с нокаутом OGG1 и MYH.
Эта группа включает E.coli AlkA и родственные белки высших эукариот. Эти гликозилазы являются монофункциональными и распознают метилированные основания, такие как 3-метиладенин.
AlkA относится к 3-метиладенин-ДНК-гликозилазе II.
Эпигенетические изменения (эпимутации) в генах ДНК-гликозилазы только недавно начали проявляться быть оцененным для нескольких видов рака, по сравнению с многочисленными предыдущими исследованиями эпимутаций в генах, действующих в других путях репарации ДНК (таких как MLH1 при репарации несоответствия и MGMT при прямом обращении). Ниже приведены два примера эпимутаций генов ДНК-гликозилаз, которые происходят при раке.
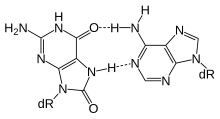
 Гидролиз цитозина до урацила
Гидролиз цитозина до урацила MBD4 (белок 4 метил-CpG-связывающего домена) представляет собой гликозилазу, используемую на начальной стадии эксцизионной репарации оснований. Белок MBD4 предпочтительно связывается с полностью метилированными сайтами CpG. Эти измененные основания возникают в результате частого гидролиза цитозина до урацила (см. Изображение) и гидролиза 5-метилцитозина до тимина с образованием пар оснований G: U и G: T. Если неподходящие урацилы или тимины в этих парах оснований не удалить до репликации ДНК, они вызовут мутации перехода . MBD4 специфически катализирует удаление T и U, спаренных с гуанином (G) в сайтах CpG. Это важная функция репарации, поскольку примерно 1/3 всех внутригенных мутаций одной пары оснований при раке человека происходит в динуклеотидах CpG и является результатом переходов G: C в A: T. Эти переходы включают наиболее частые мутации при раке человека. Например, почти 50% соматических мутаций гена-супрессора опухолей p53 при колоректальном раке представляют собой переходы из G: C в A: T в сайтах CpG. Таким образом, снижение экспрессии MBD4 может вызвать увеличение канцерогенных мутаций.
Экспрессия MBD4 снижена почти во всех колоректальных новообразованиях из-за метилирования области промотора MBD4. Кроме того, MBD4 является дефицитным из-за мутации примерно в 4% случаев колоректального рака
Большинство гистологически нормальных полей, окружающих опухолевые образования (аденомы и рак толстой кишки) в толстой кишке, также демонстрируют сниженную экспрессию мРНК MBD4 (a полевой дефект ) по сравнению с гистологически нормальной тканью людей, у которых никогда не было новообразований толстой кишки. Это открытие предполагает, что эпигенетическое молчание MBD4 является ранней стадией колоректального канцерогенеза.
В китайской популяции, которая была оценена, полиморфизм MBD4 Glu346Lys был связан примерно с Снижение риска рака шейки матки на 50%, что позволяет предположить, что изменения в MBD4 важны для этого рака.
Nei-like (NEIL) 1 - это ДНК-гликозилаза семейства Nei (которая также содержит NEIL2 и NEIL3). NEIL1 является компонентом репликационного комплекса ДНК, необходимого для наблюдения за окисленными основаниями перед репликацией, и, по-видимому, действует как «ловец коров» для замедления репликации до тех пор, пока NEIL1 не сможет действовать как гликозилаза и удалять окислительно поврежденное основание.
NEIL1 белок распознает (направляет) и удаляет определенные окислительно -поврежденные основания, а затем надрезает абазический сайт посредством β-, δ-элиминации, оставляя 3'- и 5'-фосфатные концы. NEIL1 распознает окисленные пиримидины, формамидопиримидины, тимин остатки, окисленные по метильной группе, и оба стереоизомера тимингликоля. Лучшими субстратами для человеческого NEIL1, по-видимому, являются поражения гидантоином, гуанидиногидантоин и спироиминодигидантоин, которые являются продуктами дальнейшего окисления 8-oxoG. NEIL1 также способен удалять повреждения из одноцепочечной ДНК, а также из пузырьковых и разветвленных структур ДНК. Дефицит NEIL1 вызывает усиление мутагенеза на участке пары 8-оксо-Gua: C, при этом большинство мутаций приходится на трансверсии G: C в T: A.
Исследование 2004 года показало, что 46% первичных При раке желудка наблюдалось снижение экспрессии мРНК NEIL1 , хотя механизм снижения не был известен. Это исследование также показало, что 4% случаев рака желудка имеют мутации в гене NEIL1. Авторы предположили, что низкая активность NEIL1, обусловленная сниженной экспрессией и / или мутацией гена NEIL1, часто участвует в канцерогенезе желудка.
Скрининг 145 генов репарации ДНК на аберрантное метилирование промотора был проведен на тканях плоскоклеточного рака головы и шеи (HNSCC) у 20 пациентов и на образцах слизистой оболочки головы и шеи у 5 пациентов, не страдающих раком. Этот скрининг показал, что ген NEIL1 имел существенно повышенное гиперметилирование, и из 145 оцениваемых генов репарации ДНК NEIL1 имел наиболее существенно различающуюся частоту метилирования. Более того, гиперметилирование соответствовало снижению экспрессии мРНК NEIL1. Дальнейшая работа с 135 опухолевыми и 38 нормальными тканями также показала, что 71% образцов ткани HNSCC имели повышенное метилирование промотора NEIL1.
Когда оценивали 8 генов репарации ДНК при немелкоклеточном раке легкого (NSCLC) 42% опухолей были гиперметилированы в промоторной области NEIL1. Это была самая частая аномалия репарации ДНК, обнаруженная среди 8 протестированных генов репарации ДНК. NEIL1 также был одним из шести генов репарации ДНК, которые, как было обнаружено, гиперметилированы в их промоторных областях при колоректальном раке.