| Вирусы простого герпеса 81i2 | |
|---|---|
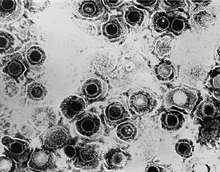 | |
| TEM микрофотография вирионов вид вируса простого герпеса | |
| Научная классификация | |
| (без рейтинга): | Вирус |
| Область: | Duplodnaviria |
| Королевство: | Heunggongvirae |
| Тип: | Peploviricota |
| Класс: | Herviviricetes |
| Порядок: | Herpesvirales |
| Семейство: | Herpesviridae |
| Подсемейство: | Alphaherpesvirinae |
| Род: | Simplexvirus |
| Включенные группы | |
| Кладистически включены, но традиционно исключены таксоны | |
Все другие виды симплексвирусов: | |
вирус простого герпеса 1и 2(HSV-1 и HSV-2 ), также известные под их таксономическими названиями Human alphaherpesvirus 1 и Человеческий альфа-герпесвирус 2 - это два члена семейства герпесвирусов человека, набора новых вирусов, вызывающих вирусные инфекции у большинства людей. И HSV-1 (который вызывает большинство герпеса ), и HSV-2 (который вызывает большинство генитального герпеса ) являются обычными и заразными. Они могут распространяться, когда инфицированный человек начинает выделять вирус .
. Около 67% населения мира в возрасте до 50 лет заражено ВПГ-1. Считается, что в Соединенных Штатах около 47,8% и 11,9% инфицированы ВПГ-1 и ВПГ-2 соответственно. Поскольку он может передаваться при любом интимном контакте, это одна из наиболее распространенных инфекций, передаваемых половым путем.
Многие из инфицированных никогда не проявляют никаких симптомов. Симптомы, когда они возникают, могут включать водянистые волдыри на коже или слизистых оболочках рта, губ, носа или половых органов. Поражения заживают струпом, характерным для герпетической болезни. Иногда во время вспышек вирусы вызывают легкие или атипичные симптомы. Однако они также могут вызывать более неприятные формы простого герпеса. Поскольку нейротропные и нейроинвазивные вирусы, HSV-1 и -2 сохраняются в организме, скрываясь от иммунной системы в клетках тел нейронов. После первоначального или первичного заражения у некоторых инфицированных людей возникают спорадические эпизоды вирусной реактивации или вспышки. Во время вспышки вирус в нервной клетке становится активным и транспортируется через аксон нейрона к коже, где происходит репликация и выделение вируса, вызывающие новые язвы.
ВПГ-1 и ВПГ-2 передаются при контакте с инфицированным человеком, у которого есть реактивация вируса. ВПГ-2 периодически выделяется в половых путях человека, чаще всего бессимптомно. Большинство случаев передачи половым путем происходит в периоды бессимптомного выделения. Бессимптомная реактивация означает, что вирус вызывает атипичные, незаметные или незаметные симптомы, которые не идентифицируются как активная герпетическая инфекция, поэтому заражение вирусом возможно даже при отсутствии активных волдырей или язв, связанных с ВПГ. В одном исследовании ежедневные пробы мазков из гениталий показали, что ВПГ-2 в среднем составляет 12–28% дней среди тех, у кого была вспышка, и 10% дней среди тех, кто страдает бессимптомной инфекцией, при этом многие из этих эпизодов происходят без видимых признаков. вспышка («субклиническое выделение»).
В другом исследовании 73 субъекта были рандомизированы для получения валацикловира 1 г ежедневно или плацебо в течение 60 дней каждый в двухстороннем перекрестном дизайне. Ежедневный мазок из области гениталий собирали самостоятельно для обнаружения ВПГ-2 с помощью полимеразной цепной реакции, чтобы сравнить влияние валацикловира и плацебо на бессимптомное выделение вируса у иммунокомпетентных серопозитивных субъектов, не имевших в анамнезе симптоматической инфекции генитального герпеса. Исследование показало, что валацикловир значительно снижает выделение в течение субклинических дней по сравнению с плацебо, показав снижение на 71%; У 84% субъектов не было выделений при приеме валацикловира по сравнению с 54% субъектов, получавших плацебо. Около 88% пациентов, получавших валацикловир, не имели распознаваемых признаков или симптомов по сравнению с 77% пациентов, получавших плацебо.
Для HSV-2 субклиническое выделение может составлять большую часть передачи. Исследования дискордантных партнеров (один инфицирован ВПГ-2, один нет) показывают, что скорость передачи составляет примерно 5 на 10 000 половых контактов. Атипичные симптомы часто связывают с другими причинами, такими как грибковая инфекция. ВПГ-1 часто передается орально в детстве. Он также может передаваться половым путем, включая контакт со слюной, например поцелуй и контакт рот к гениталиям (оральный секс ). ВПГ-2 в первую очередь передается половым путем, но частота половых инфекций ВПГ-1 растет.
Оба вируса также могут передаваться вертикально во время родов. Однако риск передачи инфекции минимален, если во время родов у матери отсутствуют симптомы или обнаружены волдыри. Риск велик, когда мать впервые заражается вирусом на поздних сроках беременности. Вопреки популярным мифам, герпес не может передаваться с поверхностей, таких как сиденья унитаза, потому что вирус герпеса начинает умирать сразу после выхода из тела.
Вирусы простого герпеса могут поражать участки кожи, контактирующие с инфицированным человеком ( хотя рукопожатие с инфицированным не передает эту болезнь). Примером этого является herpetic whitlow, то есть герпетическая инфекция пальцев. Это было обычным недугом хирургов-стоматологов до того, как стали регулярно использовать перчатки при лечении пациентов.
Инфекция HSV-2 увеличивает риск заражения ВИЧ.
 Воспроизвести медиа Трехмерная реконструкция и анимация хвостовидной сборки на капсиде HSV-1
Воспроизвести медиа Трехмерная реконструкция и анимация хвостовидной сборки на капсиде HSV-1 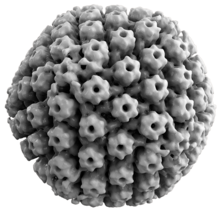 Трехмерная реконструкция капсида HSV-1
Трехмерная реконструкция капсида HSV-1  Герпес Симплексный вирус 2
Герпес Симплексный вирус 2 Все вирусы герпеса животных обладают некоторыми общими свойствами. Структура вирусов герпеса состоит из относительно большого, двухцепочечного, линейного ДНК генома, заключенного в икосаэдрическую белковую клетку, называемую капсидом, который завернут в липидный бислой , называемый оболочкой. Конверт соединяется с капсидом с помощью тегу . Эта полная частица известна как вирион. Каждый из ВПГ-1 и ВПГ-2 содержит по меньшей мере 74 гена (или открытые рамки считывания, ORF) в своих геномах, хотя предположения о скоплении генов допускают до 84 уникальных генов, кодирующих белок, с помощью 94 предполагаемых ORF. Эти гены кодируют множество белков, участвующих в формировании капсида, тегумента и оболочки вируса, а также контролирующих репликацию и инфекционность вируса. Эти гены и их функции обобщены в таблице ниже.
Геномы HSV-1 и HSV-2 являются сложными и содержат две уникальные области, называемые длинной уникальной областью (U L) и короткая уникальная область (U S). Из 74 известных ORF, U L содержит 56 вирусных генов, тогда как U S содержит только 12. Транскрипция генов HSV катализируется РНК-полимеразой II инфицированный хозяин. Немедленно ранние гены, которые кодируют белки, регулирующие экспрессию ранних и поздних вирусных генов, экспрессируются первыми после заражения. Далее следует ранняя экспрессия гена, позволяющая синтез ферментов, участвующих в репликации ДНК и выработке определенных гликопротеинов оболочки. В последнюю очередь происходит экспрессия поздних генов; эта группа генов преимущественно кодирует белки, которые образуют частицу вириона.
Пять белков из (U L) образуют вирусный капсид - UL6, UL18, UL35, UL38 и главный капсидный белок UL19.
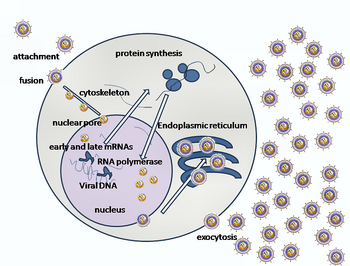 Упрощенная диаграмма репликации ВПГ
Упрощенная диаграмма репликации ВПГ Вхождение ВПГ в клетку-хозяина включает несколько гликопротеинов на поверхности оболочки связывание вируса с их трансмембранными рецепторами на поверхности клетки. Многие из этих рецепторов затем втягиваются внутрь клеткой, которая, как полагают, открывает кольцо из трех гетеродимеров gHgL, стабилизирующих компактную конформацию гликопротеина gB, так что он вырастает и прокалывает клеточную мембрану. Оболочка, покрывающая вирусную частицу, затем сливается с клеточной мембраной, создавая пору, через которую содержимое вирусной оболочки попадает в клетку-хозяин.
Последовательные стадии проникновения вируса простого герпеса аналогичны другим стадиям. вирусы. Сначала комплементарные рецепторы вируса и поверхности клетки сближают вирусную и клеточную мембраны. Затем взаимодействия этих молекул образуют стабильную входную пору, через которую содержимое вирусной оболочки вводится в клетку-хозяин. Вирус также может быть эндоцитозирован после связывания с рецепторами, и слияние может происходить в эндосоме. На электронных микрофотографиях видно, что внешние створки липидных бислоев вируса и клетки объединены; эта гемифузия может происходить по обычному пути к проникновению или обычно это может быть остановленное состояние с большей вероятностью, чем временный механизм проникновения.
В случае вируса герпеса начальные взаимодействия происходят, когда две вирусные оболочки гликопротеин, называемый гликопротеином C (gC), и гликопротеином B (gB) связываются с частицами клеточной поверхности, называемыми гепарансульфатом. Затем основной связывающий рецептор белок, гликопротеин D (gD), специфически связывается по крайней мере с одним из трех известных рецепторов входа. Эти клеточные рецепторы включают медиатор проникновения вируса герпеса (HVEM ), нектин -1 и 3-O сульфатированный гепарансульфат. Рецепторы нектина обычно производят клеточную адгезию, чтобы обеспечить надежную точку прикрепления вируса к клетке-хозяину. Эти взаимодействия сближают поверхности мембран и позволяют другим гликопротеинам, встроенным в вирусную оболочку, взаимодействовать с другими молекулами клеточной поверхности. После связывания с HVEM, gD изменяет свою конформацию и взаимодействует с вирусными гликопротеинами H (gH) и L (gL), которые образуют комплекс. Взаимодействие этих мембранных белков может привести к состоянию гемифузии. Взаимодействие gB с комплексом gH / gL создает поры входа для вирусного капсида. gB взаимодействует с гликозаминогликанами на поверхности клетки-хозяина.
После того, как вирусный капсид попадает в клеточную цитоплазму, он транспортируется к ядру клетки. Прикрепившись к ядру в поре входа в ядро, капсид выбрасывает свое содержимое ДНК через портал капсида. Портал капсида образован 12 копиями портального белка UL6, расположенными в виде кольца; белки содержат последовательность лейциновой молнии из аминокислот, которая позволяет им прикрепляться друг к другу. Каждый икосаэдрический капсид содержит единственный портал, расположенный в одной вершине. ДНК выходит из капсида в виде единственного линейного сегмента.
ВПГ ускользает от иммунной системы посредством вмешательства в презентацию антигена MHC класса I на поверхности клетки посредством блокирование транспортера , связанного с процессингом антигена (TAP), индуцированным секрецией ICP-47 HSV. В клетке-хозяине TAP транспортирует переваренные пептиды эпитопа вирусного антигена из цитозоля в эндоплазматический ретикулум, позволяя этим эпитопам объединяться с молекулами MHC класса I и представляться на поверхности клетки. Презентация вирусного эпитопа с MHC класса I является требованием для активации цитотоксических Т-лимфоцитов (CTL), основных эффекторов клеточного иммунного ответа против инфицированных вирусом клеток. ICP-47 предотвращает инициирование CTL-ответа против HSV, позволяя вирусу выжить в течение длительного периода в организме хозяина.
 Микрофотография, демонстрирующая вирусный цитопатический эффект HSV (многоядерность, хроматин матового стекла)
Микрофотография, демонстрирующая вирусный цитопатический эффект HSV (многоядерность, хроматин матового стекла) После инфицирования клетки образуется каскад белков вируса герпеса, который называется немедленным-ранним, ранним и поздним. Исследование с использованием проточной цитометрии на другом члене семейства вирусов герпеса, вирусе герпеса, связанном с саркомой Капоши, указывает на возможность дополнительной литической стадии, отсроченной-поздней. Эти стадии литической инфекции, особенно поздней литической, отличаются от латентной стадии. В случае HSV-1 белковые продукты не обнаруживаются во время латентного периода, тогда как они обнаруживаются во время литического цикла.
Ранние транскрибируемые белки используются для регуляции генетической репликации вируса. Попадая в клетку, белок α-TIF присоединяется к вирусной частице и способствует немедленной ранней транскрипции. Белок отключения вириона-хозяина (VHS или UL41) очень важен для репликации вируса. Этот фермент отключает синтез белка в хозяине, разрушает мРНК хозяина, помогает в репликации вируса и регулирует экспрессию гена вирусных белков. Вирусный геном немедленно перемещается в ядро, но белок VHS остается в цитоплазме.
Поздние белки образуют капсид и рецепторы на поверхности вируса. Упаковка вирусных частиц, включая геном, ядро и капсид, происходит в ядре клетки. Здесь конкатемеры вирусного генома разделяются путем расщепления и помещаются в сформированные капсиды. ВПГ-1 проходит процесс первичной и вторичной оболочки. Первичная оболочка приобретается почкованием внутренней ядерной мембраны клетки. Затем он сливается с внешней ядерной мембраной, высвобождая голый капсид в цитоплазму. Вирус приобретает свою окончательную оболочку, образуя цитоплазматические пузырьки.
ВПГ могут сохраняться в неактивной, но стойкой форме, известной как латентная инфекция, особенно в нервных ганглиях. ВПГ-1 имеет тенденцию находиться в ганглиях тройничного нерва, тогда как ВПГ-2 имеет тенденцию находиться в крестцовых ганглиях, но это только тенденции, а не фиксированное поведение. Во время латентной инфекции клетки HSV экспрессируют связанный с латентностью транскрипт (LAT) РНК. LAT регулирует геном клетки-хозяина и препятствует естественным механизмам гибели клеток. Поддерживая клетки-хозяева, экспрессия LAT сохраняет резервуар вируса, что делает возможными последующие, обычно симптоматические, периодические рецидивы или «вспышки», характерные для нелатентности. Независимо от того, являются ли рецидивы симптоматическими или нет, происходит выделение вируса, чтобы заразить нового хозяина.
Белок, обнаруженный в нейронах, может связываться с ДНК вируса герпеса и регулировать латентность. ДНК вируса герпеса содержит ген белка ICP4, который является важным трансактиватором генов, связанных с литической инфекцией HSV-1. Элементы, окружающие ген ICP4, связывают белок, известный как человеческий нейрональный белок, фактор рестриктивного молчания нейронов (NRSF) или фактор транскрипции подавления репрессорного элемента человека (REST) . При связывании с элементами вирусной ДНК деацетилирование гистона происходит поверх последовательности гена ICP4 для предотвращения инициации транскрипции от этого гена, тем самым предотвращая транскрипцию других вирусных генов, участвующих в литическом цикле. Другой белок HSV обращает ингибирование синтеза белка ICP4. ICP0 отделяет NRSF от гена ICP4 и, таким образом, предотвращает подавление вирусной ДНК.
Геном HSV состоит из двух уникальных сегментов, называемых уникальными длинными (UL) и уникальные короткие (США), а также концевые инвертированные повторы, обнаруженные на двух их концах, названные «длинный повтор» (RL) и короткий повтор (RS). Есть также второстепенные элементы «оконечной избыточности» (α), обнаруженные на дальнейших концах RS. Общая компоновка - RL-UL-RL-α-RS-US-RS-α, где каждая пара повторов инвертирует друг друга. Затем вся последовательность инкапсулируется в конечный прямой повтор. Каждая длинная и короткая части имеют свои собственные источники репликации, при этом OriL расположен между UL28 и UL30, а OriS находится в паре рядом с RS. Поскольку сегменты L и S могут быть собраны в любом направлении, они могут свободно инвертироваться относительно друг друга, образуя различные линейные изомеры.
| ORF | Псевдоним белка | HSV-1 | HSV-2 | Функция / описание |
|---|---|---|---|---|
| Повторить длинный (R L) | ||||
| ICP0 / RL2 | ICP0; IE110; α0 | P08393 | P28284 | E3 убиквитин лигаза, которая активирует транскрипцию вирусного гена путем противодействия хроматинизации вирусного генома и противодействует внутреннему и интерферону противовирусные реакции на основе. |
| RL1; ICP34.5 | O12396 | Фактор нейровирулентности. Противодействует PKR путем дефосфорилирования eIF4a. Связывается и инактивирует аутофагию. | ||
| LAT | LRP1, LRP2 | P17588. P17589 | Продукты белка abd, связанные с латентным транскриптом (белок, связанный с латентностью) | |
| Уникальный длинный (U L) | ||||
| UL1 | Гликопротеин L | P10185 | Поверхность и мембрана | |
| UL2 | UL2 | P10186 | Урацил-ДНК-гликозилаза | |
| UL3 | U L3 | P10187 | неизвестно | |
| UL4 | UL4 | P10188 | неизвестно | |
| UL5 | UL5 | Q2MGV2 | Репликация ДНК | |
| UL6 | Портальный белок U L-6 | P10190 | Двенадцать из этих белков составляют портальное кольцо капсида, через которое ДНК входит и выходит из капсида. | |
| UL7 | UL7 | P10191 | Созревание вириона | |
| UL8 | UL8 | P10192 | ДНК вируса белок, ассоциированный с комплексом геликаза-примаза | |
| UL9 | UL9 | P10193 | Источник репликации -связывающий белок | |
| UL10 | Гликопротеин M | P04288 | Поверхность и мембрана | |
| UL11 | UL11 | P04289 | Выход вириона и вторичная оболочка | |
| UL12 | UL12 | Q68978 | Щелочная экзонуклеаза | |
| UL13 | UL13 | Q9QNF2 | Серин - треонин протеинкиназа | |
| UL14 | UL14 | P04291 | Тегумент белок | |
| UL15 | P04295 | Обработка и упаковка ДНК | ||
| UL16 | UL16 | P10200 | Тегументный белок | |
| UL17 | U L17 | P10201 | Обработка и упаковка ДНК | |
| UL18 | VP23 | P10202 | Капсид белок | |
| UL19 | VP5 | P06491 | Главный капсидный белок | |
| UL20 | UL20 | P10204 | Мембранный белок | |
| UL21 | UL21 | P10205 | Тегументный белок | |
| UL22 | Гликопротеин H | P06477 | Поверхность и мембрана | |
| UL23 | Тимидинкиназа | O55259 | Периферическая репликация ДНК | |
| UL24 | UL24 | P10208 | неизвестно | |
| UL25 | UL25 | P10209 | Обработка и упаковка ДНК | |
| UL26 | P40; VP24; VP22A; UL26.5 (короткая изоформа HHV2) | P10210 | P89449 | Капсидный белок |
| UL27 | Гликопротеин B | A1Z0P5 | Поверхность и мембрана | |
| UL28 | ICP18.5 | P10212 | Обработка и упаковка ДНК | |
| UL29 | UL29; ICP8 | Q2MGU6 | Главный ДНК-связывающий белок | |
| UL30 | ДНК-полимераза | Q4ACM2 | Репликация ДНК | |
| UL31 | UL31 | Q25BX0 | Ядерная матричный белок | |
| UL32 | UL32 | P10216 | Конверт гликопротеин | |
| UL33 | UL33 | P10217 | Обработка и упаковка ДНК | |
| UL34 | UL34 | P10218 | Белок внутренней ядерной мембраны | |
| UL35 | VP26 | P10219 | Капсидный белок | |
| UL36 | UL36 | P10220 | Большой тегументный белок | |
| UL37 | UL37 | P10216 | Сборка капсида | |
| UL38 | UL38; VP19C | P32888 | Сборка капсида и созревание ДНК | |
| UL39 | UL39; РР-1; ICP6 | P08543 | Рибонуклеотидредуктаза (большая субъединица) | |
| UL40 | UL40; RR-2 | P06474 | Рибонуклеотидредуктаза (малая субъединица) | |
| UL41 | UL41; VHS | P10225 | белок тегумента; выключение хозяина вириона | |
| UL42 | UL42 | Q4H1G9 | ДНК-полимераза фактор процессивности | |
| UL43 | UL43 | P10227 | Мембранный белок | |
| UL44 | Гликопротеин C | P10228 | Поверхность и мембрана | |
| UL45 | UL45 | P10229 | Мембранный белок; Лектин С-типа | |
| UL46 | VP11 / 12 | P08314 | Тегументные белки | |
| UL47 | UL47; VP13 / 14 | P10231 | Тегументный белок | |
| UL48 | VP16 (Alpha-TIF) | P04486 | Созревание вириона; активировать гены IE, взаимодействуя с клеточными факторами транскрипции Oct-1 и HCF. Связывается с последовательностью TAATGARAT. | |
| UL49 | UL49A | O09800 | Белок оболочки | |
| UL50 | UL50 | P10234 | dUTP дифосфатаза | |
| UL51 | UL51 | P10234 | Тегументный белок | |
| UL52 | UL52 | P10236 | Комплексный белок ДНК-геликаза / примаза | |
| UL53 | Гликопротеин K | P68333 | Поверхность и мембрана | |
| UL54 | IE63; ICP27 | P10238 | Регуляция транскрипции и ингибирование сигнала STING | |
| UL55 | UL55 | P10239 | Неизвестно | |
| UL56 | UL56 | P10240 | Неизвестно | |
| Инвертированный длинный повтор (IR L) | ||||
| Инвертированный короткий повтор) (IR S) | ||||
| Уникальный короткий (U S) | ||||
| US1 | ICP22; IE68 | P04485 | Репликация вируса | |
| US2 | US2 | P06485 | Неизвестно | |
| US3 | P04413 | Серин / треонин-протеинкиназа | ||
| US4 | Гликопротеин G | P06484 | Поверхность и мембрана | |
| Гликопротеин J | P06480 | Поверхность и мембрана | ||
| Гликопротеин D | A1Z0Q5 | Поверхность и мембрана | ||
| US7 | Гликопротеин I | P06487 | Поверхность и мембрана | |
| US8 | Гликопротеин E | Q703F0 | Поверхность и мембрана | |
| US9 | US9 | P06481 | Тегументный белок | |
| US10 | US10 | P06486 | Капсид / тегументный белок | |
| US11 | US11; Vmw21 | P56958 | Связывает ДНК и РНК | |
| US12 | ; IE12 | P03170 | Ингибирует MHC класса I путь путем предотвращения связывания антигена с TAP | |
| Короткий концевой повтор (TR S) | ||||
| RS1 | ; IE175 | P08392 | Главный активатор транскрипции. Существенен для прогрессирования за пределами непосредственной ранней фазы инфекции. IEG репрессор транскрипции. | |
Геномы простого герпеса 1 можно разделить на шесть клад. Четыре из них встречаются в Восточной Африке, один в Восточной Азии и один в Европе и Северной Америке. Это говорит о том, что вирус, возможно, возник в Восточной Африке. Самый последний общий предок евразийских штаммов, по-видимому, появился около 60 000 лет назад. Изоляты восточноазиатского HSV-1 имеют необычный паттерн, который в настоящее время лучше всего объясняется двумя волнами миграции, ответственными за заселение Японии.
геномов Herpes simplex 2, которые можно разделить на две группы: одна распространена по всему миру и другой в основном ограничен Африкой к югу от Сахары. Глобально распределенный генотип претерпел четыре древних рекомбинации с простым герпесом 1. Также сообщалось, что HSV-1 и HSV-2 могут иметь современные и стабильные события рекомбинации у хозяев, одновременно инфицированных обоими патогенами. Во всех случаях ВПГ-2 приобретает части генома ВПГ-1, иногда в процессе меняя части его антигенного эпитопа.
Скорость мутации оценивается в ~ 1,38 × 10 замен / сайт / год. В клинических условиях мутации в гене тимидинкиназы или гене ДНК-полимеразы вызвали устойчивость к ацикловиру. Однако большинство мутаций происходит в гене тимидинкиназы, а не в гене ДНК-полимеразы.
Другой анализ показал, что частота мутаций в геноме простого герпеса 1 составляет 1,82 × 10 замен нуклеотидов на сайт в год. Этот анализ поместил самого последнего общего предка этого вируса ~ 710 000 лет назад.
Простой герпес 1 и 2 разошлись примерно 6 миллионов лет назад.
Вирусы герпеса вызывают пожизненные инфекции (таким образом, не могут быть устранены из организма).
Лечение обычно включает противовирусные препараты общего назначения, которые препятствуют репликации вируса, уменьшают физическую тяжесть поражения, связанные со вспышкой, и снижают вероятность передачи другим. Исследования уязвимых групп пациентов показали, что ежедневное использование противовирусных препаратов, таких как ацикловир и валацикловир, может снизить скорость реактивации. Широкое применение противогерпетических препаратов привело к развитию лекарственной устойчивости, что, в свою очередь, приводит к неэффективности лечения. Поэтому для решения этой проблемы широко исследуются новые источники лекарств. В январе 2020 года была опубликована всеобъемлющая обзорная статья, в которой продемонстрирована эффективность натуральных продуктов как многообещающих препаратов против ВПГ.
Пиритион, цинк ионофор, проявляет противовирусную активность против вируса простого герпеса.
В 1979 году сообщалось о возможной связи между ВПГ-1 и болезнью Альцгеймера у людей с аллелем эпсилон4 . гена APOE. ВПГ-1 особенно опасен для нервной системы и увеличивает риск развития болезни Альцгеймера. Вирус взаимодействует с компонентами и рецепторами липопротеинов, что может привести к развитию болезни Альцгеймера. Это исследование идентифицирует HSV как патоген, наиболее явно связанный с установлением болезни Альцгеймера. Согласно исследованию, проведенному в 1997 году, без присутствия гена аллеля HSV-1, по-видимому, не вызывает каких-либо неврологических повреждений или увеличивает риск болезни Альцгеймера. Однако более недавнее проспективное исследование, опубликованное в 2008 году с когортой из 591 человека, показало статистически значимое различие между пациентами с антителами, указывающими на недавнюю реактивацию ВПГ, и пациентами без этих антител в заболеваемости болезнью Альцгеймера без прямой корреляции с APOE-эпсилон4.
В исследовании была небольшая выборка пациентов, у которых не было антител на исходном уровне, поэтому результаты следует рассматривать как весьма неопределенные. В 2011 году ученые Манчестерского университета показали, что обработка инфицированных HSV1 клеток противовирусными средствами снижает накопление β-амилоида и тау-белка, а также снижает репликацию HSV-1.
Ретроспективное исследование 2018 г., проведенное в Тайване с участием 33000 пациентов, показало, что инфицирование вирусом простого герпеса увеличивает риск деменции в 2,56 раза (95% ДИ: 2,3-2,8) у пациентов, не получающих противогерпетические препараты ( 2,6 раза для инфекций HSV-1 и 2,0 раза для инфекций HSV-2). Однако у инфицированных ВПГ пациентов, получавших противогерпетические препараты (ацикловир, фамцикловир, ганцикловир, идоксуридин, пенцикловир, тромантадин, валацикловир или валганцикловир), не было повышенного риска деменции по сравнению с пациентами, не инфицированными ВПГ.
Реактивация множественности (MR) - это процесс, с помощью которого вирусные геномы, содержащие инактивирующие повреждения, взаимодействуют в инфицированной клетке с образованием жизнеспособного вирусного генома. MR был первоначально обнаружен с бактериофагом T4 бактериального вируса, но впоследствии был также обнаружен с патогенными вирусами, включая вирус гриппа, ВИЧ-1, аденовирус обезьяньего вируса 40, вирус осповакцины, реовирус, полиовирус и вирус простого герпеса.
Когда Частицы ВПГ подвергаются воздействию доз повреждающего ДНК агента, которые могут быть летальными при единичных инфекциях, но затем могут подвергнуться множественной инфекции (т.е. двум или более вирусам на клетку-хозяина), наблюдается MR. Повышенная выживаемость HSV-1 из-за MR происходит при воздействии различных повреждающих ДНК агентов, включая метилметансульфонат, триметилпсорален (который вызывает межцепочечные сшивки ДНК) и УФ-свет. После обработки генетически маркированного ВПГ триметилпсораленом рекомбинация между маркированными вирусами усиливается, что позволяет предположить, что повреждение триметилпсораленом стимулирует рекомбинацию. MR HSV, по-видимому, частично зависит от механизма рекомбинационной репарации клеток-хозяев, поскольку клетки фибробластов кожи, дефектные по компоненту этого механизма (например, клетки пациентов с синдромом Блума), испытывают дефицит MR.
Эти наблюдения предполагают, что MR в Инфекции HSV включают генетическую рекомбинацию между поврежденными вирусными геномами, приводящую к образованию жизнеспособных потомков вирусов. HSV-1 при инфицировании клеток-хозяев вызывает воспаление и окислительный стресс. Таким образом, оказывается, что геном HSV может подвергаться окислительному повреждению ДНК во время инфекции, и что MR может повышать выживаемость и вирулентность вируса в этих условиях.
Модифицированный вирус простого герпеса считается потенциальным средством лечения рака и прошел всесторонние клинические испытания для оценки его онколитических свойств. (убивать рак) способность. Промежуточные данные об общей выживаемости из исследования Amgen фазы 3 генетически аттенуированного вируса герпеса свидетельствуют об эффективности против меланомы.
Вирус простого герпеса также используется в качестве транснейронального индикатора, определяющего связи между нейронами посредством прохождения синапсов.
Вирус простого герпеса, вероятно, является наиболее частой причиной болезни Молларе. менингит. В худшем случае это может привести к потенциально смертельному случаю энцефалита простого герпеса.
Существуют широко используемые вакцины против некоторых вирусов герпеса, но только ветеринарные, такие как (вектор герпесвируса Турции вакцина против ларинготрахеита). Однако он предотвращает атеросклероз (который гистологически отражает атеросклероз у людей) у вакцинированных животных-мишеней.