 | |
| Имена | |
|---|---|
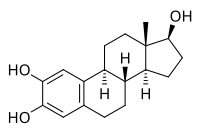
| Название IUPAC (8R, 9S, 13S, 14S, 17S) -13-Метил-6,7,8,9,11,12,14,15,16,17-декагидроциклопента [a] фенантрен-2,3,17-триол | |
| Другие названия 2 -ОНЕ2; Эстра-1,3,5 (10) -триен-2,3,17β-триол | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.160.393 |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C18H24O3 |
| Молярная масса | 288,387 г · моль |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
2-гидроксиэстрадиол (2-OHE2 ), также известный как эстра-1,3,5 (10) -триен-2,3,17β-триол, представляет собой эндогенный стероид, катехол эстроген и метаболит эстрадиола, а также позиционный изомер эстриола.
Превращение эстрадиола в 2-гидроксиэстрадиол является основным метаболическим путем эстрадиола в печень. CYP1A2 и CYP3A4 являются основными ферментами, катализирующими 2-гидроксилирование эстрадиола. Превращение эстрадиола в 2-гидроксиэстрадиол также было обнаружено в матке, груди, почках, мозге и гипофизе. железа, а также плаценты, и могут аналогичным образом опосредоваться ферментами цитохрома P450. Хотя эстрадиол в значительной степени превращается в 2-гидроксиэстрадиол, циркулирующие уровни 2-гидроксиэстрадиола и уровни 2-гидроксиэстрадиола в различных тканях очень низкие. Это может быть связано с быстрым конъюгированием (O- метилирование, глюкуронирование, сульфирование ) 2-гидроксиэстрадиола с последующим мочевым экскреция.
2-гидроксиэстрадиол имеет примерно 7% и 11% от аффинности эстрадиола в рецепторы эстрогена (ER) ERα и ERβ соответственно. Он диссоциирует от рецепторов эстрогена быстрее, чем эстрадиол. Стероид очень слабо эстроген и способен противодействовать эстрогенным эффектам эстрадиола, что указывает на его внутреннюю активность на рецепторе эстрогена меньше, чем у эстрадиола, и, следовательно, он обладает профилем селективного модулятора рецептора эстрогена. Он показывает эстрогенную активность в отношении клеток рака груди человека. В дополнение к своей активности в отношении ядерных ER 2-гидроксиэстрадиол является антагонистом G-белкового рецептора эстрогена (GPER) (100–1000 мкМ).
| Эстроген | ER RBA (%) | Масса матки (%) | Уровни утеротрофии | LH (%) | SHBG RBA (%) |
|---|---|---|---|---|---|
| Контроль | – | 100 | – | 100 | – |
| Эстрадиол | 100 | 506 ± 20 | ++ + | 12–19 | 100 |
| Эстрон | 11 ± 8 | 490 ± 22 | +++ | ? | 20 |
| Эстриол | 10 ± 4 | 468 ± 30 | +++ | 8–18 | 3 |
| Эстетрол | 0,5 ± 0,2 | ? | Неактивный | ? | 1 |
| 17α-эстрадиол | 4,2 ± 0,8 | ? | ? | ? | ? |
| 2-гидроксиэстрадиол | 24 ± 7 | 285 ± 8 | + | 31–61 | 28 |
| 2-Метоксиэстрадиол | 0,05 ± 0,04 | 101 | Неактивный | ? | 130 |
| 4-Гидроксиэстрадиол | 45 ± 12 | ? | ? | ? | ? |
| 4-Метоксиэстрадиол | 1,3 ± 0,2 | 260 | ++ | ? | 9 |
| 4-фторэстрадиол | 180 ± 43 | ? | +++ | ? | ? |
| 2-гидроксиэстрон | 1,9 ± 0,8 | 130 ± 9 | Неактивно | 110–142 | 8 |
| 2-метоксиэстрон | 0,01 ± 0,00 | 103 ± 7 | Неактивный | 95–100 | 120 |
| 4-гидроксиэстрон | 11 ± 4 | 351 | ++ | 21–50 | 35 |
| 4-метоксиэстрон | 0,13 ± 0,04 | 338 | ++ | 65–92 | 12 |
| 16α-гидроксиэстрон | 2,8 ± 1,0 | 552 ± 42 | +++ | 7–24 | <0.5 |
| 2-гидроксиэстриол | 0,9 ± 0,3 | 302 | + | ? | ? |
| 2-метоксиэстриол | 0,01 ± 0,00 | ? | неактивный | ? | 4 |
| Примечания: Значения являются средними ± стандартное отклонение или диапазон. ERRBA = Относительная аффинность связывания с рецепторами эстрогена крысы матки цитозоль. Масса матки = процентное изменение влажной массы матки крыс с удаленными яичниками через 72 часа при непрерывном введении 1 мкг / час с помощью подкожно имплантированных осмотических насосов. LHуровней = Уровни лютеинизирующего гормона относительно исходного уровня у овариэктомированных крыс после 24-72 часов непрерывного введения через подкожный имплантат. Сноски: = Синтетический (т. Е. Не эндогенный ). = Атипичный утеротрофический эффект, достигающий плато в течение 48 часов (утеротрофия эстрадиола линейно продолжается до 72 часов). Источники: См. Шаблон. | |||||
2-Гидроксиэстрадиол представляет собой катехол эстроген и в этом отношении имеет некоторое структурное сходство с катехоламинами дофамином, норэпинефрин (норадреналин) и адреналин (адреналин). В соответствии с этим было обнаружено, что 2-гидроксиэстрадиол взаимодействует с системами катехоламинов. Известно, что стероид конкурирует с катехоламинами за связывание с катехол-O-метилтрансферазой и тирозингидроксилазой, а также за прямое и конкурентное ингибирование этих ферментов. Кроме того, было обнаружено, что 2-гидроксиэстрадиол замещает спиперон из D2рецептора примерно с 50% сродства дофамина, тогда как эстрадиол, эстрон и эстриол и их другие 2- гидроксилированные и 2- метоксилированные производные показали только слабое или незначительное ингибирование. Более того, было обнаружено, что 2-гидроксиэстрадиол связывается с α1-адренергическим рецептором с чуть более чем половиной сродства норэпинефрина. Однако, хотя это сродство сравнимо с аффинностью дофамина и норадреналина, тем не менее, они находятся в двузначном микромолярном диапазоне.
Было обнаружено, что 2-гидроксиэстрадиол увеличивает секрецию пролактина при введении внутривенно женщинам. Было отмечено, что это может происходить из-за связывания 2-гидроксиэстрадиола с рецептором D 2 и противодействия ему. Однако исследователи возражали против этой возможности, потому что она была отложена (на несколько часов) и имела относительно небольшую величину, тогда как установленные антагонисты рецептора D 2 быстро вызывают заметное повышение уровня пролактина. Исследователи также возражали против возможности того, что это было связано с ингибированием биосинтеза дофамина 2-гидроксиэстрадиолом, поскольку 2-гидроксиэстрон, который ингибирует тирозингидроксилазу аналогично 2-гидроксиэстрадиолу, не показал такого увеличение секреции пролактина. Исследователи пришли к выводу, что наиболее вероятным объяснением было то, что повышение было опосредовано эстрогенной активностью 2-гидроксиэстрадиола, поскольку аналогичные приросты уровней пролактина наблюдались и с эстрадиолом. В любом случае, эти данные опровергают идею основных взаимодействий 2-гидроксиэстрадиола с дофаминовой системой.
2-гидроксиэстрадиол, а также 2-гидроксиэстрон и 4 -гидроксиэстрадиол, может подвергаться метаболическому окислительно-восстановительному циклу с образованием свободных радикалов, таких как супероксид и реактивный эстроген семихинон / хинон промежуточные продукты. Эти метаболиты могут повреждать ДНК и другие клеточные компоненты. Однако 2-гидроксиэстрадиол проявляет небольшую канцерогенную активность или совсем не проявляет ее в отношении почки самцов сирийского хомячка, и есть доказательства того, что 2-гидроксиэстрадиол действительно может снижать онкогенез в чувствительных к эстрогену тканях. Было высказано предположение, что отсутствие туморогенеза 2-гидроксиэстрона связано с его быстрым клиренсом. Кроме того, его метаболит 2-метоксиэстрадиол является очень сильным ингибитором роста опухоли и ангиогенеза, и это тоже может вносить свой вклад.
2-Гидроксиэстрадиол было идентифицировано как пролекарство 2-метоксиэстрадиола, превращение, которое катализируется очень эффективно катехол-O-метилтрансферазой в печени. 2-Метоксиэстрадиол не является эстрогеном, но является мощным ингибитором ангиогенеза и агонистом GPER с потенциальным терапевтическим действием при раке.
Подобно другим стероидным эстрогенам, 2-гидроксиэстрадиол является антиоксидантом, но катехоловые эстрогены (2- и 4-гидроксилированные эстрогены), такие как 2-гидроксиэстрадиол, считаются наиболее мощными с точки зрения антиоксидантной активности.
2-Гидроксиэстрадиол был идентифицирован как метаболит эстрадиола в 1960 году.