| Ретровирусы | |
|---|---|
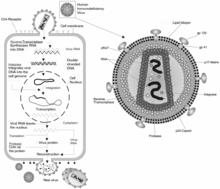 | |
| Схема клеточной инфекции, продуцирования вируса и структуры вируса ретровируса ВИЧ | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Царство: | Рибовирия |
| Королевство: | Парарнавиры |
| Тип: | Artverviricota |
| Класс: | Revtraviricetes |
| Порядок: | Ортервиралес |
| Семья: | Retroviridae |
| Подсемейства и роды | |
| |
Ретровирус является типом вируса, который вставляет копию своей РНК генома в ДНК из в клетке - хозяине, что он вторгается, изменяя тот самый ген этой клетки. Оказавшись внутри клетки-хозяина цитоплазме, вирус использует свой собственный обратной транскриптазы фермента для получения ДНК из ее РНК - генома, обратной обычной схеме, таким образом, ретро ( в обратном направлении). Затем новая ДНК включается в геном клетки-хозяина с помощью фермента интегразы, после чего ретровирусная ДНК называется провирусом. Затем клетка-хозяин обрабатывает вирусную ДНК как часть своего собственного генома, транскрибируя и транслируя вирусные гены вместе с собственными генами клетки, производя белки, необходимые для сборки новых копий вируса.
Хотя ретровирусы имеют разные подсемейства, у них есть три основные группы: онкоретровирусы (онкогенные ретровирусы), лентивирусы (медленные ретровирусы) и спумавирусы (пенистые вирусы). Онкоретровирусы могут вызывать рак у некоторых видов, лентивирусы могут вызывать тяжелый иммунодефицит и смерть у людей и других животных, а спумавирусы доброкачественны и не связаны с какими-либо заболеваниями у людей или животных.
Многие ретровирусы вызывают серьезные заболевания у людей, других млекопитающих и птиц. Ретровирусы человека включают ВИЧ-1 и ВИЧ-2, вызывающие заболевание СПИД. Кроме того, человеческий Т-лимфотропный вирус (HTLV) вызывает заболевание у людей. Вирусы мышиного лейкоза (MLV) вызывают рак у мышей-хозяев. Ретровирусы - ценные инструменты исследования в молекулярной биологии, и они успешно используются в системах доставки генов.
Вирионы, вирусы в виде независимых частиц ретровирусов, состоят из обволакивающих частиц диаметром около 100 нм. Внешняя липидная оболочка состоит из гликопротеина. Вирионы также содержат две идентичные одноцепочечные молекулы РНК длиной 7–10 тыс. Оснований. Две молекулы представлены в виде димера, образованного спариванием оснований между комплементарными последовательностями. Сайты взаимодействия между двумя молекулами РНК были идентифицированы как « целующаяся стебель-петля ». Хотя вирионы разных ретровирусов не имеют одинаковой морфологии или биологии, все компоненты вирионов очень похожи.
Основные компоненты вириона:
 Геномная и субгеномная организация прототипного ретровируса. Сокращения объясняются в описании файла.
Геномная и субгеномная организация прототипного ретровируса. Сокращения объясняются в описании файла. Ретровирусный геном упакован в виде вирусных частиц. Эти вирусные частицы представляют собой димеры одноцепочечных линейных молекул РНК с положительным смыслом.
Ретровирусы (и orterviruses в целом) следуют расположение 5'- затычки - про - Pol - ENV - 3' в РНК - генома. gag и pol кодируют полипротеины, каждый из которых управляет капсидом и репликацией. Область pol кодирует ферменты, необходимые для репликации вируса, такие как обратная транскриптаза, протеаза и интеграза. В зависимости от вируса гены могут перекрываться или сливаться в более крупные полипротеиновые цепи. Некоторые вирусы содержат дополнительные гены. Род лентивирусов, род спумавирусов, род HTLV / вирус лейкемии крупного рогатого скота (BLV) и недавно введенный род рыбьего вируса относятся к ретровирусам, классифицируемым как комплексные. Эти вирусы имеют гены, называемые вспомогательными генами, в дополнение к генам gag, pro, pol и env. Дополнительные гены расположены между pol и env, ниже env, включая U3-область LTR, или в env и перекрывающихся частях. Хотя вспомогательные гены выполняют вспомогательные функции, они также координируют и регулируют экспрессию вирусных генов. Кроме того, некоторые ретровирусы могут нести гены, называемые онкогенами, или гены онкогенов из другого класса. Ретровирусы с этими генами (также называемые трансформирующими вирусами) известны своей способностью быстро вызывать опухоли у животных и переводить клетки в культуре в онкогенное состояние.
Полипротеины расщепляются на более мелкие белки, каждый из которых выполняет свою функцию. Кодирующие их нуклеотиды известны как подгены.
 Ретровирус имеет мембрану, содержащую гликопротеины, которые способны связываться с рецепторным белком в клетке-хозяине. Внутри клетки есть две цепи РНК, содержащие три фермента: протеаза, обратная транскриптаза и интеграза (1). Первым этапом репликации является связывание гликопротеина с рецепторным белком (2). После связывания клеточная мембрана разрушается, становясь частью клетки-хозяина, и цепи РНК и ферменты попадают в клетку (3). Внутри клетки обратная транскриптаза создает комплементарную цепь ДНК из РНК ретровируса, и РНК разрушается; эта цепь ДНК известна как кДНК (4). Затем кДНК реплицируется, и две цепи образуют слабую связь и входят в ядро (5). Попадая в ядро, ДНК интегрируется в ДНК клетки-хозяина с помощью интегразы (6). Эта клетка может либо оставаться в спящем состоянии, либо РНК может быть синтезирована из ДНК и использована для создания белков для нового ретровируса (7). Единицы рибосомы используются для трансляции мРНК вируса в аминокислотные последовательности, которые могут быть преобразованы в белки грубого эндоплазматического ретикулума. На этом этапе также будут производиться вирусные ферменты и капсидные белки (8). Вирусная РНК будет производиться в ядре. Затем эти части собираются вместе и отщепляются от клеточной мембраны как новый ретровирус (9).
Ретровирус имеет мембрану, содержащую гликопротеины, которые способны связываться с рецепторным белком в клетке-хозяине. Внутри клетки есть две цепи РНК, содержащие три фермента: протеаза, обратная транскриптаза и интеграза (1). Первым этапом репликации является связывание гликопротеина с рецепторным белком (2). После связывания клеточная мембрана разрушается, становясь частью клетки-хозяина, и цепи РНК и ферменты попадают в клетку (3). Внутри клетки обратная транскриптаза создает комплементарную цепь ДНК из РНК ретровируса, и РНК разрушается; эта цепь ДНК известна как кДНК (4). Затем кДНК реплицируется, и две цепи образуют слабую связь и входят в ядро (5). Попадая в ядро, ДНК интегрируется в ДНК клетки-хозяина с помощью интегразы (6). Эта клетка может либо оставаться в спящем состоянии, либо РНК может быть синтезирована из ДНК и использована для создания белков для нового ретровируса (7). Единицы рибосомы используются для трансляции мРНК вируса в аминокислотные последовательности, которые могут быть преобразованы в белки грубого эндоплазматического ретикулума. На этом этапе также будут производиться вирусные ферменты и капсидные белки (8). Вирусная РНК будет производиться в ядре. Затем эти части собираются вместе и отщепляются от клеточной мембраны как новый ретровирус (9). Когда ретровирусы интегрировали свой собственный геном в зародышевую линию, их геном передается следующему поколению. Эти эндогенные ретровирусы (ERV), в отличие от экзогенных, в настоящее время составляют 5–8% генома человека. Большинство вставок не имеют известной функции и часто называются « мусорной ДНК ». Тем не менее, многие эндогенные ретровирусы играют важную роль в биологии хозяина, такие как контроль транскрипции гена, слияние клеток во время плацентарного развития в ходе прорастания в качестве зародыша, и устойчивости к экзогенной ретровирусной инфекции. Эндогенным ретровирусам также уделялось особое внимание при исследовании патологий, связанных с иммунологией, таких как аутоиммунные заболевания, такие как рассеянный склероз, хотя эндогенные ретровирусы еще не доказали, что играют какую-либо причинную роль в этом классе заболеваний.
В то время как классически считалось, что транскрипция происходит только от ДНК к РНК, обратная транскриптаза транскрибирует РНК в ДНК. Термин «ретро» в ретровирусе относится к этому обращению (создание ДНК из РНК) обычного направления транскрипции. Он по-прежнему подчиняется центральной догме молекулярной биологии, согласно которой информация может передаваться от нуклеиновой кислоты к нуклеиновой кислоте, но не может быть передана обратно от белка ни к белку, ни к нуклеиновой кислоте. Активность обратной транскриптазы за пределами ретровирусов была обнаружена почти у всех эукариот, что позволяет создавать и вставлять новые копии ретротранспозонов в геном хозяина. Эти вставки транскрибируются ферментами хозяина в новые молекулы РНК, которые попадают в цитозоль. Затем некоторые из этих молекул РНК транслируются в вирусные белки. Белки, кодируемые генами gag и pol, транслируются с мРНК длины генома в полипротеины Gag и Gag-Pol. Например, для гена gag ; он транслируется в молекулы капсидного белка и гена pol ; он транслируется в молекулы обратной транскриптазы. Ретровирусам требуется гораздо больше белков Gag, чем белков Pol, и они разработали передовые системы для синтеза необходимого количества каждого из них. Например, после синтеза Gag почти 95 процентов рибосом прекращают трансляцию, тогда как другие рибосомы продолжают трансляцию с синтезом Gag-Pol. В грубом эндоплазматическом ретикулуме начинается гликозилирование, и ген env транслируется из сплайсированных мРНК в грубом эндоплазматическом ретикулуме в молекулы белка оболочки. Когда молекулы белка оболочки переносятся в комплекс Гольджи, они разделяются протеазой хозяина на поверхностный гликопротеин и трансмембранный гликопротеин. Эти два продукта гликопротеина остаются в тесном родстве и транспортируются к плазматической мембране после дальнейшего гликозилирования.
Важно отметить, что ретровирус должен «вносить» свою собственную обратную транскриптазу в свой капсид, в противном случае он не сможет использовать ферменты инфицированной клетки для выполнения этой задачи из-за необычной природы получения ДНК из РНК.
Промышленные лекарственные препараты, разработанные как ингибиторы протеаз и обратной транскриптазы, производятся таким образом, что они нацелены на определенные участки и последовательности в пределах соответствующих ферментов. Однако эти препараты могут быстро стать неэффективными из-за того, что последовательности генов, кодирующие протеазу и обратную транскриптазу, быстро мутируют. Эти изменения в основаниях вызывают изменение определенных кодонов и сайтов с ферментами и, таким образом, предотвращают нацеливание лекарственного средства, теряя сайты, на которые лекарство фактически нацелено.
Поскольку в обратной транскрипции отсутствует обычная проверка репликации ДНК, ретровирус очень часто мутирует. Это позволяет вирусу быстро вырабатывать устойчивость к противовирусным фармацевтическим препаратам и препятствует разработке эффективных вакцин и ингибиторов ретровируса.
Одна трудность, с которой сталкиваются некоторые ретровирусы, такие как ретровирус Молони, заключается в том, что клетки должны активно делиться для трансдукции. В результате клетки, такие как нейроны, очень устойчивы к инфекции и трансдукции ретровирусами. Это вызывает опасения, что инсерционный мутагенез из-за интеграции в геном хозяина может привести к раку или лейкемии. Это отличается от лентивирусов, рода Retroviridae, которые способны интегрировать свою РНК в геном неделящихся клеток-хозяев.
Два генома РНК упакованы в каждую частицу ретровируса, но после заражения каждый вирус генерирует только один провирус. После заражения происходит обратная транскрипция, и этот процесс сопровождается рекомбинацией. Рекомбинация включает переключение цепи матрицы между двумя копиями генома (рекомбинация по выбору копии) во время обратной транскрипции. В каждом цикле репликации происходит от 5 до 14 событий рекомбинации на геном. Генетическая рекомбинация, по-видимому, необходима для поддержания целостности генома и в качестве механизма восстановления поврежденных геномов.
ДНК, образованная после обратной транскрипции (провирус), длиннее, чем геном РНК, потому что каждый из концов имеет последовательности U3 - R - U5, называемые длинным концевым повтором (LTR). Таким образом, 5 'терминал имеет дополнительную последовательность U3, а другой терминал имеет последовательность U5. LTR могут посылать сигналы для выполнения жизненно важных задач, таких как инициирование продукции РНК или управление скоростью транскрипции. Таким образом, LTR могут контролировать репликацию, а значит, и весь цикл вирусного цикла. Хотя неинтегрированная ретровирусная кДНК расположена в ядре, она является очень слабым субстратом для транскрипции. По этой причине интегрированный провирус необходим для постоянной и эффективной экспрессии ретровирусных генов.
Эта ДНК может быть включена в геном хозяина как провирус, который может передаваться дочерним клеткам. ДНК ретровируса случайным образом вставляется в геном хозяина. Из-за этого он может быть вставлен в онкогены. Таким образом, некоторые ретровирусы могут превращать нормальные клетки в раковые. Некоторые провирусы остаются латентными в клетке в течение длительного периода времени, прежде чем они активируются изменением клеточной среды.
Исследования ретровирусов привели к первому продемонстрированному синтезу ДНК из матриц РНК, фундаментальному способу передачи генетического материала, который встречается как у эукариот, так и у прокариот. Было высказано предположение, что процессы транскрипции РНК в ДНК, используемые ретровирусами, могли сначала привести к использованию ДНК в качестве генетического материала. В этой модели, гипотезе мира РНК, клеточные организмы приняли более химически стабильную ДНК, когда ретровирусы эволюционировали, чтобы создать ДНК из матриц РНК.
По оценкам даты эволюции пенистых эндогенных ретровирусов, время появления последнего общего предка было более 450 миллионов лет назад.
Были разработаны гаммаретровирусные и лентивирусные векторы для генной терапии, которые опосредуют стабильную генетическую модификацию обработанных клеток путем хромосомной интеграции геномов перенесенных векторов. Эта технология используется не только для исследовательских целей, но и для клинической генной терапии, направленной на долгосрочную коррекцию генетических дефектов, например, в стволовых клетках и клетках-предшественниках. Созданы ретровирусные векторные частицы с тропизмом к различным клеткам-мишеням. Гаммаретровирусные и лентивирусные векторы к настоящему времени использовались в более чем 300 клинических испытаниях, посвященных вариантам лечения различных заболеваний. Ретровирусные мутации могут быть разработаны для создания моделей трансгенных мышей для изучения различных видов рака и их метастатических моделей.
Ретровирусы, вызывающие рост опухоли, включают вирус саркомы Рауса и вирус опухоли молочной железы мышей. Рак может быть вызван протоонкогенами, ошибочно включенными в провирусную ДНК, или разрушением клеточных протоонкогенов. Вирус саркомы Рауса содержит ген src, запускающий образование опухоли. Позже было обнаружено, что в клеточной передаче сигналов участвует похожий ген в клетках, который, скорее всего, был вырезан с помощью провирусной ДНК. Нетрансформирующие вирусы могут случайным образом вставлять свою ДНК в протоонкогены, нарушая экспрессию белков, регулирующих клеточный цикл. Промотор ДНК провируса также может вызывать сверхэкспрессию регуляторных генов. Ретровирусы могут вызывать такие заболевания, как рак и иммунодефицит. Если вирусная ДНК интегрирована в хромосомы хозяина, это может привести к необратимым инфекциям. Поэтому важно выяснить реакцию организма на ретровирусы. Особенно экзогенные ретровирусы связаны с патогенными заболеваниями. Например, у мышей есть вирус опухоли молочной железы мыши (MMTV), который является ретровирусом. Этот вирус передается новорожденным мышам через грудное молоко. Мыши-носители вируса заболевают раком молочной железы из-за ретровируса в возрасте 6 месяцев. Кроме того, вирус лейкемии I (HTLV-1), обнаруженный в Т-клетках человека, был обнаружен у людей в течение многих лет. Подсчитано, что этот ретровирус вызывает лейкоз в возрасте от 40 до 50 лет. Он имеет воспроизводимую структуру, которая может вызывать рак. В дополнение к обычной последовательности гена ретровирусов HTLV-1 содержит четвертую область, PX. Эта область кодирует регуляторные белки Tax, Rex, p12, p13 и p30. Белок Tax запускает лейкемический процесс и организует транскрипцию всех вирусных генов в интегрированной провирусной ДНК HTLV.
 Филогения Retroviridae
Филогения Retroviridae Экзогенные ретровирусы - это инфекционные вирусы, содержащие РНК или ДНК, которые передаются от одного организма к другому. В системе классификации Балтимора, которая группирует вирусы вместе на основе их способа синтеза информационной РНК, они классифицируются на две группы: Группа VI: одноцепочечные РНК-вирусы с промежуточным звеном ДНК в их жизненном цикле, и Группа VII: двухцепочечные. ДНК-вирусы с промежуточной РНК в их жизненном цикле.
Все члены группы VI используют кодируемую вирусами обратную транскриптазу, РНК-зависимую ДНК-полимеразу, для получения ДНК из исходного генома РНК вириона. Эта ДНК часто интегрируется в геном хозяина, как в случае ретровирусов и псевдовирусов, где она реплицируется и транскрибируется хозяином.
В группу VI входят:
Семейство Retroviridae ранее было разделено на три подсемейства ( Oncovirinae, Lentivirinae и Spumavirinae), но теперь разделено на два: Orthoretrovirinae и Spumaretrovirinae. Термин онковирус в настоящее время широко используется для описания вируса, вызывающего рак. В это семейство сейчас входят следующие роды:
Обратите внимание, что согласно ICTV 2017, род Spumavirus был разделен на пять родов, и его прежний типовой вид обезьяньего пенистого вируса теперь повышен до рода Simiispumavirus с не менее чем 14 видами, включая новый типовой вид пенистого вируса обезьяны восточного шимпанзе.
У обоих семейств в Группе VII есть ДНК-геномы, содержащиеся внутри вторгающихся вирусных частиц. Геном ДНК транскрибируется как в мРНК для использования в качестве транскрипта в синтезе белка, так и в прегеномную РНК для использования в качестве матрицы во время репликации генома. Вирусно-кодируемая обратная транскриптаза использует пре-геномную РНК в качестве матрицы для создания геномной ДНК.
Группа VII включает:
Последнее семейство тесно связано с недавно предложенными
в то время как семейства Belpaoviridae, Metaviridae, Pseudoviridae, Retroviridae и Caulimoviridae составляют отряд Ortervirales.
Эндогенные ретровирусы формально не включены в эту систему классификации и в целом классифицируются на три класса на основе родства с экзогенными родами:
Антиретровирусные препараты - это лекарства для лечения ретровирусов, в первую очередь ВИЧ. Различные классы антиретровирусных препаратов действуют на разных этапах жизненного цикла ВИЧ. Комбинация нескольких (обычно трех или четырех) антиретровирусных препаратов известна как высокоактивная антиретровирусная терапия (ВААРТ).
Кошачий вирус лейкемии и вирус иммунодефицита Feline инфекции лечатся с биопрепаратами,том числе единственного иммуномодуляторанастоящее время лицензии на продажу в Соединенных Штатах, лимфоцит T-Cell иммуномодулятор (LTCI).