| Ротавирусный гастроэнтерит | |
|---|---|
 | |
| Ротавирус A из фекалий инфицированного ребенка | |
| Специальность | Инфекционные заболевания, педиатрия, интенсивная терапия |
Ротавирусный гастроэнтерит - наиболее частая причина тяжелой диареи среди младенцев и детей раннего возраста. Это вызвано ротавирусом, родом вируса с двухцепочечной РНК в семействе Reoviridae. К пяти годам почти каждый ребенок в мире хотя бы раз был инфицирован ротавирусом. Однако с каждой инфекцией иммунитет развивается, и последующие инфекции становятся менее тяжелыми; взрослые страдают редко. Существует пять видов этого вируса, обозначаемых как A, B, C, D и E. Ротавирус A, самый распространенный, вызывает более 90% инфекций у людей.
Вирус передается фекально-оральным путем. Он заражает и повреждает клетки, выстилающие тонкий кишечник, и вызывает гастроэнтерит (который часто называют «желудочным гриппом», несмотря на то, что он не имеет отношения к гриппу ). Хотя ротавирус был обнаружен в 1973 году и составляет до 50% госпитализаций по поводу тяжелой диареи у младенцев и детей, его значение до сих пор не широко известно в сообществе общественного здравоохранения, особенно в развивающихся странах. Помимо воздействия на здоровье человека, ротавирус также поражает животных и является патогеном домашнего скота.
Ротавирус обычно легко поддается лечению детским заболеванием, но во всем мире почти 500 000 детей в возрасте до пяти лет в возрасте до сих пор умирают от ротавирусной инфекции каждый год, и почти два миллиона человек серьезно заболевают. В Соединенных Штатах, до начала программы вакцинации против ротавируса, ротавирус вызывал около 2,7 миллиона случаев тяжелого гастроэнтерита у детей, почти 60 000 госпитализаций и около 37 смертей каждый год. Кампании общественного здравоохранения по борьбе с ротавирусом сосредоточены на обеспечении пероральной регидратационной терапии для инфицированных детей и вакцинации для предотвращения заболевания. Заболеваемость и тяжесть ротавирусных инфекций значительно снизились в странах, которые включили ротавирусную вакцину в свою обычную политику иммунизации детей.
Ротавирусный гастроэнтерит - заболевание от легкой до тяжелой степени, характеризующееся рвотой, водянистой диареей и субфебрильной лихорадкой. После заражения ребенка вирусом проходит инкубационный период около двух дней до появления симптомов. Симптомы часто начинаются с рвоты, за которой следует от четырех до восьми дней обильной диареи. Обезвоживание чаще встречается при ротавирусной инфекции, чем при большинстве инфекций, вызываемых бактериальными патогенами, и является наиболее частой причиной смерти, связанной с ротавирусной инфекцией.
Ротавирусная инфекция A может возникать в течение всей жизни: первое обычно вызывает симптомы, но последующие инфекции обычно легкие или бессимптомные, поскольку иммунная система обеспечивает некоторую защиту. Следовательно, частота симптоматических инфекций наиболее высока у детей в возрасте до двух лет и постепенно снижается к 45 годам. Инфекция у новорожденных детей, хотя и встречается часто, часто связана с легким или бессимптомным течением заболевания; наиболее серьезные симптомы, как правило, возникают у детей от шести месяцев до двух лет, пожилых людей и лиц с нарушением или отсутствием функций иммунной системы. Из-за иммунитета, приобретенного в детстве, большинство взрослых не восприимчивы к ротавирусу; гастроэнтерит у взрослых обычно имеет не ротавирусную причину, но бессимптомные инфекции у взрослых могут поддерживать передачу инфекции в обществе.
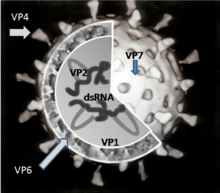 Упрощенная диаграмма расположения структурных белков ротавируса
Упрощенная диаграмма расположения структурных белков ротавируса Ротавирус передается фекально-оральным путем, через контакт с зараженными руками, поверхностями и предметами и, возможно, респираторным путем. Фекалии инфицированного человека могут содержать более 10 триллионов инфекционных частиц на грамм; менее 100 из них необходимы для передачи инфекции другому человеку.
Ротавирусы стабильны в окружающей среде и были обнаружены в лимане проб на уровне 1–5 инфекционных частиц на Галлон США. Санитарные меры, необходимые для уничтожения бактерий и паразитов, кажутся неэффективными в борьбе с ротавирусом, поскольку частота случаев ротавирусной инфекции в странах с высокими и низкими стандартами здравоохранения одинакова.
Существует пять видов ротавирусов, обозначаемых как A, B, C, D и E. Люди в основном заражаются видами A, B и C, чаще всего видами A. Все пять видов вызывают болезнь у других животных. Внутри ротавируса А существуют разные штаммы, называемые серотипами. Как и в случае вируса гриппа, используется двойная система классификации, основанная на двух белках на поверхности вируса. гликопротеин VP7 определяет серотипы G, а чувствительный к протеазе белок VP4 определяет серотипы P. Поскольку два гена, которые определяют G-тип и P-тип, могут передаваться по отдельности вирусам-потомкам, обнаруживаются разные комбинации.
Ротавирусы реплицируются в основном в кишечнике и заражают энтероциты ворсинок тонкой кишки, что приводит к структурным и функциональным изменениям эпителия. Тройная белковая оболочка делает их устойчивыми к кислому pH желудка и пищеварительным ферментам в кишечнике.
Вирус проникает в клетки посредством рецепторно-опосредованного эндоцитоза и образует везикулу, известную как эндосома. Белки в третьем слое (VP7 и шип VP4) разрушают мембрану эндосомы, создавая разницу в концентрации кальция. Это вызывает расщепление тримеров VP7 на отдельные белковые субъединицы, оставляя белковые оболочки VP2 и VP6 вокруг вирусной дцРНК, образуя двухслойную частицу (DLP).
Одиннадцать цепей дцРНК остаются в пределах защиты двух белковых оболочек, а вирусная РНК-зависимая РНК-полимераза создает транскрипты мРНК двухцепочечного вирусного генома. Оставаясь в ядре, вирусная РНК уклоняется от врожденных иммунных ответов хозяина, называемых РНК-интерференцией, которые запускаются присутствием двухцепочечной РНК.
Во время инфекции ротавирус продуцирует мРНК как для биосинтеза белка, так и для репликации гена. Большинство ротавирусных белков накапливаются в вироплазме, где реплицируется РНК и собираются DLP. Вироплазма образуется вокруг ядра клетки уже через два часа после заражения вирусом и состоит из вирусных фабрик, которые, как считается, состоят из двух вирусных неструктурных белков: NSP5 и NSP2. Ингибирование NSP5 с помощью РНК-интерференции приводит к резкому снижению репликации ротавируса. DLP мигрируют в эндоплазматический ретикулум, где они получают свой третий внешний слой (образованный VP7 и VP4). потомство вирусов высвобождается из клетки путем лизиса.
 Электронная микрофотография энтероцита, инфицированного ротавирусом (вверху), по сравнению с неинфицированной клеткой (внизу). Планка = прибл. 500 нм
Электронная микрофотография энтероцита, инфицированного ротавирусом (вверху), по сравнению с неинфицированной клеткой (внизу). Планка = прибл. 500 нм Диарея вызвана множественной активностью вируса. Мальабсорбция возникает из-за разрушения клеток кишечника, называемых энтероцитами. токсичный ротавирусный белок NSP4 индуцирует возрастную и кальций ион-зависимую секрецию хлорида, нарушает SGLT1 опосредованная транспортером реабсорбция воды, по-видимому, снижает активность мембраны щеточной каймы дисахаридаз и, возможно, активирует кальций-зависимую секреторную рефлексы кишечной нервной системы. Здоровые энтероциты секретируют лактазу в тонкий кишечник; непереносимость молока из-за лактазной недостаточности - симптом ротавирусной инфекции, которая может сохраняться в течение нескольких недель. Рецидив легкой диареи часто возникает после повторного включения молока в рацион ребенка из-за бактериальной ферментации дисахарида лактозы в кишечнике.
Диагностика ротавирусной инфекции обычно следует после диагноза гастроэнтерита как причины тяжелой диареи. Большинство детей, поступающих в больницу с гастроэнтеритом, проходят тестирование на ротавирус А. Специфический диагноз инфицирования ротавирусом А ставится при обнаружении вируса в стуле ребенка с помощью иммуноферментного анализа. На рынке имеется несколько лицензированных наборов тестов, которые чувствительны, специфичны и выявляют все серотипы ротавируса А. В исследовательских лабораториях используются другие методы, такие как электронная микроскопия и ПЦР. Полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР ) может обнаруживать и идентифицировать все виды и серотипы ротавируса человека.
Потому что улучшение санитарных условий не снижает распространенность ротавирусной болезни, и уровень госпитализаций остается высоким, несмотря на использование пероральных регидратирующих лекарств, основным вмешательством общественного здравоохранения является вакцинация. Две ротавирусные вакцины против инфекции ротавируса А безопасны и эффективны для детей: Rotarix от GlaxoSmithKline и RotaTeq от Merck. Обе вакцины принимаются перорально и содержат ослабленный живой вирус.
Ротавирусные вакцины лицензированы более чем в 100 странах, но только 17 стран внедрили плановую вакцинацию против ротавируса. После введения рутинной ротавирусной вакцинации в США в 2006 году бремя ротавирусного гастроэнтерита для здоровья «быстро и резко снизилось», несмотря на более низкие уровни охвата по сравнению с другими обычными прививками младенцев. Клинические испытания ротавирусной вакцины Rotarix в Южной Африке и Малави показали, что вакцина значительно снижает количество случаев тяжелой диареи, вызванной ротавирусом, и что инфекцию можно предотвратить с помощью вакцинации. В систематическом обзоре Cochrane за 2019 г., в котором участвовало 216 480 участников, были сделаны выводы о том, что вакцины RV1 (Rotarix), RV5 (RotaTeq) и Rotavac являются эффективными. Дополнительные ротавирусные вакцины находятся в стадии разработки. Всемирная организация здравоохранения (ВОЗ) рекомендует включить ротавирусную вакцину во все национальные программы иммунизации. Заболеваемость и тяжесть ротавирусных инфекций значительно снизились в странах, которые действовали в соответствии с этой рекомендацией.
Программа создания ротавирусных вакцин является результатом сотрудничества PATH, (ВОЗ) и США Центров по контролю и профилактике заболеваний и финансируется Альянсом ГАВИ. Программа направлена на сокращение детской заболеваемости и смертности от диарейных заболеваний за счет создания вакцины против ротавируса, доступной для использования в развивающихся странах.
Лечение острой ротавирусной инфекции неспецифично и включает лечение симптомов и, что наиболее важно, поддержание гидратации. При отсутствии лечения дети могут умереть от серьезного обезвоживания. В зависимости от тяжести диареи лечение состоит из пероральной регидратации, во время которой ребенку дают пить дополнительную воду, содержащую небольшое количество соли и сахара. Некоторые инфекции достаточно серьезны, чтобы потребовать госпитализации, когда жидкости вводятся внутривенно капельно или назогастральным зондом, а у ребенка электролиты и уровень сахара в крови контролируются. Не рекомендуются антибиотики.
Ротавирусные инфекции редко вызывают другие осложнения, и для хорошо воспитанного ребенка прогноз отличный.
 Сезонное изменение ротавирусной инфекции в регионе Англии: пик инфицирования приходится на зимние месяцы.
Сезонное изменение ротавирусной инфекции в регионе Англии: пик инфицирования приходится на зимние месяцы. Ротавирус А, на который приходится более 90% ротавирусных гастроэнтеритов у людей, эндемичен во всем мире. Ежегодно ротавирус вызывает миллионы случаев диареи в развивающихся странах, почти 2 миллиона случаев приводят к госпитализации и, по оценкам, 453 000 случаев смерти ребенка в возрасте до пяти лет. Это около 40 процентов всех госпитализаций, связанных с диареей у детей до пяти лет во всем мире.
Только в Соединенных Штатах - до начала программы вакцинации против ротавирусной инфекции - ежегодно регистрировалось более 2,7 миллиона случаев ротавирусного гастроэнтерита, 60 000 дети были госпитализированы, около 37 человек умерли от инфекции. Основная роль ротавируса в возникновении диареи не получила широкого признания в сообществе общественного здравоохранения, особенно в развивающихся странах. Почти каждый ребенок инфицирован ротавирусом к пяти годам. Это основная причина тяжелой диареи среди младенцев и детей, на нее приходится около 20% случаев и 50% случаев, требующих госпитализации. Ротавирус является причиной 37% смертей, связанных с диареей, и 5% всех смертей среди детей младше пяти лет. Мальчики в два раза чаще попадают в больницу, чем девочки. Ротавирусные инфекции возникают в основном в прохладное сухое время года. Число случаев заражения пищевых продуктов неизвестно.
Вспышки ротавируса Диарея часто встречается среди госпитализированных младенцев, маленьких детей, посещающих детские сады, и пожилых людей в домах престарелых. Вспышка заболевания, вызванная загрязненной городской водой, произошла в Колорадо в 1981 году. В 2005 году самая крупная зарегистрированная эпидемия диареи произошла в Никарагуа. Эта необычно крупная и серьезная вспышка была связана с мутациями в геноме ротавируса А, что, возможно, помогло вирусу избежать преобладающего иммунитета среди населения. Подобная крупная вспышка произошла в Бразилии в 1977 году.
Ротавирус B, также называемый ротавирусом диареи взрослых или ADRV, вызвал серьезные эпидемии тяжелой диареи, поразившие тысячи людей всех возрастов в Китае. Эти эпидемии возникли в результате загрязнения сточными водами питьевой воды. Инфекции ротавирусом B также произошли в Индии в 1998 году; причинный штамм был назван CAL. В отличие от ADRV, штамм CAL является эндемичным. На сегодняшний день эпидемии, вызванные ротавирусом B, ограничиваются материковым Китаем, и исследования указывают на отсутствие иммунитета к этому виду в Соединенных Штатах.
 Одна из оригинальных работ Флюетта. электронные микрофотографии
Одна из оригинальных работ Флюетта. электронные микрофотографии В 1943 году Джейкоб Лайт и Гораций Ходс доказали, что фильтруемый агент в фекалиях детей с инфекционной диареей также вызывает побои (диарею домашнего скота) у крупного рогатого скота. Спустя три десятилетия было показано, что сохранившиеся образцы возбудителя являются ротавирусом. В последующие годы было показано, что вирус у мышей связан с вирусом, вызывающим чистки. В 1973 году Рут Бишоп и его коллеги описали родственные вирусы, обнаруженные у детей с гастроэнтеритом.
В 1974 году Томас Генри Флюетт предложил название ротавирус, заметив, что при просмотре в электронном микроскопе частица ротавируса выглядит как колесо (rota на латыни); это название было официально признано Международным комитетом по таксономии вирусов четыре года спустя. В 1976 году родственные вирусы были описаны у нескольких других видов животных. Эти вирусы, вызывающие острый гастроэнтерит, были признаны коллективным патогеном, поражающим людей и животных во всем мире. Серотипы ротавирусов были впервые описаны в 1980 году, а в следующем году ротавирус от человека был впервые выращен в культурах клеток, полученных из почек обезьян, путем добавления трипсина (фермент, обнаруженный в двенадцатиперстной кишки млекопитающих и теперь известно, что он необходим для репликации ротавируса) в культуральную среду. Способность выращивать ротавирус в культуре ускорила темпы исследований, и к середине 1980-х первые вакцины-кандидаты проходили оценку.
В 1998 году ротавирусная вакцина была лицензирована для использования в Соединенные Штаты. Клинические испытания в США, Финляндии и Венесуэле показали его эффективность от 80 до 100% в предотвращении тяжелой диареи, вызванной ротавирусом А, и исследователи не обнаружили статистически значимых серьезных побочные эффекты. Однако производитель снял ее с рынка в 1999 году после того, как было обнаружено, что вакцина могла способствовать увеличению риска инвагинации, типа непроходимости кишечника, в одном из каждых 12000 вакцинированных младенцев. Этот опыт вызвал ожесточенные дискуссии об относительных рисках и преимуществах ротавирусной вакцины. В 2006 году было показано, что две новые вакцины против ротавирусной инфекции A безопасны и эффективны для детей, а в июне 2009 года Всемирная организация здравоохранения рекомендовала включить вакцинацию против ротавируса во все национальные программы иммунизации для обеспечения защиты от этой инфекции.
Ротавирусы инфицируют молодь многих видов животных и являются основной причиной диареи у диких и выращиваемых животных во всем мире. В качестве патогена домашнего скота, особенно молодых телят и поросят, ротавирусы причиняют фермерам экономические потери из-за затрат на лечение, связанных с высокими показателями заболеваемости и смертности. Эти ротавирусы являются потенциальным резервуаром для генетического обмена с ротавирусами человека. Имеются доказательства того, что ротавирусы животных могут инфицировать людей либо путем прямой передачи вируса, либо путем внесения одного или нескольких сегментов РНК в реассортанты с человеческими штаммами.
| Классификация | D |
|---|---|
| Внешние ресурсы |