| Лактаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Тетрамер лактазы, Э. coli Тетрамер лактазы, Э. coli | |||||||||
| Идентификаторы | |||||||||
| Номер EC | 3.2.1.108 | ||||||||
| Номер CAS | 9031-11-2 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
| Гликозилцерамидаза. (Флоризингидролаза) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 3.2.1.62 | ||||||||
| Номер CAS | 9033-10-7 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
| Лактаза | |
|---|---|
| Идентификаторы | |
| Символ | LCT |
| Альт. символы | LAC; LPH; LPH1 |
| ген NCBI | 3938 |
| HGNC | 6530 |
| OMIM | 603202 |
| RefSeq | NM_002299 |
| UniProt | P09848 |
| Прочие данные | |
| Номер ЕС | 3.2.1.108 |
| Locus | Chr. 2 q21 |
Лактаза представляет собой фермент, продуцируемый многими организмами. Он расположен в щеточной кайме тонкой кишки человека и других млекопитающих. Лактаза необходима для полного переваривания цельного молока ; он расщепляет лактозу, сахар, придающий молоку сладость. При недостатке лактазы человек, употребляющий молочные продукты, может испытывать симптомы непереносимости лактозы. Лактазу можно приобрести в качестве пищевой добавки, и ее добавляют в молоко для производства «безлактозных» молочных продуктов.
Лактаза (также известная как лактаза-флоризингидролаза или LPH ), часть семейства β-галактозидазы из ферменты, представляет собой гликозидгидролазу, участвующую в гидролизе дисахарида лактозы на составляющую галактозу и глюкозу мономеры. Лактаза присутствует преимущественно вдоль щеточной каймы мембраны дифференцированных энтероцитов, выстилающих ворсинки тонкой кишки. У людей лактаза кодируется геном LCT .
Лактаза - это фермент, который некоторые люди не могут производить в тонком кишечнике. Без него они не могут расщепить естественную лактозу в молоке, что приведет к диарее, газам и вздутию живота при употреблении обычного молока. Технология производства безлактозного молока, мороженого и йогурта была разработана Службой сельскохозяйственных исследований Министерства сельского хозяйства США в 1985 году. Эта технология используется для добавления лактазы в молоко, тем самым гидролизуя лактозу, содержащуюся в молоке. слегка сладкий, но легко усваиваемый. Без лактазы люди с непереносимостью лактозы передают непереваренную лактозу в толстую кишку, где бактерии расщепляют ее, создавая углекислый газ, что приводит к вздутию живота и метеоризму.
Добавки лактазы иногда используются для лечения непереносимости лактозы.
Коммерчески производимая лактаза может быть извлечена из дрожжей, например, Kluyveromyces fragilis и Kluyveromyces lactis, и плесневых грибов, таких как Aspergillus niger и Aspergillus oryzae. Его основное коммерческое использование в таких добавках, как Lacteeze и Lactaid, заключается в расщеплении лактозы в молоке, чтобы сделать его пригодным для людей с непереносимостью лактозы, однако США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов официально не оценивало эффективность этих продуктов.
Лактаза также используется для скрининга сине-белых колоний в сайтах множественного клонирования различных плазмидных векторов в Escherichia coli или других бактериях.
Оптимальная температура для лактазы человека составляет около 37 ° C, а оптимальная pH равно 6.
В метаболизме β-гликозидная связь в D -лактозе гидролизуется с образованием D <85.>-галактоза и D -глюкоза, которые могут всасываться через стенки кишечника и попадать в кровоток. Общая реакция, которую катализирует лактаза, представляет собой C 12H22O11+ H 2 O → C 6H12O6+ C 6H12O6+ тепло.
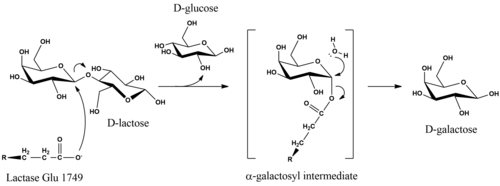
Каталитический механизм гидролиза D -лактозы сохраняет аномерную конфигурацию субстрата в продуктах. Хотя детали механизма неизвестны, стереохимическое удержание достигается за счет реакции двойного вытеснения. Исследования лактазы E. coli предположили, что гидролиз инициируется, когда глутаматный нуклеофил на фермент атакует с аксиальной стороны галактозильного углерода в β-гликозидной связи. Удаление уходящей группы D -глюкозы может быть облегчено с помощью Mg-зависимого кислотного катализа. Фермент высвобождается из α-галактозильной части при экваториальной нуклеофильной атаке водой, которая производит D-галактозу.
Исследования модификации субстрата показали, что 3'-OH и 2'- Фрагменты ОН в кольце галактопиранозы важны для ферментативного распознавания и гидролиза. 3'-гидроксигруппа участвует в начальном связывании с субстратом, тогда как 2'-группа не является необходимой для распознавания, но необходима на последующих этапах. Это демонстрируется тем фактом, что 2-дезокси-аналог является эффективным конкурентным ингибитором (K i = 10 мМ). Удаление определенных гидроксильных групп на фрагменте глюкопиранозы не устраняет полностью катализ.
Лактаза также катализирует превращение флоризина в флоретин и глюкозу.
Препролактаза, первичный продукт трансляции, имеет единственную первичную структуру полипептида, состоящую из 1927 аминокислот. Его можно разделить на пять доменов: (i) расщепленную 19 аминокислотами сигнальную последовательность ; (ii) большой домен пропоследовательности, которого нет в зрелой лактазе; (iii) зрелый лактазный сегмент; (iv) гидрофобный якорь, охватывающий мембраны; и (v) короткий гидрофильный карбоксильный конец. Сигнальная последовательность расщепляется в эндоплазматическом ретикулуме, и полученный 215-кДа про-LPH направляется в аппарат Гольджи, где он сильно гликозилируется и протеолитически процессируется до зрелой формы.. Было показано, что продомен действует как внутримолекулярный шаперон в ER, предотвращая расщепление трипсина и позволяя LPH принять необходимую трехмерную структуру для транспортировки в аппарат Гольджи.
 Схема процессинга и локализации продукта трансляции человеческой лактазы.
Схема процессинга и локализации продукта трансляции человеческой лактазы. Зрелая человеческая лактаза состоит из одной полипептидной цепи массой 160 кДа, которая локализуется на мембране щеточной каймы эпителиальных клеток кишечника. Он ориентирован с N-концом вне клетки и C-концом в цитозоле. LPH содержит два каталитических центра глутаминовой кислоты. В человеческом ферменте активность лактазы связана с Glu-1749, в то время как Glu-1273 является участком функции флоризингидролазы.
Лактаза кодируется одним генетический локус на хромосоме 2. Он экспрессируется исключительно энтероцитами тонкого кишечника млекопитающих и на очень низких уровнях в толстой кишке во время внутриутробного развития. Люди рождаются с высоким уровнем экспрессии лактазы. У большей части населения мира транскрипция лактазы снижается после отлучения от груди, что приводит к снижению экспрессии лактазы в тонком кишечнике, что вызывает общие симптомы гиполактазии взрослого типа или непереносимости лактозы.
Некоторые слои населения проявляют персистентность лактазы в результате мутации, которая, как предполагается, произошла 5 000–10 000 лет назад, что совпало с ростом приручения крупного рогатого скота. Эта мутация позволила почти половине населения мира бессимптомно метаболизировать лактозу. Исследования связывают возникновение персистенции лактазы с двумя разными однонуклеотидными полиморфизмами на расстоянии 14 и 22 килобаз перед 5’-концом гена LPH. Обе мутации, C → T в положении -13910 и G → A в положении -22018, были независимо связаны с персистенцией лактазы.
Промотор лактазы имеет длину 150 пар оснований и расположен прямо перед сайтом инициация транскрипции. Последовательность высококонсервативна у млекопитающих, что позволяет предположить, что критические регуляторы цис-транскрипции расположены поблизости. Идентифицированы Cdx-2, HNF-1α и GATA. как факторы транскрипции. Исследования начала гиполактазии показали, что, несмотря на полиморфизм, существует небольшая разница в экспрессии лактазы у младенцев, показывая, что мутации становятся все более актуальными в процессе развития. Регулируемые в процессе развития ДНК-связывающие белки могут подавлять транскрипцию или дестабилизировать транскрипты мРНК, вызывая снижение экспрессии LPH после отлучения.
| Викискладе есть материалы, связанные с лактазой. |