| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 1,3,5-триметилбензол | |||
| Другие имена Мезитилен SYM -Trimethylbenzene | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.278 | ||
| Номер ЕС | |||
| КЕГГ | |||
| PubChem CID | |||
| UNII | |||
| Номер ООН | 2325 | ||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | C 9 H 12 | ||
| Молярная масса | 120,19 г / моль | ||
| Появление | Прозрачная бесцветная жидкость | ||
| Запах | Самобытный, ароматный | ||
| Плотность | 0,8637 г / см 3 при 20 ° C | ||
| Температура плавления | -44,8 ° С (-48,6 ° F, 228,3 К) | ||
| Точка кипения | 164,7 ° С (328,5 ° F, 437,8 К) | ||
| Растворимость в воде | 0,002% (20 ° С) | ||
| Давление газа | 2 мм рт. Ст. (20 ° C) | ||
| Магнитная восприимчивость (χ) | -92,32 10 −6 см 3 / моль | ||
| Состав | |||
| Дипольный момент | 0,047 Д | ||
| Опасности | |||
| Паспорт безопасности | [1] | ||
| точка возгорания | 50 ° С; 122 ° F; 323 К | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (Допустимо) | никто | ||
| REL (рекомендуется) | TWA 25 частей на миллион (125 мг / м 3) | ||
| IDLH (Непосредственная опасность) | ND | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
Мезитилен или 1,3,5-триметилбензол представляет собой производное бензола с тремя метильными заместителями, расположенными симметрично вокруг кольца. Два других изомерных триметилбензола - это 1,2,4-триметилбензол (псевдокумол) и 1,2,3-триметилбензол (гемимеллитен). Все три соединения имеют формулу C 6 H 3 (CH 3) 3, которая обычно обозначается сокращенно C 6 H 3 Me 3. Мезитилен - бесцветная жидкость со сладким ароматным запахом. Это компонент каменноугольной смолы, которая является его традиционным источником. Это предшественник различных тонких химикатов. Мезитили группа (Mes) представляет собой заместитель с формулой С 6 Н 2 Me 3 и находится в различных других соединениях.
Мезитилен получают путь уравновешивания ксилола (или простого метиловый эфир алкилирования его) над твердым кислотным катализатором :
Тримеризации из ацетона с помощью альдольной конденсации, которая катализируется и обезвоженная с помощью серной кислоты дает смесь 1,3,5 и 1,2,4-триметилбензола.
Окисление мезитилена азотной кислотой дает тримезиновую кислоту C 6 H 3 (COOH) 3. С помощью диоксида марганца, более мягкий окислитель, 3,5-диметил бензальдегида образуется. Мезитилен окисляется трифторопераксусной кислотой с образованием мезитола (2,4,6-триметилфенола).
Мезитилен в основном используется в качестве предшественника 2,4,6-триметиланилина, предшественника красителей. Это производное получают селективным мононитрированием мезитилена, избегая окисления метильных групп.
Присадка и компонент некоторых газовых смесей (авиационных бензинов).
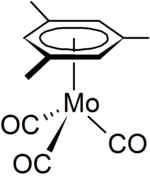 Структура (мезитилена) трикарбонила молибдена, [(η 6 -C 6 H 3 Me 3) Mo (CO) 3 ]
Структура (мезитилена) трикарбонила молибдена, [(η 6 -C 6 H 3 Me 3) Mo (CO) 3 ] Мезитилен используется в лаборатории как специальный растворитель. Он также может действовать как лиганд в металлоорганической химии, одним из примеров является органо-молибденовый комплекс [( η 6 -C 6 H 3 Me 3) Mo (CO) 3 ]. который может быть получен из гексакарбонила молибдена.
В электронной промышленности мезитилен использовался в качестве проявителя для силиконов с фотошаблонами из-за его свойств растворителя.
Три ароматических атома водорода мезитилена находятся в идентичных средах химического сдвига. Следовательно, они дают только один пик около 6,8 м.д. в спектре 1 H ЯМР ; то же самое верно и для девяти протонов метила, которые дают синглет около 2,3 частей на миллион. По этой причине мезитилен иногда используется в качестве внутреннего стандарта в образцах ЯМР, содержащих ароматические протоны.
Увитиновая кислота получается окислением мезитилена или конденсацией пировиноградной кислоты с баритовой водой.
Реакция гаттерман может быть упрощена путем замены HCN / AlCl 3 комбинации с цианидом цинка (Zn (CN) 2). Несмотря на высокую токсичность, Zn (CN) 2 является твердым веществом, поэтому работать с ним безопаснее, чем с газообразным цианистым водородом (HCN). Zn (CN) 2 реагирует с HCl с образованием основного реагента HCN и Zn (CN) 2, который служит катализатором на основе кислоты Льюиса на месте. Примером метода Zn (CN) 2 является синтез мезитальдегида из мезитилена.
Мезитилен был впервые получен в 1837 году ирландским химиком Робертом Кейном путем нагревания ацетона с концентрированной серной кислотой. Он назвал свое новое вещество «мезитилен», потому что немецкий химик Карл Райхенбах назвал ацетон «мезит» (от греческого μεσίτης, посредник), и Кейн полагал, что его реакция обезвоживала мезит, превращая его в алкен, «мезитилен». Однако определение Кейном химического состава («эмпирической формулы») мезитилена было неверным. Правильная эмпирическая формула была предоставлена Августом В. фон Хофманном в 1849 году. В 1866 году Адольф фон Байер показал, что структура мезитилена согласуется со структурой 1,3,5-триметилбензола; однако неопровержимое доказательство того, что мезитилен идентичен 1,3,5-триметилбензолу, было предоставлено Альбертом Ладенбургом в 1874 году.
Группа (CH 3) 3 C 6 H 2 - называется мезитил (символ органической группы: Mes). Производные мезитила, например тетрамезитилдиирон, обычно получают из реактива Гриньяра (CH 3) 3 C 6 H 2 MgBr. Из-за большой стерической потребности мезитильная группа используется в качестве большой блокирующей группы в асимметричном катализе (для повышения диастерео- или энантиоселективности) и в металлоорганической химии (для стабилизации металлических центров с низкой степенью окисления или с низким координационным числом). Более крупные аналоги с еще большей стерической потребностью, например 2,6-диизопропилфенил (Dipp) и аналогично названный Tripp (( i Pr) 3 C 6 H 2, Is) и супермеситил (( t Bu) 3 C 6 H 2, Mes *) группы, могут быть даже более эффективными в достижении этих целей.
Мезитилен также является одним из основных городских летучих органических соединений (ЛОС), образующихся при сгорании. Он играет важную роль в образовании аэрозолей и тропосферного озона, а также в других реакциях в химии атмосферы.