 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.008.331 |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | Zn (CN) 2 |
| Молярная масса | 117,444 г / моль |
| Внешний вид | бежевый порошок |
| Плотность | 1,852 г / см, твердое вещество |
| Точка плавления | 800 ° C (1470 ° F; 1070 K) (разлагается) |
| Растворимость в воде | 0,00005 г / 100 мл (20 ° C) |
| Растворимость | подвержена воздействию щелочей, KCN, аммиака |
| Магнитная восприимчивость (χ) | -46,0 · 10 см / моль |
| Опасности | |
| Классификация ЕС (DSD) (устаревшая) | не указана |
| NFPA 704 (огненный алмаз) |  0 3 0 0 3 0 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 100 мг / кг, крыса (внутрибрюшинно) |
| Ссылки ink | |
Цианид цинка неорганическое соединение формулы Zn (CN )2. Это белое твердое вещество, которое используется в основном для гальваники цинка, но также имеет более специализированные применения для синтеза органических соединений.
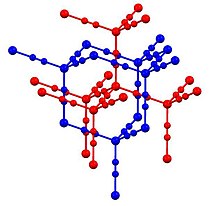
В Zn (CN) 2 цинк принимает тетраэдрическую координационную среду, все связаны посредством образования мостиков цианид лигандов. Структура состоит из двух «взаимопроникающих» структур (синяя и красная на рисунке выше). Такие мотивы иногда называют «расширенными алмазоидными структурами. Некоторые формы SiO 2 имеют аналогичную структуру, в которой тетраэдрические центры Si связаны оксидами. Цианидная группа демонстрирует беспорядок от головы к хвосту, когда любой атом цинка имеет от одного до четырех атомов углерода, а остальные являются атомами азота. Он показывает один из самых больших отрицательных коэффициентов теплового расширения (превышающий предыдущий рекордсмен, вольфрамат циркония ).
Типичный для неорганического полимера Zn (CN) 2 нерастворим в большинстве растворителей. Твердое вещество растворяется или, более точно, разлагается в водных растворах основных лигандов, таких как гидроксид, аммиак, и дополнительного цианида с образованием анионных комплексов.
Zn (CN) 2 довольно легко получить, комбинируя водные растворы цианида и ионов цинка, например, посредством реакции двойного замещения между KCN и ZnSO 4 :
В коммерческих приложениях некоторые попытки избежать примеси галогенидов с использованием ацетатных солей цинка:
Цианид цинка также производится как побочный продукт некоторых способов извлечения золота. Процедуры выделения золота из водного цианида золота иногда требуют добавления цинка:
Основное применение Zn (CN) 2 - это гальваника цинка из водных растворов, содержащих дополнительное количество цианида.
Zn (CN) 2 используется для введения группы формила в ароматические соединения в Реакция Гаттермана, где она служит удобной, более безопасной и негазообразной альтернативой HCN. Поскольку в реакции используется HCl, Zn (CN) 2 также обеспечивает реакцию in situ с ZnCl 2, кислотным катализатором Льюиса. Примеры использования Zn (CN) 2 таким образом включают синтез 2-гидрокси-1-нафтальдегида и мезитальдегида.
Zn (CN) 2 представляет собой также используется в качестве катализатора цианосилилирования альдегидов и кетонов.