 | |
 | |
| Идентификаторы | |
|---|---|
| Номер CAS |
|
| 3D модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.037.470 |
| Номер EC |
|
| Справочник Гмелина | 846955 |
| PubChem CID | |
| номер RTECS |
|
| UNII |
|
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Pro perties | |
| Химическая формула | Ba (OH) 2 |
| Молярная масса | 171,34 г / моль (безводный). 189,355 г / моль (моногидрат). 315,46 г / моль (октагидрат) |
| Внешний вид | белое твердое вещество |
| Плотность | 3,743 г / см (моногидрат). 2,18 г / см (октагидрат, 16 ° C) |
| Температура плавления | 78 ° C ( 172 ° F; 351 K) (октагидрат). 300 ° C (моногидрат). 407 ° C (безводный) |
| Точка кипения | 780 ° C (1440 ° F; 1050 K) |
| Растворимость в воде | масса BaO (не Ba (OH) 2):. 1,67 г / 100 мл (0 ° C). 3,89 г / 100 мл (20 ° C). 4,68 г / 100 мл (25 ° C). 5,59 г / 100 мл (30 ° C). 8,22 г / 100 мл (40 ° C). 11,7 г / 100 мл (50 ° C). 20,94 г / 100 мл (60 ° C). 101,4 г / 100 мл (100 ° C) |
| Растворимость в других растворителях | низкая |
| Основность (pK b) | 0,15 (первый OH), 0,64 (второй OH) |
| Магнитная восприимчивость (χ) | -53,2 · 10 см / моль |
| Показатель преломления (nD) | 1,50 (октагидрат) |
| Структура | |
| Кристаллическая структура | октаэдрическая |
| Термохимия | |
| Стандартная энтальпия образования. (ΔfH298) | -944,7 кДж / моль |
| Опасности | |
| Паспорт безопасности | См. : страница данных |
| пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H302, H314, H318, H332, H412 |
| NFPA 704 (огненный алмаз) |  0 3 0 0 3 0 |
| Температура вспышки | Негорючие |
| Родственные соединения | |
| Прочие анионы | Оксид бария. Пероксид бария |
| Прочие катионы | Гидроксид кальция. Гидроксид стронция |
| Дополнительный страница данных | |
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. д. |
| Термодинамические. данные | Фаза поведение. твердое тело – жидкость – газ |
| Спектральные данные | UV, IR, ЯМР, MS |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [ 77 ° F], 100 кПа). | |
| Ссылки в ink | |
Гидроксид бария - это химическое соединение с химическая формула Ba (OH) 2(H2O)x. Моногидрат (x = 1), известный как барита или барита-вода, является одним из основных соединений бария. Этот белый гранулированный моногидрат является обычной коммерческой формой.
Гидроксид бария можно получить растворением оксида бария (BaO) в воде:
Он кристаллизуется в виде октагидрата, который превращается в моногидрат при нагревании на воздухе. При 100 ° C в вакууме моногидрат будет давать BaO и воду. Моногидрат имеет слоистую структуру (см. Рисунок выше). Центры Ва имеют квадратную антипризматическую геометрию. Каждый центр Ba связан с двумя водными лигандами и шестью гидроксидными лигандами, которые соответственно имеют двойные и тройные мостиковые соединения с соседними центрами Ba. В октагидрате отдельные центры Ba снова имеют восемь координат, но не имеют общих лигандов.
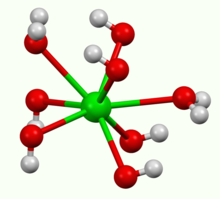 Координационная сфера вокруг отдельного иона бария в Ba (OH) 2.H2O.
Координационная сфера вокруг отдельного иона бария в Ba (OH) 2.H2O.В промышленности гидроксид бария используется в качестве предшественник других соединений бария. Моногидрат используется для обезвоживания и удаления сульфата из различных продуктов. В этом приложении используется очень низкая растворимость сульфата бария. Это промышленное применение также применяется в лабораторных условиях.
Гидроксид бария используется в аналитической химии для титрования слабых кислот, в частности органические кислоты. Его прозрачный водный раствор гарантированно не содержит карбоната, в отличие от растворов гидроксида натрия и гидроксида калия, поскольку карбонат бария нерастворим в воде. Это позволяет использовать такие индикаторы, как фенолфталеин или тимолфталеин (со щелочным изменением цвета) без риска ошибок титрования из-за присутствия ионов карбоната, которые являются гораздо менее основными.
Гидроксид бария иногда используется в органическом синтезе в качестве сильного основания, например, для гидролиза сложных эфиров и нитрилов, и в качестве основания в альдольной конденсации.


Его использовали для гидролиза одной из двух эквивалентных сложноэфирных групп в диметилгендекандиоате.
Гидроксид бария также используется при декарбоксилировании аминокислот с высвобождением карбоната бария в процессе.
Он также используется при получении циклопентанона, диацетонового спирта и.

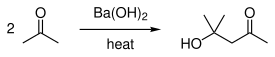
Гидроксид бария разлагается до оксида бария при нагревании до 800 ° C. Реакция с диоксидом углерода дает карбонат бария. Его водный раствор, будучи сильно щелочным, вступает в реакцию нейтрализации кислотами. Таким образом, он образует сульфат бария и с серной и фосфорной кислотами соответственно. Реакция с сероводородом дает сульфид бария. Осаждение многих нерастворимых или менее растворимых солей бария может быть результатом реакции двойного замещения, когда водный раствор гидроксида бария смешивают со многими растворами солей других металлов.
Реакции гидроксида бария с аммонием соли сильно эндотермичны. Реакция октагидрата гидроксида бария с хлоридом аммония или тиоцианатом аммония часто используется в качестве демонстрации химии в классе, обеспечивая температуру, достаточно низкую, чтобы заморозить воду, и достаточное количество воды для растворения полученной смеси.
Гидроксид бария представляет те же опасности, что и другие сильные основания, а также другие водорастворимые соединения бария: он агрессивен и токсичен.