 | |
 | |
| Имена | |
|---|---|
| Название IUPAC барий пероксид | |
| Другие названия Биноксид бария,. Диоксид бария | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.754 |
| Номер EC |
|
| PubChem CID | |
| RTECS номер |
|
| UNII | |
| Номер ООН | 1449 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | BaO 2 |
| Молярная масса | 169,33 г / моль ( безводный). 313,45 (октагидрат) |
| Внешний вид | Серо-белый кристаллический (безводный). бесцветное твердое вещество (октагидрат) |
| Запах | без запаха |
| Плотность | 5,68 г / см (безводный) 2,292 г / см (октагидрат) |
| Точка плавления | 450 ° C (842 ° F; 723 K) |
| Точка кипения | 800 ° C (1470 ° F; 1070 K) (разлагается до BaO O2.) |
| Растворимость в воде | безводный 0,091 г / 100 мл (20 ° C). октагидрата 0,168 г / см |
| Растворимость | растворяется с разложением в кислоте |
| Магнитная восприимчивость (χ) | -40,6 · 10 см / моль |
| Структура | |
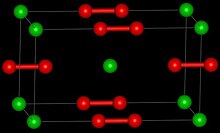
| Кристаллическая структура | Тетрагональная |
| Пространственная группа | D4h, I4 / mmm, tI6 |
| Координационная геометрия | 6 |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнал GHS word | Предупреждение |
| Краткая характеристика опасности GHS | H272, H302, H332 |
| Меры предосторожности GHS | P210, P220, P221, P261, P264, P270, P271, P280, P301 + 312, P304 + 312, P304 + 340, P312, P330, P370 + 378, P501 |
| NFPA 704 (огненный алмаз) |  0 2 2 OX 0 2 2 OX |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии ( при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Пероксид бария - это неорганическое соединение с формулой Ba O2. Это белое твердое вещество (серое в случае загрязнения) является одним из наиболее распространенных неорганических пероксидов, и это было первое обнаруженное пероксидное соединение. Являясь окислителем и при воспламенении дает ярко-зеленый цвет (как и все соединения бария), он находит некоторое применение в фейерверках ; исторически он также использовался в качестве прекурсора для перекиси водорода.
Пероксид бария представляет собой пероксид, содержащий субъединицы O. 2. Твердое вещество является изоморфным карбидом кальция, CaC 2.
Пероксид бария возникает в результате обратимой реакции O 2 с оксид бария. Пероксид образуется при температуре около 500 ° C, а кислород выделяется при температуре выше 820 ° C.
Эта реакция является основой для устаревшего сейчас Brin процесс отделения кислорода от атмосферы. Другие оксиды, например Na 2 O и SrO ведут себя аналогичным образом.
В другом устаревшем применении пероксид бария когда-то использовался для получения пероксида водорода посредством его реакции с серной кислотой:
Нерастворимый сульфат бария отфильтровывают из смеси.