 | |
 | |
 | |
| Названия | |
|---|---|
| Предпочтительное название IUPAC Ацетилид кальция | |
| Систематический IUPAC имя Этиндиид кальция | |
| Другие названия Перкарбид кальция. Карбид кальция. Дикарбид кальция | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.000.772 |
| Номер EC |
|
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | CaC 2 |
| Молярная масса | 64,099 г / моль |
| Внешний вид | От белого порошка до серых / черных кристаллов |
| Плотность | 2,22 г / см |
| Температура плавления | 2160 ° C (3920 ° F; 2430 K) |
| Точка кипения | 2300 ° C (4170 ° F; 2570 K) |
| Растворимость в воде | Быстрый гидролиз |
| Структура | |
| Кристаллическая структура | Тетрагональная |
| Пространство группа | D4h, I4 / mmm, tI6 |
| Координационная геометрия | 6 |
| Термохимия | |
| Стандартная молярная. энтропия (S 298) | 70 Дж · моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −63 кДж · моль |
| Опасности | |
| Основные опасности | Реагирует с водой с выделением ацетилена газа |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H260 |
| NFPA 704 (огненный алмаз) |  4 1 2 4 1 2 |
| Самовоспламенение. температура | 305 ° C (581 ° F; 578 K) (ацетилен) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа | |
| Ссылки в ink | |
Карбид кальция, также известный как ацетилид кальция, представляет собой химическое соединение с химической формулой из Ca C2. Его основное промышленное применение - производство Содержание ацетилена и цианамида кальция.
Чистый материал бесцветен, однако куски карбида кальция технической чистоты серого или коричневого цвета и состоят примерно на 80–85%. CaC 2 (остальное - CaO (оксид кальция ), Ca 3P2(фосфид кальция ), CaS (сульфид кальция ), Ca 3N2(нитрид кальция ), SiC (карбид кремния ) и т. Д.). В присутствии следов влаги технический карбид кальция издает неприятный запах, напоминающий запах чеснока.
Применение карбида кальция включает производство газа ацетилена, а также для производства ацетилена в карбидные лампы ; производство химикатов для удобрений; и в сталеплавильном производстве.
Карбид кальция получают промышленным способом в электродуговой печи из смеси извести и кокс приблизительно при 2200 ° C (3990 ° F). Это эндотермическая реакция, требующая 110 килокалорий (460 кДж) на моль и высоких температур для удаления монооксида углерода. Этот метод не изменился с момента его изобретения в 1892 году:
Высокая температура, необходимая для этой реакции, практически недостижима при традиционном сжигании, поэтому реакция выполняется в дуговой электропечи с электродами графит. Полученный карбидный продукт обычно содержит около 80% карбида кальция по весу. Карбид измельчается, чтобы получить небольшие комочки размером от нескольких до 50 мм. Примеси концентрируются в более мелких фракциях. Содержание CaC 2 в продукте определяют путем измерения количества ацетилена, образующегося при гидролизе. Например, британские и немецкие стандарты содержания более крупных фракций составляют 295 л / кг и 300 л / кг соответственно (при давлении 101 кПа и температуре 20 ° C (68 ° F)). Примеси, присутствующие в карбиде, включают фосфид, который при гидролизе дает фосфин.
Эта реакция была важной частью промышленной революции в химии и стала возможной в Соединенные Штаты в результате огромного количества недорогой гидроэлектроэнергии, производимой на Ниагарском водопаде до начала 20-го века.
Метод производства в дуговая печь была открыта в 1892 году Т. Л. Уилсон и независимо Х. Муассан в том же году. В Боснии и Герцеговине город Яйце австрийский промышленник доктор Йозеф Кранц и его компания «Bosnische-Elektrizitäts AG», преемником которой впоследствии стала «Электро-Босна», открыли крупнейший химический завод. завод по производству карбида кальция в то время в Европе в 1899 году. Гидроэлектростанция на реке Плива с установленной мощностью 8 МВт была построена для электроснабжения завода. Это была первая электростанция такого типа в Юго-Восточной Европе, которая была введена в эксплуатацию 24 марта 1899 года.
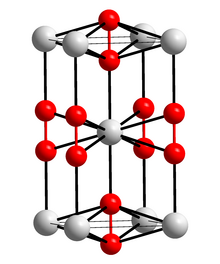
Чистый карбид кальция представляет собой бесцветное твердое вещество. Обычной кристаллической формой при комнатной температуре является искаженная структура каменной соли с параллельными блоками C 2.
Реакция карбида кальция с водой с образованием ацетилена и гидроксида кальция была открыта Фридрихом Велером в 1862 году.
Эта реакция легла в основу промышленного производства ацетилена и является основным промышленным применением карбида кальция.
Сегодня ацетилен в основном производится путем частичного сжигания метана или появляется как побочный продукт в потоке этилена при крекинге углеводородов. Таким образом ежегодно производится около 400 000 тонн (см. Получение ацетилена ).
В Китае ацетилен, полученный из карбида кальция, остается сырьем для химической промышленности, в частности для производства поливинилхлорида. Ацетилен местного производства более экономичен, чем использование импортного масла. Производство карбида кальция в Китае увеличивается. В 2005 году объем производства составил 8,94 миллиона тонн при мощности производства 17 миллионов тонн.
В США, Европе и Японии потребление карбида кальция в целом сокращается. Уровень производства в США в 1990-е годы составлял 236 000 тонн в год.
Карбид кальция реагирует с азотом при высокой температуре с образованием цианамида кальция :
Цианамид кальция, обычно известный как нитролим, используется в качестве удобрения. Гидролизуется до цианамида, H 2 NCN.
Используется карбид кальция:
 Горит карбидные лампы
Горит карбидные лампы Карбид кальция используется в карбидных лампах. При попадании капель воды на карбид образуется газ ацетилен, который горит и дает свет. Хотя эти лампы давали более ровный и яркий свет, чем свечи, они были опасны в угольных шахтах, где горючий метан газ представлял серьезную опасность. Присутствие горючих газов в угольных шахтах привело к появлению горняков аварийных ламп, таких как лампа Дэви, в которой проволочная сетка снижает риск воспламенения метана. Карбидные лампы по-прежнему широко использовались на рудниках сланца, меди и олова, где метан не представляет серьезной опасности. Большинство горняков заменено электрическими лампами.
Карбидные лампы по-прежнему используются для добычи полезных ископаемых в некоторых менее богатых странах, например, на серебряных рудниках около Потоси, Боливия. Карбидные лампы до сих пор используются некоторыми спелеологами, исследующими пещеры и другие подземные области, хотя их все чаще заменяют светодиодными лампами.
Карбидные лампы также широко использовались в качестве фар в ранних автомобилях, мотоциклах и велосипедах, но были полностью заменены электрическими лампами.
Карбид кальция иногда используется в качестве источника газообразного ацетилена, который является агентом созревания, аналогичным этилену. Однако в некоторых странах это является незаконным, поскольку при производстве ацетилена из карбида кальция загрязнение часто приводит к образованию следов фосфина и арсина. Эти примеси можно удалить, пропустив газообразный ацетилен через подкисленный раствор сульфата меди, но в развивающихся странах этой мерой предосторожности часто пренебрегают.
Карбид кальция используется в игрушечных пушках, таких как Big-Bang Cannon, а также в бамбуковых пушках. В Нидерландах карбид кальция используется в преддверии Нового года для стрельбы из бидонов.
Карбид кальция вместе с фосфидом кальция используется в плавающих самовоспламеняющихся морских сигнальных ракетах ., например, производимые Ассоциацией защиты морской флоры и фауны Холмса..
Карбид кальция используется для определения влажности почвы. Когда почва и карбид кальция смешиваются в закрытом цилиндре под давлением, содержание воды в почве вступает в реакцию с карбидом кальция с выделением ацетилена, давление которого можно измерить для определения содержания влаги.