 | |
 | |
| Имена | |
|---|---|
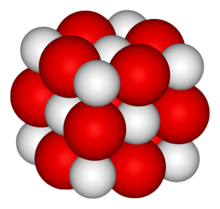
| Название IUPAC Оксид кальция | |
| Другие названия Негашеная известь, негашеная известь, галька, кальций | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.013.763 |
| Номер EC |
|
| E номер | E529 (регуляторы кислотности,...) |
| Ссылка на Гмелин | 485425 |
| KEGG | |
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1910 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | CaO |
| Молярная масса | 56,0774 г / моль |
| Внешний вид e | Порошок от белого до бледно-желтого / коричневого |
| Запах | Без запаха |
| Плотность | 3,34 г / см |
| Точка плавления | 2613 ° C (4735 ° F; 2886 K) |
| Точка кипения | 2850 ° C (5160 ° F; 3120 K) (100 гПа ) |
| Растворимость в воде | Реагирует с образованием гидроксида кальция |
| Растворимость в Метаноле | Нерастворим (также в диэтиловом эфире, октаноле ) |
| Кислотность (pK a) | 12,8 |
| Магнитная восприимчивость (χ) | -15,0 × 10 см / моль |
| Структура | |
| Кристаллическая структура | Кубическая, cF8 |
| Термохимия | |
| Стандартная молярная. энтропия (S 298) | 40 Дж · моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −635 кДж · моль |
| Фармакология | |
| Код ATCvet | QP53AX18 (ВОЗ ) |
| Опасности | |
| Паспорт безопасности | Hazard.com |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H302, H314, H315, H318, H335 |
| Меры предосторожности GHS | P260, P261, P264, P270, P271, P280, P301 + 312, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P312, P321, P330, P332 + 313, P362, P363, P403 + 233, P405, P501 |
| NFPA 704 (огонь алмаз) |  0 3 2 0 3 2 |
| Температура вспышки | Невоспламеняющийся |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 5 мг / м |
| REL (рекомендуется) | TWA 2 мг / м |
| IDLH (непосредственная опасность) | 25 мг / м |
| Родственные соединения | |
| Другие анионы | Сульфид кальция. Гидроксид кальция. Селенид кальция. |
| Прочие катионы | Оксид бериллия. Оксид магния. Оксид стронция. Оксид бария. |
| Если не указано иное, данные являются приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Оксид кальция (CaO ), широко известная как негашеная известь или негашеная известь, является широко используемым химическим соединением . Это белое щелочное, щелочное, кристаллическое твердое вещество при комнатной температуре. Широко используемый термин «известь » означает кальцийсодержащие неорганические материалы, в которых преобладают карбонаты, оксиды и гидроксиды кальция, кремния, магния, алюминия и железа. Напротив, негашеная известь относится к единственному химическому соединению оксиду кальция. Оксид кальция, который выживает при переработке и не вступает в реакцию со строительными материалами, такими как цемент, называется известь без содержания .
Негашеная известь является относительно недорогой. И он, и его химическое производное (гидроксид кальция, из которого негашеная известь является основным ангидридом ) являются важными товарными химическими веществами.
Оксид кальция обычно получают в результате термического разложения материалов, таких как известняк или ракушки, которые содержат карбонат кальция (CaCO 3 ; минерал кальцит ) в печи для обжига извести. Это достигается путем нагревания материала до температуры выше 825 ° C (1517 ° F), процесса, называемого прокаливание или обжигание извести, для высвобождения молекулы диоксида углерода (CO 2), оставив негашеную известь.
Негашеная известь нестабильна и при охлаждении самопроизвольно реагирует с CO 2 из воздуха до тех пор, пока, по прошествии определенного времени, он полностью не превратится обратно в карбонат кальция, если его не гашить водой до состояния известковой штукатурки или извести раствор.
Ежегодное мировое производство негашеной извести составляет около 283 миллионов тонн. Китай, безусловно, является крупнейшим производителем в мире с общим объемом производства около 170 миллионов тонн в год. Следующими по величине являются Соединенные Штаты - около 20 миллионов тонн в год.
На 1 тонну негашеной извести требуется примерно 1,8 т известняка. Негашеная известь имеет высокое сродство к воде и является более эффективным осушителем, чем силикагель. Реакция негашеной извести с водой связана с увеличением объема по крайней мере в 2,5 раза.
 Play media Демонстрация гашения негашеной извести как сильно экзотермической реакции. К кусочкам негашеной извести добавляют капли воды. Через некоторое время происходит выраженная экзотермическая реакция («гашение извести»). Температура может достигать примерно 300 ° C (572 ° F).
Play media Демонстрация гашения негашеной извести как сильно экзотермической реакции. К кусочкам негашеной извести добавляют капли воды. Через некоторое время происходит выраженная экзотермическая реакция («гашение извести»). Температура может достигать примерно 300 ° C (572 ° F). В 80 г. до н.э. римский полководец Серторий развернули удушающие облака едкого известкового порошка, чтобы победить чаразитани из Испании, укрывшихся в недоступных пещерах. Подобная пыль использовалась в Китае для подавления вооруженного крестьянского восстания в 178 году нашей эры, когда известняковые колесницы, оснащенные мехами, выдували известняковый порошок в толпы.
Считается, что негашеная известь была составной частью греческой культуры. огонь. При контакте с водой негашеная известь повысит свою температуру выше 150 ° C (302 ° F) и воспламенит топливо.
Дэвид Хьюм в своей Истории Англии рассказывает об этом в начале Во время правления Генриха III, английский флот уничтожил вторгшийся французский флот, ослепив вражеский флот негашеной известью. Негашеная известь, возможно, использовалась в средневековой морской войне - вплоть до использования «известковых мин», чтобы бросать ее во вражеские корабли.
Известняк заменяет известь во многих областях применения, которые включают сельское хозяйство, флюсование и удаление серы. Известняк, который содержит меньше реактивного материала, медленнее реагирует и может иметь другие недостатки по сравнению с известью, в зависимости от области применения; однако известняк значительно дешевле, чем известь. Кальцинированный гипс - альтернативный материал в промышленных штукатурках и растворах. Цемент, цементная пыль, летучая зола и известковая пыль являются потенциальными заменителями некоторых строительных применений извести. Гидроксид магния является заменителем извести при контроле pH, а оксид магния - заменителем доломитовой извести в качестве флюса в сталеплавильном производстве.
Из-за интенсивной реакции негашеной извести с водой возникает негашеная известь. сильное раздражение при вдыхании или контакте с влажной кожей или глазами. Вдыхание может вызвать кашель, чихание, затрудненное дыхание. Затем он может перерасти в ожоги с перфорацией носовой перегородки, болью в животе, тошнотой и рвотой. Хотя негашеная известь не считается пожароопасной, ее реакция с водой может выделять достаточно тепла для воспламенения горючих материалов.
| На Викискладе есть материалы, связанные с Оксид кальция. |