Войти
 | |
| Имена | |
|---|---|
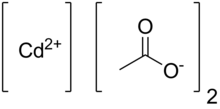
| Название IUPAC Ацетат кадмия | |
| Другие названия Диацетат кадмия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) |
|
| ChemSpider | |
| ECHA Info Карта | 100.008.049 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 2570 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | Cd (CH 3 COO) 2 (безводный). Cd (CH 3 COO) 2 · 2H 2 O (дигидрат) |
| Молярная масса | 230,500 г / моль (безводный). 266,529 г / моль (дигидрат) |
| Внешний вид | бесцветные кристаллы (безводные). белые кристаллы (дигидрат) |
| Запах | уксусная кислота |
| Плотность | 2,341 г / см (безводный). 2,01 г / см (дигидрат) |
| Температура плавления | 255 ° C (491 ° F; 528 K) (безводный) дигидрат разлагается при 130 ° C |
| Растворимость в воде | растворим (безводный), очень растворим (дигидрат) |
| Растворимость | растворим в метаноле, этанол (безводный). растворим в этаноле (дигидрат) |
| Магнитная восприимчивость (χ) | -83,7 · 10 см / моль |
| Структура | |
| Кристаллическая структура | моноклинная |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
| Краткая характеристика опасности GHS | H302, H312, H332, H400, H410 |
| Меры предосторожности GHS | P261, P264, P270, P271, P273, P280, P301 + 312, P302 + 352, P304 + 312, P304 + 340, P312, P322, P330, P363, P391, P501 |
| NFPA 704 (огненный алмаз) |  1 3 0 1 3 0 |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимо) | [1910.1027] TWA 0,005 мг / м (как Cd) |
| REL (рекомендуется) | Ca |
| IDLH (Немедленно da число) | Ca [9 мг / м (в виде Cd)] |
| Родственные соединения | |
| Другие анионы | Фторид кадмия. Хлорид кадмия. Бромид кадмия. Иодид кадмия |
| Другие катионы | Ацетат цинка. Ацетат ртути (II). Ацетат серебра |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Ацетат кадмия - это химическое соединение по формуле Cd (CH3CO2 )2. Это бесцветное твердое вещество классифицируется координационным полимером, содержащим ацетатные лиганды, соединяющие центры кадмия. Соединение существует в безводной форме и в виде дигидрата. Он образуется при обработке оксида кадмия уксусной кислотой :
Ацетат кадмия используется для глазурования керамики и керамика ; в гальванических ваннах, в крашении и печати текстильных изделий; и в качестве аналитического реагента для серы, селена и теллура.
ацетат кадмия получают обработкой оксид кадмия с уксусной кислотой. Соединение также может быть получено обработкой нитрата кадмия уксусным ангидридом.
Соединения кадмия считаются канцерогенами группы 1 согласно IARC.
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | He | ||||||||||||||||||
| LiOAc | Be (OAc) 2. BeAcOH | AcOAc. ROAc | NH4OAc | AcOOH | FAc | Ne | |||||||||||||
| NaOAc | Mg (OAc) 2 | Al (OAc) 3. ALSOL. Al (OAc) 2OH. Al2SO4(OAc) 4 | Si | P | S | ClAc | Ar | ||||||||||||
| KOAc | Ca (OAc) 2 | Cr (OAc) 2. Cr (OAc) 3 | Mn (OAc) 2. Mn (OAc) 3 | Fe (OAc) 2. Fe (OAc) 3 | Co (OAc) 2,. | Ni (OAc) 2 | Cu (OAc) 2 | Zn (OAc) 2 | Ge | Se | BrAc | Kr | |||||||
| Y (OAc) 3 | Nb | Mo (OAc) 2 | Tc | .. | Rdiv class="ht"(OAc) 4 | Pd (OAc) 2 | AgOAc | Cd (OAc) 2 | In | . | Sb (OAc) 3 | Te | IAc | Xe | |||||
| CsOAc | Ba (OAc) 2 | Hf | Ta | W | Re | Os | Ir | Pt (OAc) 2 | Au | ,. Hg (OAc) 2 | TlOAc. | Pb (OAc) 2. Pb ( OAc) 4 | Bi (OAc) 3 | Po | At | Rn | |||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| Pr | Nd | Pm | Tb | Er | Tm | ||||||||||||||
| Ac | Th | Па | UO2(OAc) 2 | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | Нет | Lr | |||||