 | |
| Имена | |
|---|---|
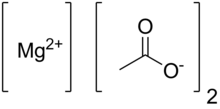
| Название ИЮПАК Ацетат магния | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.005.050 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | Mg (CH 3 COO) 2 |
| Молярная масса | 142,394 (безводный) 214,455 (тетрагидрат) |
| Появление | Белые гигроскопичные кристаллы |
| Плотность | 1,45 г / см 3 |
| Температура плавления | 80 ° С (176 ° F, 353 К) (тетрагидрат) |
| Растворимость в воде | Растворимый |
| Магнитная восприимчивость (χ) | −116,0 10 −6 см 3 / моль (+4 H 2 O |
| Родственные соединения | |
| Другие катионы | Ацетат кальция |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Безводный ацетат магния имеет химическую формулу Mg (C 2 H 3 O 2 ) 2, а в его гидратированной форме, тетрагидрат ацетата магния, он имеет химическую формулу Mg (CH 3 COO) 2 • 4H 2 O. В этом соединении магний имеет степень окисления 2+. Ацетат магния - это магниевая соль уксусной кислоты. Он расплывается и при нагревании разлагается с образованием оксида магния. Ацетат магния обычно используется в качестве источника магния в биологических реакциях.
Ацетат магния выглядит как белые гигроскопичные кристаллы. Пахнет уксусной кислотой и растворяется в воде. Когда он находится в водном растворе, его pH будет от щелочного до нейтрального.
Из-за того, что он очень гигроскопичен, его необходимо хранить вдали от воды. Он также несовместим с сильными окислителями и не должен смешиваться с ними.
Синтез ацетата магния по реакции гидроксида магния с уксусной кислотой.
Карбонат магния суспендировали в дистиллированной воде с 20% -ным раствором уксусной кислоты.
Взаимодействие металлического магния с уксусной кислотой, растворенной в сухом бензоле, вызывает образование ацетата магния с выделением газообразного водорода.
В 1881 году Чарльз Кламонд изобрел корзину Кламонда, одну из первых эффективных газовых мантий. Реагенты, используемые в этом изобретении, включали ацетат магния, гидроксид магния и воду.
Ацетат магния обычно используется в качестве источника магния или ацетат-иона в химических экспериментах. Одним из примеров этого является использование ацетата магния и нитрата магния для проведения молекулярно-динамического моделирования и измерения поверхностного натяжения. В эксперименте авторы обнаружили, что ацетат имеет более сильное сродство к поверхности по сравнению с нитрат-ионом и что Mg 2+ сильно отталкивается от интерференции воздух / жидкость. Они также обнаружили, что Mg 2+ имеет более сильную тенденцию связываться с ионом ацетата по сравнению с нитратом.
Одно из наиболее распространенных применений ацетата магния - это смесь под названием ацетат кальция и магния (CMA). Это смесь ацетата кальция и ацетата магния. CMA считается экологически чистой альтернативой антиобледенителю NaCl и CaCl 2. CMA также действует как мощный агент для снижения выбросов SO 2, NO x и токсичных твердых частиц в процессах сжигания угля для уменьшения кислотных дождей и как эффективный катализатор для облегчения сжигания угля.
Было обнаружено, что ацетат магния вызывает конформационные изменения в ферменте Primase Escherichia coli. В этом эксперименте сравнивали Mg (OAc) 2, MnCl 2, CaCl 2, NaOAc, LiCl, MgSO 4 и MgCl 2, чтобы увидеть, какое влияние они оказывают на фермент Escherichia coli Primase. Экспериментаторы обнаружили, что Mg (OAc) 2 вызывает наилучшие конформационные изменения. MgSO 4 и MgCl 2 слегка вызывали эффект, а остальные - нет.
Когда ацетат магния смешивают с перекисью водорода, он действует как бактерицидное средство.
Было показано, что ацетат магния эффективен для озоления органических соединений при подготовке к анализу на фтор, когда присутствуют высокие или низкие концентрации фтора.
Ацетат магния - относительно безопасное соединение, которому присвоен нулевой рейтинг опасности для здоровья. Однако всегда следует обращаться с ним в перчатках и защитных очках. При попадании в глаза, на кожу, при проглатывании или вдыхании он вызовет раздражение в соответствующих областях: глазах, коже, пищеварительной системе и легких.
| ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | Он | |||||||||||||||||||
| LiOAc | Be (OAc) 2 BeAcOH | B (OAc) 3 | AcOAc ROAc | NH 4 OAc | AcOOH | FAc | Ne | |||||||||||||
| NaOAc | Mg (OAc) 2 | Al (OAc) 3 АЛСОЛ Al (OAc) 2 OH Al 2 SO 4 (OAc) 4 | Si | п | S | ClAc | Ar | |||||||||||||
| KOAc | Ca (OAc) 2 | Sc (OAc) 3 | Ti (OAc) 4 | VO (OAc) 3 | Cr (OAc) 2 Cr (OAc) 3 | Mn (OAc) 2 Mn (OAc) 3 | Fe (OAc) 2 Fe (OAc) 3 | Co (OAc) 2 | Ni (OAc) 2 | Cu (OAc) 2 | Zn (OAc) 2 | Ga (OAc) 3 | Ge | As (OAc) 3 | Se | BrAc | Kr | |||
| RbOAc | Sr (OAc) 2 | Y (OAc) 3 | Zr (OAc) 4 | Nb | Пн (OAc) 2 | Tc | Ru 2 (OAc) 4 Cl Ru (OAc) 3 | Rh 2 (OAc) 4 | Pd (OAc) 2 | AgOAc | Cd (OAc) 2 | В | Sn (OAc) 2 Sn (OAc) 4 | Sb (OAc) 3 | Te | IAc | Xe | |||
| CsOAc | Ba (OAc) 2 | * | Лу (OAc) 3 | Hf | Та | W | Re | Операционные системы | Ir | Pt (OAc) 2 | Au | Hg 2 (OAc) 2, Hg (OAc) 2 | TlOAc Tl (OAc) 3 | Pb (OAc) 2 Pb (OAc) 4 | Bi (OAc) 3 | По | В | Rn | ||
| Пт | Ра | ** | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | ||
| * | La (OAc) 3 | Ce (OAc) x | Pr | Nd | Вечера | Sm (OAc) 3 | Eu (OAc) 3 | Gd (OAc) 3 | Tb | Dy (OAc) 3 | Хо (OAc) 3 | Э | Тм | Yb (OAc) 3 | ||||||
| ** | Ac | Чт | Па | UO 2 (OAc) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | ||||||