 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Ethenylbenzene | |
| Другие имена Стирол винилбензол фенилэтен фенилэтилен Cinnamene Стирол Diarex ВЧ 77 Styrolene Styropol | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100,002,592 |
| КЕГГ | |
| PubChem CID | |
| Номер RTECS | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | С 8 Н 8 |
| Молярная масса | 104,15 г / моль |
| Появление | бесцветная маслянистая жидкость |
| Запах | сладкий, цветочный |
| Плотность | 0,909 г / см 3 |
| Температура плавления | -30 ° С (-22 ° F, 243 К) |
| Точка кипения | 145 ° С (293 ° F, 418 К) |
| Растворимость в воде | 0,03% (20 ° С) |
| журнал P | 2,70 |
| Давление газа | 5 мм рт. Ст. (20 ° C) |
| Магнитная восприимчивость (χ) | −6,82 × 10 −5 см 3 / моль |
| Показатель преломления ( n D) | 1,5469 |
| Вязкость | 0,762 сП в 20 ° C |
| Состав | |
| Дипольный момент | 0,13 Д |
| Опасности | |
| Основные опасности | легковоспламеняющийся, токсичный, вероятно канцерогенный |
| Паспорт безопасности | Паспорт безопасности |
| R-фразы (устаревшие) | R10 R36 |
| S-фразы (устаревшие) | S38 S20 S23 |
| NFPA 704 (огненный алмаз) |  2 3 2 2 3 2 |
| точка возгорания | 31 ° С (88 ° F, 304 К) |
| Пределы взрываемости | 0,9–6,8% |
| Смертельная доза или концентрация (LD, LC): | |
| ЛК 50 ( средняя концентрация ) | 2194 ppm (мышь, 4 ч ) 5543 ppm (крыса, 4 ч) |
| LC Lo ( самый низкий опубликованный ) | 10000 частей на миллион (человек, 30 мин) 2771 частей на миллион (крыса, 4 часа) |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 100 ppm C 200 ppm 600 ppm (максимум 5 минут за любые 3 часа) |
| REL (рекомендуется) | TWA 50 частей на миллион (215 мг / м 3) ST 100 частей на миллион (425 мг / м 3) |
| IDLH (Непосредственная опасность) | 700 частей на миллион |
| Родственные соединения | |
| Родственные стиролы; родственные ароматические соединения | полистирол, стильбен ; этилбензол |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Стирол ( / с т aɪ г я н / ) представляет собой органическое соединение, с химической формулой С 6 Н 5 СН = СН 2. Это производное бензола представляет собой бесцветную маслянистую жидкость, хотя выдержанные образцы могут иметь желтоватый оттенок. Соединение легко испаряется и имеет сладкий запах, хотя высокие концентрации имеют менее приятный запах. Стирол является предшественником полистирола и некоторых сополимеров. В 2010 году было произведено около 25 миллионов тонн стирола, а к 2018 году оно увеличится до примерно 35 миллионов тонн.
Стирол назван в честь бальзама Storax, смолы деревьев Liquidambar семейства Altingiaceae. В естественных условиях стирол содержится в небольших количествах в некоторых растениях и пищевых продуктах ( корице, кофейных зернах, бальзамических деревьях и арахисе ), а также в каменноугольной смоле.
В 1839 году немецкий аптекарь Эдуард Симон выделил летучую жидкость из смолы (названной storax или стиракс (лат.)) Американской сладкой резинки ( Liquidambar styraciflua). Он назвал жидкость «стирол» (теперь стирол). Он также заметил, что когда стирол подвергался воздействию воздуха, света или тепла, он постепенно превращался в твердое, похожее на резину вещество, которое он назвал «оксидом стирола». К 1845 году немецкий химик Август Хофманн и его ученик Джон Блит определили эмпирическую формулу стирола: C 8 H 8. Они также определили, что «оксид стирола» Саймона, который они переименовали в «метастирол», имел ту же эмпирическую формулу, что и стирол. Кроме того, они могли получить стирол путем сухой перегонки «метастирола». В 1865 году немецкий химик Эмиль Эрленмейер обнаружил, что стирол может образовывать димер, а в 1866 году французский химик Марселин Бертло заявил, что «метастирол» представляет собой полимер стирола (то есть полистирола ). Тем временем другие химики изучали другой компонент сторакса, а именно коричную кислоту. Они обнаружили, что коричная кислота может декарбоксилироваться с образованием «циннамола» (или «циннамола»), который оказался стиролом. В 1845 году французский химик Эмиль Копп предположил, что эти два соединения идентичны, а в 1866 году Эрленмейер предположил, что и «циннамол», и стирол могут быть винилбензолом. Однако стирол, полученный из коричной кислоты, по-видимому, отличался от стирола, полученного путем перегонки смолы Storax: последний был оптически активным. В конце концов, в 1876 году голландский химик Ван'т Хофф разрешил двусмысленность: оптическая активность стирола, полученного перегонкой смолы Storax, была обусловлена загрязнением.
Подавляющее большинство стирола производится из этилбензола, и почти весь производимый в мире этилбензол предназначен для производства стирола. Таким образом, два производственных процесса часто тесно интегрированы. Этилбензол получают в результате реакции Фриделя – Крафтса между бензолом и этиленом ; Первоначально в качестве катализатора использовался хлорид алюминия, но в современном производстве он был заменен цеолитами.
Около 80% стирола получают путем дегидрирования из этилбензола. Это достигается за счет использования перегретого пара (до 600 ° C) на катализаторе из оксида железа (III). Реакция сильно эндотермична и обратима, с типичным выходом 88–94%.
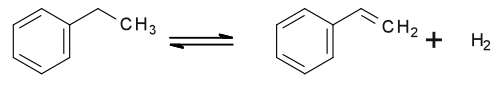
Затем неочищенный продукт этилбензол / стирол очищают перегонкой. Поскольку разница в точках кипения между двумя соединениями составляет всего 9 ° C при атмосферном давлении, это требует использования ряда дистилляционных колонн. Это требует больших затрат энергии и дополнительно осложняется тенденцией стирола подвергаться термически индуцированной полимеризации в полистирол, что требует непрерывного добавления в систему ингибитора полимеризации.
Стирол также коммерчески производится совместно в процессе, известном как POSM ( Lyondell Chemical Company ) или SM / PO ( Shell ) для мономера стирола / оксида пропилена. В этом процессе этилбензол обрабатывают кислородом с образованием гидропероксида этилбензола. Этот гидропероксид затем используется для окисления пропилена до оксида пропилена, который также извлекается как побочный продукт. Оставшийся 1-фенилэтанол обезвоживают с получением стирола:

Экстракция пиролизного бензина осуществляется в ограниченном масштабе.
Стирол можно производить из толуола и метанола, которые являются более дешевым сырьем, чем те, которые используются в обычном процессе. Этот процесс страдает низкой селективностью, связанной с конкурирующим разложением метанола. Exelus Inc. утверждает, что разработала этот процесс с коммерчески жизнеспособной селективностью при 400–425 ° C и атмосферном давлении, пропуская эти компоненты через запатентованный цеолитный катализатор. Сообщается, что получают смесь стирола и этилбензола приблизительно 9: 1 с общим выходом стирола более 60%.
Другой путь получения стирола включает реакцию бензола и этана. Этот процесс разрабатывают Снампроджетти и Доу. Этан вместе с этилбензолом подается в реактор дегидрирования с катализатором, способным одновременно производить стирол и этилен. Отходящий поток дегидрирования охлаждается и отделяется, а поток этилена рециркулируют в установку алкилирования. В способе предпринимаются попытки преодолеть предыдущие недостатки в более ранних попытках развития производства стирола из этана и бензола, такие как неэффективное извлечение ароматических углеводородов, получение высоких уровней тяжелых фракций и смол и неэффективное разделение водорода и этана. Разработка процесса продолжается.
Лабораторный синтез стирола влечет за собой декарбоксилирование из коричной кислоты :
Этим методом впервые был получен стирол.
Наличие винильной группы позволяет стиролу полимеризоваться. Коммерчески значимые продукты включают полистирол, АБС, стирол-бутадиеновый (SBR) каучук, стирол-бутадиеновый латекс, SIS (стирол-изопрен-стирол), S-EB-S (стирол-этилен / бутилен-стирол), стирол- дивинилбензол (S -DVB), стирол-акрилонитриловая смола (SAN) и ненасыщенные полиэфиры, используемые в смолах и термореактивных компаундах. Эти материалы используются в резине, пластике, изоляционных материалах, стекловолокне, трубах, деталях автомобилей и лодок, пищевых контейнерах и подложках для ковров.
В жидком или газообразном состоянии чистый стирол самопроизвольно полимеризуется в полистирол без необходимости использования внешних инициаторов. Это известно как автополимеризация. При 100 ° C он будет автополимеризоваться со скоростью ~ 2% в час, а при более высоких температурах - быстрее. Реакция полимеризации экзотермична ; следовательно, существует реальный риск теплового разгона и взрыва. Примером может служить взрыв танкера Stolt Groenland в 2019 году, а также взрывы на Phillips Petroleum Company в 1999 и 2000 годах. Реакцию автополимеризации можно контролировать только путем непрерывного добавления ингибиторов полимеризации.
Согласно нескольким источникам, стирол считается «известным канцерогеном », особенно в случае контакта с глазами, а также в случае контакта с кожей, при проглатывании и вдыхании. Стирол в значительной степени метаболизируется в оксид стирола в организме человека в результате окисления цитохромом P450. Оксид стирола считается токсичным, мутагенным и, возможно, канцерогенным. Оксид стирола впоследствии гидролизуется in vivo до стиролгликоля ферментом эпоксидгидролазой. Агентство США по охране окружающей среды (EPA) описал стирол быть «подозревается токсин в желудочно - кишечный тракт, почки и дыхательную систему, среди других». 10 июня 2011 года Национальная токсикологическая программа США охарактеризовала стирол как «разумно предполагаемый канцероген для человека». Однако автор STATS описывает обзор научной литературы и приходит к выводу, что «имеющиеся эпидемиологические данные не подтверждают причинно-следственную связь между воздействием стирола и любым типом рака человека». Несмотря на это утверждение, датские исследователи провели работу по изучению взаимосвязи между воздействием стирола на рабочем месте и раком. Они пришли к выводу: «Результаты следует интерпретировать с осторожностью из-за оценки воздействия, проведенной компанией, но возможная связь между воздействием в промышленности армированных пластиков, в основном стирола, и дегенеративными заболеваниями нервной системы и раком поджелудочной железы, заслуживает внимания».. В 2012 году Датское EPA пришло к выводу, что данные по стиролу не подтверждают опасения по поводу рака для стирола. У Агентства по охране окружающей среды США нет классификации рака для стирола, но он был предметом их программы Интегрированной системы информации о рисках (IRIS). Национальная токсикологическая программа из Департамента здравоохранения и социальных служб определила, что стирол «разумно ожидается, будет канцерогенными для человека». Различные регулирующие органы рассматривают стирол в различных контекстах как возможный или потенциальный канцероген для человека. Международное агентство по изучению рака считает стирол быть «вероятно канцерогенные для человека».
Нейротоксические свойства стирола также были изучены, и сообщалось о его влиянии на зрение (хотя его невозможно воспроизвести в последующем исследовании) и на функции слуха. Исследования на крысах дали противоречивые результаты, но эпидемиологические исследования наблюдали синергетическое взаимодействие с шумом, вызывающее проблемы со слухом.
7 мая 2020 года из резервуара на заводе LG Chem (LG Polymers India Private Limited) в RR Venkatapuram, Visakhapatnam, Andra Pradesh, India, произошла утечка газа, который, как сообщается, представляет собой стирол. Утечка произошла рано утром, когда рабочие готовились к открытию завода, который был закрыт из -за пандемии COVID-19. По сообщениям, тринадцать человек погибли и более 200 человек были госпитализированы.