Радикальный инициатор
редактировать
В химии, радикальные инициаторы представляют собой вещества, которые могут образовывать радикальные частицы в мягких условиях и способствовать радикальным реакциям. Эти вещества обычно обладают слабыми связями - связями, которые имеют небольшие энергии диссоциации связи. Радикальные инициаторы используются в промышленных процессах, таких как синтез полимера. Типичными примерами являются молекулы галогена , азосоединения и органические и неорганические пероксиды.
Основные типы реакций инициирования
- Галогены подвергаются гомолитическое деление относительно легко. Хлор, например, дает два радикала хлора (Cl •) при облучении ультрафиолетовым светом. Этот процесс используется для хлорирования алканов.
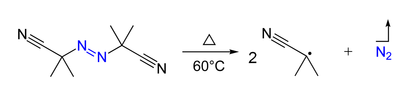
- Азосоединения (R- N = N-R ') могут быть предшественниками двух атомов углерода -центрированные радикалы (R • и R '•) и газообразный азот при нагревании и / или облучении. Например, AIBN и ABCN дают изобутиронитрильный и циклогексанкарбонитрильный радикалы соответственно.
- Органические пероксиды имеют пероксидную связь (- O -O -), который легко расщепляется с образованием двух кислородно-центрированных радикалов. Оксильные радикалы нестабильны и, как полагают, превращаются в относительно стабильные углеродно-центрированные радикалы. Например, ди-трет-бутилпероксид (т- Bu OO трет-Bu) дает два трет-бутоксирадикала (трет-BuO •), и эти радикалы становятся метил радикалами ( C H 3•) с потерей ацетона. Пероксид бензоила ((Ph C) OO) 2) образует бензоилоксильные радикалы (PhCOO •), каждый из которых теряет диоксид углерода и превращается в фенильный радикал (Ph •). Пероксид метилэтилкетона также широко распространен, и пероксид ацетона также в редких случаях используется в качестве радикального инициатора.
- Неорганические пероксиды действуют аналогично органическим пероксидам. Многие полимеры часто получают из алкенов при инициировании солями пероксидисульфата. В растворе пероксидисульфат диссоциирует с образованием сульфатных радикалов:
- [O3SO-OSO 3 ] ⇌ 2 [SO 4]
Сульфатный радикал присоединяется к алкенам, образуя радикальные сульфатные эфиры, например CHPhCH 2 OSO 3, которые добавляют дополнительные алкены за счет образования связей C-C. Таким способом получают многие полимеры стирола и фторалкена.
- При радикальной полимеризации с переносом атома (ATRP) галогениды углерода обратимо образуют органические радикалы в присутствии переходного металла катализатора.

Общая реакция ATRP. А. Посвящение. Б. Равновесие с покоящимися видами. C. Распространение
Безопасность
Некоторые радикальные инициаторы, такие как азосоединения и пероксиды, могут детонировать при повышенных температурах, поэтому их следует хранить в холодном состоянии.
Ссылки

 Общая реакция ATRP. А. Посвящение. Б. Равновесие с покоящимися видами. C. Распространение
Общая реакция ATRP. А. Посвящение. Б. Равновесие с покоящимися видами. C. Распространение