 | |
| Имена | |
|---|---|
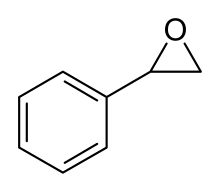
| Предпочтительное название IUPAC Фенилоксиран | |
| Другие названия Эпоксистирол; Оксид стирила; Фенилэтилен оксид | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.002.252 |
| КЕГГ | |
| PubChem CID | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | С 8 Н 8 О |
| Молярная масса | 120,151 г моль -1 |
| Появление | От бесцветной до светло-желтой жидкости |
| Плотность | 1,052 г / мл |
| Температура плавления | -37 ° С (-35 ° F, 236 К) |
| Точка кипения | 194 ° С (381 ° F, 467 К) |
| Опасности | |
| Паспорт безопасности | MSDS Оксфордского университета |
| Классификация ЕС (DSD) (устарела) | Вреден (XN); Коррозионный (C) |
| R-фразы (устаревшие) | R20 R22 R34 R36 R37 R38 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Оксид стирола - это эпоксид, полученный из стирола. Он может быть получен путем эпоксидирования стирола с пероксибензойной кислотой, в реакции Прилежаева :

Оксид стирола плохо растворяется в воде. Незначительное количество кислоты в воде вызывает гидролиз до рацемического фенилэтиленгликоля через бензильный катион. Если количества воды недостаточно, произойдет катализируемая кислотой изомеризация фенилацетальдегида.
Оксид стирола в организме метаболизируется до миндальной кислоты, фенилглиоксиловой кислоты, бензойной кислоты и гиппуровой кислоты.
Гидрирование оксида стирола дает фенэтиловый спирт.
Поскольку оксид стирола имеет хиральный центр у бензильного атома углерода, существуют ( R) -оксид стирола и ( S) -оксид стирола. Если используется оптически чистый реагент, будет получено только одно оптически чистое соединение.
Оксид стирола является основным метаболитом стирола у людей или животных, возникающим в результате окисления цитохромом P450. Считается, что он может вызывать канцерогенность при попадании значительного количества через желудочный зонд мышам и крысам. Оксид Стирола затем гидролизует в естественных условиях до стирола гликоля с помощью эпоксидгидролазы.
Оксид стирола имеет хиральный центр и, следовательно, два энантиомера. Сообщалось, что два энантиомера имели разную токсикокинетику и токсичность. Сообщалось, что оксид ( R) -стирола преимущественно образуется у мышей, особенно в легких, тогда как оксид ( S) -стирола предпочтительно образуется у крыс. У добровольцев кумулятивная экскреция ( S) -энантиомера стиролгликоля и миндальной кислоты была выше, чем у R- формы после воздействия стирола. В микросомах печени человека опосредованное цитохромом P450 окисление стирола показало продукцию большего количества S- энантиомера по сравнению с R- энантиомером. Также было обнаружено, что ( S) -стирол оксид предпочтительно гидролизуется, чем R- энантиомер, в микросомах печени человека. Исследования на животных показали, что ( R) -энантиомер оксида стирола был более токсичным, чем ( S) -энантиомер для мышей.