MIR-155 является микроРНК, что в организме человека кодируется MIR155 хост - гена или MIR155HG. МиР-155 участвует в различных физиологических и патологических процессах. Экзогенный молекулярный контроль in vivo экспрессии miR-155 может подавлять злокачественный рост, вирусные инфекции и усиливать прогрессирование сердечно-сосудистых заболеваний.
СОДЕРЖАНИЕ
- 1 открытие
- 2 Биогенез
- 3 Эволюционное сохранение
- 4 Распределение тканей
- 5 мишеней
- 6 физиологических ролей
- 6.1 Кроветворение
- 6.2 Иммунная система
- 7 Активность и фенотипы
- 8 Клиническое значение
- 8.1 Сердечно-сосудистые
- 8.2 Иммунитет
- 8.2.1 Снижение IgG1
- 8.2.2 Злокачественные новообразования лимфоцитов
- 8.3 Воспаление
- 8.4 ДНК-вирусы
- 8.5 Рак
- 9 Примечания
- 10 См. Также
- 11 Источники
- 12 Дальнейшее чтение
- 13 Внешние ссылки
Открытие
Первоначально MIR155HG был идентифицирован как ген, который транскрипционно активируется путем вставки промотора в общий сайт интеграции ретровирусов в B-клеточных лимфомах, и ранее назывался BIC (B-cell Integration Cluster). MIR155HG транскрибируется РНК - полимеразы II и полученную ~ 1500 нуклеотид РНК ограничен и Полиаденилированная. Одноцепочечный miR-155 из 23 нуклеотидов, содержащийся в экзоне 3, впоследствии процессируется из исходной молекулы РНК.
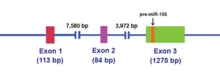
Рисунок 1. Схематическое изображение MIR155HG (инвентарный номер NC_000021). Этот ген занимает 13024 п.н., состоит из трех экзонов и кодирует некодирующую первичную миРНК (pri-miRNA) размером 1500 п.н. (номер доступа NR_001458). Расположение пре-Мир-155 обозначено оранжевой рамкой.
Биогенез
Транскрипт РНК MIR155HG не содержит длинной открытой рамки считывания (ORF), однако он включает петлю ствола с несовершенными парами оснований, которая сохраняется у разных видов. Эта некодирующая РНК ( нкРНК ) теперь определяется как первичная миРНК (pri-miRNA). После того, как miR-155 pri-miRNA транскрибируется, этот транскрипт расщепляется ядерным микропроцессорным комплексом, основными компонентами которого являются эндонуклеаза Drosha типа РНКазы III и белок критической области 8 DiGeorge ( DGCR8 ), с образованием 65-нуклеотидной основы. микроРНК-предшественник петли (pre-mir-155) (см. рисунок 2).

Рисунок 2. Последовательность стволовой петли pre-mir-155, которая созревает из транскрипта pri-miRNA. Последовательность зрелой miR-155 (miR-155-5p) показана зеленым, а последовательность зрелой miR-155 * (miR-155-3p) показана красным.
После экспорта из ядра с помощью exportin-5 молекулы pre-mir-155 расщепляются Dicer рядом с концевой петлей, в результате чего образуются дуплексы РНК из ~ 22 нуклеотидов. После расщепления Дайсером белок Argonaute (Ago) связывается с короткими дуплексами РНК, образуя ядро многосубъединичного комплекса, называемого комплексом индуцированного РНК сайленсинга ( RISC ). Подобно дуплексам миРНК, одна из двух цепей, «пассажирская миРНК» (miR-155 *), высвобождается и деградирует, в то время как другая цепь, обозначенная как «направляющая цепь» или «зрелая миРНК» (miR-155), сохраняется в RISC.
Недавние данные подтверждают, что оба плеча шпильки pre-miRNA могут давать зрелые miRNAs. В связи с увеличением числа примеров, когда две функциональные зрелые miRNA обрабатываются из противоположных плеч одной и той же пре-miRNA, продукты pre-mir-155 теперь обозначаются суффиксом -5p (от 5'-плеча) (например, miR-155 -5p) и -3p (от 3'-плеча) (например, miR-155-3p) после их названия (см. Рисунок 3).

Рисунок 3. Последовательность зрелой miR-155 (miR-155-5p) показана зеленым, а последовательность зрелой miR-155 * (miR-155-3p) показана красным.
Как только miR-155-5p / -3p собирается в RISC, эти молекулы впоследствии узнают свою информационную РНК-мишень ( мРНК ) посредством взаимодействий спаривания оснований между нуклеотидами 2 и 8 miR-155-5p / -3p (затравочная область) и комплементарные нуклеотиды преимущественно в 3'-нетранслируемой области ( 3'-UTR ) мРНК (см. рисунки 4 и 5 ниже). Наконец, когда miR-155-5p / -3p действует как адаптер для RISC, комплексно связанные мРНК подвергаются репрессии трансляции (то есть ингибированию инициации трансляции ) и / или деградации после деаденилирования.
Эволюционное сохранение
Ранние филогенетические анализы показали, что последовательность pre-mir-155 и miR-155-5p сохраняется у человека, мыши и курицы. Недавние аннотированные данные секвенирования показали, что 22 различных организма, включая млекопитающих, земноводных, птиц, рептилий, морских брызг и морских миног, экспрессируют консервативную miR-155-5p. [1] В настоящее время доступно гораздо меньше данных о последовательностях miR-155-3p, поэтому неясно, насколько консервативна эта miRNA у разных видов. [2]
Распределение тканей
Нозерн-блоттинг показал, что pri-miRNA miR-155 обильно экспрессируется в селезенке и тимусе человека и обнаруживается в печени, легких и почках. Впоследствии эксперименты с полимеразной цепной реакцией ( ПЦР ) показали, что miR-155-5p обнаруживается во всех исследованных тканях человека. Анализ последовательности библиотек клонов малых РНК, сравнивающий экспрессию miRNA со всеми другими исследованными системами органов, показал, что miR-155-5p была одной из пяти miRNA (т.е. miR-142, miR-144, miR-150, miR-155 и miR-223).), который был специфичным для гемопоэтических клеток, включая В-клетки, Т-клетки, моноциты и гранулоциты. Вместе эти результаты предполагают, что miR-155-5p экспрессируется в ряде тканей и типов клеток и, следовательно, может играть решающую роль в широком спектре биологических процессов, включая гематопоэз.
Хотя очень мало исследований изучали уровни экспрессии miR-155-3p, Landgraf et al. установили, что уровни экспрессии этой miRNA были очень низкими в гемопоэтических клетках. Кроме того, анализ ПЦР показал, что хотя miR-155-3p обнаруживается в ряде тканей человека, уровни экспрессии этой miRNA были в 20-200 раз меньше по сравнению с уровнями miR-155-5p. Несмотря на то, что функция miR-155-3p в значительной степени игнорировалась, несколько исследований теперь показывают, что в некоторых случаях (астроциты и плазмацитоидные дендритные клетки) как miR-155-5p, так и -3p могут функционально созревать из пре-зеркалки. 155.
Цели
Биоинформатический анализ с использованием TargetScan 6.2 (дата выпуска июнь 2012 г.) [3] выявил, как минимум, 4 174 предполагаемых мишени мРНК miR-155-5p человека, в общей сложности 918 консервативных сайтов (т.е. между мышью и человеком) и 4249 плохо консервативных сайтов ( т.е. только человек). Хотя алгоритм TargetScan 6.2 не может быть использован для определения предполагаемых мишеней miR-155-3p, можно предположить, что эта miRNA может также потенциально регулировать экспрессию тысяч мишеней мРНК.
Недавно был составлен исчерпывающий список мишеней miR-155-5p / мРНК, которые были экспериментально подтверждены как демонстрацией регуляции эндогенного транскрипта с помощью miR-155-5p, так и проверкой посевной последовательности miR-155-5p с помощью репортерного анализа. В этот список включены 140 генов и регуляторные белки миелопоэза и лейкемогенеза (например, SHIP-1, AICDA, ETS1, JARID2, SPI1 и т. Д.), Воспаления (например, BACH1, FADD, IKBKE, INPP5D, MYD88, RIPK1, SPI1, SOCS, и т.д.) и известные опухолевые супрессоры (например, CEBPβ, IL17RB, PCCD4, TCF12, ZNF652 и т.д.). Подтвержденный сайт связывания miR-155-5p в мРНК SPI1 и валидированный сайт связывания miR-155-3p в мРНК IRAK3 показаны на фигурах 4 и 5 соответственно.

Рисунок 4. Дополнительные спаривания оснований между MIR-155-5p и человеческого SPI1 (селезенку фокус вируса, образующего провирусной интеграции онкоген) (также известный как PU.1) мРНК. Сайт связывания miR-155-5p расположен на 46–53 парах оснований ниже стоп-кодона мРНК SPI1. Необходимая пара оснований «исходной последовательности» обозначена жирным тире.

Фигура 5. Комплементарное спаривание оснований между miR-155-3p и мРНК IRAK3 человека (киназа 3, ассоциированная с рецептором интерлейкина-1). Сайт связывания miR-155-3p расположен на 424–430 пар оснований ниже стоп-кодона мРНК IRAK3. Необходимая пара оснований «исходной последовательности» обозначена жирным тире.
Физиологические роли
Кроветворение
Гемопоэз определяется как образование и развитие клеток крови, все из которых происходят из гемопоэтических стволовых клеток-предшественников (HSPC). HSPC представляют собой примитивные клетки, способные к самообновлению и первоначально дифференцирующиеся в общие миелоидные предшественники (CMP) или общие лимфоидные предшественники (CLP) клетки. CMP представляют собой клеточную популяцию, которая превратилась в миелоидную линию, и именно здесь начинается миелопоэз. Во время миелопоэза происходит дальнейшая клеточная дифференцировка, включая тромбопоэз, эритропоэз, гранулопоэз и моноцитопоэз. CLP впоследствии дифференцируются в B-клетки и T-клетки в процессе, обозначенном как лимфопоэз. Учитывая, что miR-155-5p экспрессируется в гемопоэтических клетках, было высказано предположение, что эта miRNA играет критическую роль в этих процессах клеточной дифференцировки. В поддержку этой предпосылки было обнаружено, что miR-155-5p экспрессируется в CD34 (+) HSPC человека, и было высказано предположение, что эта miRNA может удерживать эти клетки на ранней стадии стволовых клеток-предшественников, ингибируя их дифференцировку в более зрелые клетки. клеточный (т.е. мегакариоцитарный / эритроидный / гранулоцитарный / моноцитарный / B-лимфоидный / T-лимфоидный). Эта гипотеза была подтверждена, когда HSPC, трансдуцированные pre-mir-155, генерировали в 5 раз меньше миелоидных и в 3 раза меньше эритроидных колоний. Кроме того, Hu et al. продемонстрировали, что белок гомеобокса, HOXA9, регулирует экспрессию MIR155HG в миелоидных клетках и что эта miRNA играет функциональную роль в гематопоэзе. Эти исследователи обнаружили, что форсированная экспрессия miR-155-5p в клетках костного мозга приводит к ~ 50% снижению SPI1 (т.е. PU.1), фактора транскрипции и регулятора миелопоэза, а также подтвержденной мишени этой miRNA. Также было установлено, что дифференцировка очищенных эритроидных клеток-предшественников in vitro приводит к прогрессивному снижению экспрессии miR-155-5p в зрелых эритроцитах. Кроме того, у мышей с дефицитом pre-mir-155 обнаружены явные дефекты в развитии лимфоцитов и генерации B- и T-клеточных ответов in vivo. Наконец, было установлено, что для развития регуляторных Т-клеток ( Tregs ) требуется miR-155-5p, и было показано, что эта miRNA играет роль в гомеостазе Treg и общей выживаемости, напрямую воздействуя на SOCS1, негативный регулятор передачи сигналов IL-2. Взятые вместе, эти результаты убедительно свидетельствуют о том, что miR-155-5p является важной молекулой в контроле нескольких аспектов гематопоэза, включая миелопоэз, эритропоэз и лимфопоэз.
Иммунная система
Врожденная иммунная система представляет собой первую линию обороны против вторжения патогенных микроорганизмов и рассматривается в качестве основного инициатора воспалительных реакций. Его клеточный компонент включает в себя в первую очередь моноциты / макрофаги, гранулоциты и дендритные клетки (DC), которые активируются при восприятии консервативных структур патогенов ( PAMP ) рецепторами распознавания образов, такими как Toll-подобные рецепторы ((TLR)). Экспрессия MIR155HG (т.е. miR-155-5p) значительно усиливается за счет стимуляции макрофагов и дендритных клеток агонистами TLR. Поскольку микробный липополисахарид (агонист TLR4) активирует цепь событий, которые приводят к стимуляции факторов транскрипции NF-κB и AP-1, было высказано предположение, что активация MIR155HG эндотоксином может быть опосредована этими факторами транскрипции. Действительно, было обнаружено, что экспрессия MIR155HG активируется в обработанных LPS мышиных макрофагальных клетках (т.е. Raw264.7) посредством механизма, опосредованного NF-κB. Кроме того, инфекция H. pylori первичных макрофагов, происходящих из костного мозга мыши, приводила к усилению регуляции MIR155HG, зависимой от NF-κB. В контексте вирусной инфекции вирусом везикулярного стоматита (VSV) заражение перитонеальных макрофагов мыши, как сообщается, приводит к сверхэкспрессии miR-155-5p через индуцируемый ретиноевой кислотой ген, I / JNK / NF-κB-зависимый путь. В пользу роли AP-1 в активации MIR155HG свидетельствуют исследования с использованием стимулов, относящихся к вирусной инфекции, таких как поли (I: C) лиганда TLR3 или бета-интерферон (IFN-β). Ниже этих стимулов AP-1, по-видимому, играет основную роль в активации MIR155HG.
После инициации через активацию, например, TLR стимулами патогенов miR-155-5p функционирует как посттранскрипционный регулятор сигнальных путей врожденного иммунитета. Важно отметить, что miR-155-5p проявляет такую же реакцию на стимулы патогенов (например, LPS, агонист TLR4), что и мРНК основных провоспалительных маркеров. После активации miR-155-5p подавляет негативные регуляторы воспаления. К ним относятся инозитолполифосфат-5-фосфатаза (INPP5D, также обозначаемая как SHIP1) и супрессор передачи сигналов цитокинов 1 (SOCS1), подавление которых способствует выживанию клеток, их росту, миграции и антипатогенным ответам. Помимо поддержки активации защитных путей miR-155-5p может также ограничивать силу результирующего NF-κB-зависимого воспалительного ответа, предполагая различные функции miR-155 на разных стадиях воспаления.
Взятые вместе, эти наблюдения подразумевают, что активация MIR155HG может зависеть от контекста, учитывая, что как AP-1-, так и NF-κB-опосредованные механизмы регулируют экспрессию этого гена. Эти исследования также предполагают, что широкий спектр вирусных и бактериальных медиаторов воспаления может стимулировать экспрессию miR-155-5p и указывают на тесную взаимосвязь между воспалением, врожденным иммунитетом и экспрессией MIR155HG.
Активность и фенотипы
Имеются данные о том, что miR-155 участвует в каскадах, связанных с сердечно-сосудистыми заболеваниями и гипертонией, а также, как было обнаружено, участвует в иммунитете, геномной нестабильности, дифференцировке клеток, воспалении, вирусных инфекциях и раке.
Защитные роли miR-155 могут возникать в ответ на его действие на гены сайленсинга, тем самым регулируя время их экспрессии, мутации в сайте-мишени miR-155 лишают его оптимального доступа, необходимого для заглушения генов, что приводит к чрезмерному количеству делинквентных действий, которые могут становятся злокачественными, например, роль miR-155 как защитного агента против предрасположенности к злокачественным новообразованиям, связанным с В-клетками, подчеркивается поддержанием баланса фермента цитидин дезаминазы, индуцированного активацией ( AID ). MiR-155 опосредует регуляцию количества и времени экспрессии AID по иммунологическим сигналам, однако мутации в мишени на мРНК AID приводят к ее невосприимчивости к сайленсингу miR-155 и приводят к необузданной экспрессии его белка, вызывая всплески диких незрелых B-лимфоцитов и AID- опосредованные хромосомные транслокации.
Клиническое значение
Сердечно-сосудистые
Трансфекция miR-155 в первичные фибробласты легких человека снижает эндогенную экспрессию белка AT1R рецептора ангиотензина II. Кроме того, AT1R опосредует связанное с ангиотензином II повышение артериального давления и вносит вклад в патогенез сердечной недостаточности. Нарушение функции miR-155 может быть связано с гипертензией и сердечно-сосудистыми заболеваниями, если цис-регуляторный сайт на 3` UTR AT1R (целевой сайт miR-155) был затронут из-за полиморфизма SNP в самом AT1R. Эта мутация нарушает нацеливание miR-155 и, таким образом, предотвращает подавление экспрессии AT1R. При низком артериальном давлении сверхэкспрессия miR-155 коррелирует с нарушением активности AT1R.
Иммунитет
miR-155 участвует в иммунитете, играя ключевую роль в модуляции гуморальных и врожденных клеточно-опосредованных иммунных ответов, например, у мышей с дефицитом miR-155 иммунологическая память нарушена; делая его жертвой повторяющихся приступов вторжений одного и того же патогена (Rodriguez et al. 2007), созревание и специфичность miR-155-дефицитных B-лимфоцитов нарушаются, поскольку этот процесс зависит от фермента AID, который имеет мишень miR-155 в его конец 3 'UTR. Последствия фенотипические, связанные с дефицитом MIR-155 на мышах показывают позже в жизни, где животные развиваются легкие и кишечные поражения.
Активированные В и Т - клетки демонстрируют повышенную экспрессию микроРНК-155, то же самое для макрофагов и дендритных клеток в иммунной системе. MiR-155 имеет решающее значение для правильного развития и созревания лимфоцитов. Подробности различных проявлений уровней miR-155 и участия в деятельности, определяющей оптимальные иммунные ответы, были предметом многих исследований:
Снижение IgG1
У мышей с дефицитом miR-155 наблюдались дефектные Т- и В-клетки, а также заметно сниженные ответы IgG1, IgG1 снижен, тогда как экспрессия иммуноглобулина IgM остается нормальной у этих мышей. Изменение уровней IgG1 может быть объяснено тем фактом, что он является мишенью для miR-155 в B-клетках, мРНК, кодирующей белок для регулятора транскрипции белка Pu.1, повышение уровня белка Pu.1 предрасполагает к дефектной продукции IgG1. Помимо Pu.1, имеется около 60 других дифференциально повышенных генов в miR-155-дефицитных B-клетках, дальнейшее изучение выявило возможные сайты-мишени miR-155 в 3'-UTR областях этих генов.
Лимфоцитарные злокачественные новообразования
Сродство зрелых рецепторов и специфичность лимфоцитов к патогенным агентам лежат в основе правильных иммунных ответов, оптимальная координация miR-155 требуется для производства нормальных B-лимфоцитов, продукции высокоаффинных антител и балансировки передачи сигналов BCR. Было продемонстрировано, что miR-155 может передаваться через щелевые соединения от лейкозных клеток к здоровым В-клеткам и способствовать их трансформации в опухолеподобные клетки.
Отбор компетентных В-клеток происходит в зародышевом центре, где они обучаются дифференцировать клетки тела от чужеродных антигенов, они конкурируют за распознавание антигена и за помощь Т-клеток, таким способом селективного давления на те В-клетки, которые продемонстрировали высокоаффинные рецепторы. и сотрудничество с Т-клетками ( созревание аффинности ) рекрутируется и внедряется в костный мозг или становится В-клетками памяти, апоптотическое прекращение происходит для тех В-клеток, которые не выдерживают конкуренции. Незрелые В-клетки с дефицитом miR-155 избегают апоптоза в результате повышенных уровней белка Bcl-2 ; белок, который, как было обнаружено, участвует в злокачественных новообразованиях В-клеток и контролируется miR-155.
Воспаление
Воспалительные реакции на триггеры, такие как TNF-α, включают макрофаги с компонентами, которые включают miR-155. miR-155 сверхэкспрессируется при атопическом дерматите и способствует хроническому воспалению кожи за счет увеличения пролиферативного ответа T (H) -клеток за счет подавления CTLA-4. При аутоиммунных заболеваниях, таких как ревматоидный артрит, miR-155 проявляет более высокую экспрессию в тканях пациентов и синовиальных фибробластах. При рассеянном склерозе повышенная экспрессия mir-155 также была измерена в периферических и резидентных миелоидных клетках ЦНС, включая моноциты циркулирующей крови и активированную микроглию. Также было обнаружено, что mir-155 участвует в воспалении. Сверхэкспрессия mir-155 приведет к хроническому воспалительному состоянию у человека.
ДНК-вирусы
В ДНК-вирусах miRNA были экспериментально подтверждены, miRNA в вирусах кодируются dsDNA, примеры таких вирусов включают вирусы герпеса, такие как вирус Эпштейна-Барра ( EBV ) и аденовирусы, еще один вирус, экспрессирующий miR-155-подобную miRNA у кур, является вирусом герпеса. онкогенный MDV-1, неонкогенный родственник которого MDV-2 не обладает, это предполагает участие miR-155 в лимфомагенезе. Вирусы могут использовать миРНК хозяина в той степени, в которой они используют миРНК хозяина для кодирования вирусных клонов, например: miR-K12-11 в герпесвирусе, ассоциированном с саркомой Капоши, имеет область целевой специфичности, ортологичную таковой у miR-155; имитируя действие miR-155 и разделяя с ней мишени, можно предположить, что она подавляет доступность miR-155 к ее мишеням за счет конкуренции, и это, по сути, подавляет экспрессию генов, играющих роль в клеточном росте и апоптозе, таким образом, что бросает вызов правила по miR-155. EBV модулирует экспрессию miR-155 хозяина, которая необходима для роста В-клеток, инфицированных EBV. Клетки, инфицированные EBV, имеют повышенную экспрессию miR-155, тем самым нарушая равновесие экспрессии генов, регулирующих транскрипцию в этих клетках.
Рак
Чрезмерное молчание miR-155 может привести к запуску онкогенных каскадов, которые начинаются с устойчивости к апоптозу, проапоптотический Tumor Protein-53-индуцированный-ядерный белок 1 ( TP53INP1 ) подавляется miR-155, сверхэкспрессия miR-155 приводит к снижению уровней TP53INP1 в аденокарциномах протоков поджелудочной железы и, возможно, в других эпителиальных раках, где активность TP53INP1 теряется, что приводит к уклонению от апоптоза и неконтролируемым приступам роста.
Инактивация репарации несоответствия ДНК ( MMR ), определяемая по увеличению частоты мутаций, является причиной синдрома Линча (LS), также известного как наследственный неполипозный колоректальный рак (HNPCC), подавление белка, контролирующего MMR, осуществляется за счет сверхэкспрессии. miR-155, MMR контролируется группой консервативных белков, снижение активности этих белков приводит к повышенным уровням мутаций в фенотипе, запускающих марш к развитию этого типа рака.
К другим типам опухолей, в которых сообщалось о сверхэкспрессии miR-155, относятся: карцинома щитовидной железы, рак груди, рак толстой кишки, рак шейки матки и рак легких, где количественная оценка различных профилей экспрессии miR-155 потенциально может служить сигналами для обнаружения и оценки опухоли. исхода прогноза. Анализ показывает, что экспрессия miR-155 связана с выживаемостью при тройном отрицательном раке молочной железы.
Примечания
Смотрите также
использованная литература
дальнейшее чтение
- Бентвич I, Авниэль А., Каров Ю., Ааронов Р., Гилад С., Барад О., Барзилай А., Эйнат П., Эйнав Ю., Мейри Е., Шарон Е., Спектор И., Бентвич З. (июль 2005 г.). «Идентификация сотен консервативных и неконсервативных микроРНК человека». Генетика природы. 37 (7): 766–770. DOI : 10.1038 / ng1590. PMID 15965474. S2CID 7746954.
- Хуан Р.С., Ху GQ, Линь Б., Линь З.Й., Сунь CC (декабрь 2010 г.). «Подавление звука MicroRNA-155 усиливает воспалительную реакцию и захват липидов в окисленных липопротеинах низкой плотности, стимулированных макрофагами человека THP-1». Журнал следственной медицины. 58 (8): 961–967. DOI : 10,2310 / jim.0b013e3181ff46d7. PMID 21030878. S2CID 83123221.
- Ceolotto G, Papparella I, Bortoluzzi A, Strapazzon G, Ragazzo F, Bratti P, Fabricio AS, Squarcina E, Gion M, Palatini P, Semplicini A (февраль 2011 г.). «Взаимодействие между miR-155, полиморфизмом AT1R A1166C и экспрессией AT1R у молодых нелеченных гипертоников». Американский журнал гипертонии. 24 (2): 241–246. DOI : 10.1038 / ajh.2010.211. PMID 20966899.
- Ван Г., Там Л.С., Ли Е.К., Кван BC, Чоу К.М., Лук С.К., Ли П.К., Сзето С.К. (декабрь 2010 г.). «Бесклеточные MiR-146a и MiR-155 в сыворотке и моче у пациентов с системной красной волчанкой». Журнал ревматологии. 37 (12): 2516–2522. DOI : 10,3899 / jrheum.100308. PMID 20952466. S2CID 23208771.
- Kutty RK, Nagineni CN, Samuel W, Vijayasarathy C, Hooks JJ, Redmond TM (ноябрь 2010 г.). «Воспалительные цитокины регулируют экспрессию микроРНК-155 в клетках пигментного эпителия сетчатки человека путем активации пути JAK / STAT». Сообщения о биохимических и биофизических исследованиях. 402 (2): 390–395. DOI : 10.1016 / j.bbrc.2010.10.042. PMC 2992362. PMID 20950585.
- Имаидзуми Т, Танака Х, Тадзима А, Йоконо Й, Мацумия Т, Йошида Х, Цуруга К., Айзава-Яширо Т, Хаякари Р., Иноуэ I, Ито Э, Сато К. (2010). «IFN-γ и TNF-α синергетически индуцируют микроРНК-155, которая регулирует экспрессию TAB2 / IP-10 в мезангиальных клетках человека». Американский журнал нефрологии. 32 (5): 462–468. DOI : 10.1159 / 000321365. PMID 20948191. S2CID 12859943.
- Thompson RC, Herscovitch M, Zhao I., Ford TJ, Gilmore TD (январь 2011 г.). «NF-kappaB подавляет экспрессию маркера CD10 В-лимфомы посредством пути miR-155 / PU.1». Журнал биологической химии. 286 (3): 1675–1682. DOI : 10.1074 / jbc.M110.177063. PMC 3023462. PMID 20947507.
- Ван П, Хоу Дж, Линь Л., Ван С, Лю Х, Ли Д., Ма Ф, Ван З, Цао Х (ноябрь 2010 г.). «Индуцируемая обратная связь микроРНК-155 способствует передаче сигналов IFN типа I в противовирусном врожденном иммунитете путем воздействия на супрессор передачи сигналов цитокинов 1». Журнал иммунологии. 185 (10): 6226–6233. DOI : 10.4049 / jimmunol.1000491. PMID 20937844.
- О'Коннелл Р.М., Кан Д., Гибсон В.С., Раунд JL, Шольц Р.Л., Чаудхури А.А., Кан М.Э., Рао Д.С., Балтимор Д. (октябрь 2010 г.). «МикроРНК-155 способствует аутоиммунному воспалению, усиливая развитие воспалительных Т-клеток». Иммунитет. 33 (4): 607–619. DOI : 10.1016 / j.immuni.2010.09.009. PMC 2966521. PMID 20888269.
- Ся QS, Исигаки Y, Чжао X, Шимасаки Т, Накадзима Х, Накагава Х, Такегами Т, Чен Чж, Мотоо Y (январь 2011 г.). «Человеческий SMG-1 участвует в индуцированной гемцитабином первичной микроРНК-155 / BIC-регуляции в клетках PANC-1 рака поджелудочной железы человека». Поджелудочная железа. 40 (1): 55–60. DOI : 10.1097 / MPA.0b013e3181e89f74. PMID 20871480. S2CID 39789659.
- Чжоу Х, Хуан Х, Цуй Х, Ло Х, Тан И, Чен С., Ву Л, Шен Н. (декабрь 2010 г.). «miR-155 и его звездообразный партнер miR-155 * кооперативно регулируют продукцию интерферона I типа плазматическими дендритными клетками человека». Кровь. 116 (26): 5885–5894. DOI : 10.1182 / кровь-2010-04-280156. PMID 20852130.
- Linnstaedt SD, Gottwein E, Skalsky RL, Luftig MA, Cullen BR (ноябрь 2010 г.). «Вирусно-индуцированная клеточная микроРНК miR-155 играет ключевую роль в иммортализации В-клеток вирусом Эпштейна-Барра». Журнал вирусологии. 84 (22): 11670–11678. DOI : 10,1128 / JVI.01248-10. PMC 2977875. PMID 20844043.
- Чжэн Л., Сюй С.К., Чен В.Д., Шэнь В.Л., Жуань С.К., Чжу Л.М., Чжу Д.Л., Гао П.Дж. (октябрь 2010 г.). «МикроРНК-155 регулирует экспрессию рецептора ангиотензина II типа 1 и фенотипическую дифференциацию в адвентициальных фибробластах сосудов». Сообщения о биохимических и биофизических исследованиях. 400 (4): 483–488. DOI : 10.1016 / j.bbrc.2010.08.067. PMID 20735984.
- Тили Э, Мишай Дж. Дж., Адаир Б., Олдер Х, Лимань Э, Такчиоли С., Феррацин М., Дельмас Д., Латруфф Н., Кроче С. М. (сентябрь 2010 г.). «Ресвератрол снижает уровни miR-155 за счет активации miR-663, микроРНК, нацеленной на JunB и JunD». Канцерогенез. 31 (9): 1561–1566. DOI : 10.1093 / carcin / bgq143. PMC 4647642. PMID 20622002.
- Бош-Саадатманди С., Лобода А., Вагнер А.Е., Стахурска А., Йозкович А., Дулак Дж., Деринг Ф., Вольфрам С., Римбах Г. (март 2011 г.). «Влияние кверцетина и его метаболитов изорамнетина и кверцетин-3-глюкуронида на экспрессию воспалительных генов: роль miR-155». Журнал пищевой биохимии. 22 (3): 293–299. DOI : 10.1016 / j.jnutbio.2010.02.008. PMID 20579867.
- Лю Дж., Ван Мил А., Врийсен К., Чжао Дж., Гао Л., Мец СН, Гуманс М.Дж., Доевенданс П.А., Слуиджтер Дж.П. (июль 2011 г.). «МикроРНК-155 предотвращает некротическую гибель клеток-предшественников кардиомиоцитов человека посредством нацеливания на RIP1». Журнал клеточной и молекулярной медицины. 15 (7): 1474–1482. DOI : 10.1111 / j.1582-4934.2010.01104.x. PMC 3823192. PMID 20550618.
- Погрибный И.П., Старлард-Давенпорт А., Трындяк В.П., Хан Т., Росс С.А., Русин I, Беланд Ф.А. (октябрь 2010 г.). «Разница в экспрессии печеночных микроРНК miR-29c, miR-34a, miR-155 и miR-200b связана со штаммом-специфической восприимчивостью мышей к диетическому неалкогольному стеатогепатиту». Лабораторные исследования. 90 (10): 1437–1446. DOI : 10.1038 / labinvest.2010.113. PMC 4281935. PMID 20548288.
- Чжан И, Дяо З., Су Л, Сун Х, Ли Р, Цуй Х, Ху Й (май 2010 г.). «MicroRNA-155 способствует преэклампсии, подавляя CYR61». Американский журнал акушерства и гинекологии. 202 (5): 466.e1–7. DOI : 10.1016 / j.ajog.2010.01.057. PMID 20452491.
- Ху Ю.Л., Фонг С., Ларгман С., Шен В.Ф. (сентябрь 2010 г.). «HOXA9 регулирует miR-155 в кроветворных клетках». Исследования нуклеиновых кислот. 38 (16): 5472–5478. DOI : 10.1093 / NAR / gkq337. PMC 2938212. PMID 20444872.
- McCoy CE, Sheedy FJ, Qualls JE, Doyle SL, Quinn SR, Murray PJ, O'Neill LA (июль 2010 г.). «IL-10 ингибирует индукцию miR-155 толл-подобными рецепторами». Журнал биологической химии. 285 (27): 20492–20498. DOI : 10.1074 / jbc.M110.102111. PMC 2898307. PMID 20435894.
- Yin Q, Wang X, Fewell C, Cameron J, Zhu H, Baddoo M, Lin Z, Flemington EK (июль 2010 г.). «МикроРНК miR-155 ингибирует передачу сигналов костного морфогенетического белка (BMP) и реактивацию BMP-опосредованного вируса Эпштейна-Барра». Журнал вирусологии. 84 (13): 6318–6327. DOI : 10,1128 / JVI.00635-10. PMC 2903268. PMID 20427544.
- Чжу Дж, Ху XQ, Гуо GL, Чжан Y, Ван О.К., Ю Дж, Хуан QD, Чжан XH (февраль 2010 г.). «[Экспрессия и ее клиническое значение miR-155 при первичном раке груди человека]». Чжунхуа Вай Кэ За Чжи [Китайский журнал хирургии]. 48 (3): 205–208. PMID 20388420.
- Kong W, He L, Coppola M, Guo J, Esposito NN, Coppola D, Cheng JQ (июнь 2010 г.). «MicroRNA-155 регулирует выживаемость, рост и химиочувствительность клеток, воздействуя на FOXO3a при раке груди». Журнал биологической химии. 285 (23): 17869–17879. DOI : 10.1074 / jbc.M110.101055. PMC 2878550. PMID 20371610.
- Ся QS, Исигаки Ю., Сун Л., Чен Р., Мотоу И. (январь 2010 г.). «[Влияние противораковых препаратов на экспрессию BIC / miR-155 в клетках рака поджелудочной железы человека PANC-1]». Чжунхуа И Сюэ За Чжи. 90 (2): 123–127. PMID 20356498.
- Цзян С., Чжан Х.В., Лу М.Х., Хе ХХ, Ли И, Гу Х, Лю М.Ф., Ван Э.Д. (апрель 2010 г.). «MicroRNA-155 действует как OncomiR при раке груди, воздействуя на супрессор гена передачи сигналов цитокина 1». Исследования рака. 70 (8): 3119–3127. DOI : 10.1158 / 0008-5472.CAN-09-4250. PMID 20354188.
- Рю Дж. К., Хонг С. М., Карикари К. А., Хрубан Р. Х., Гоггинс М. Г., Майтра А. (2010). «Аберрантная экспрессия MicroRNA-155 является ранним событием в многоэтапном прогрессировании аденокарциномы поджелудочной железы». Панкреатология. 10 (1): 66–73. DOI : 10.1159 / 000231984. PMC 2865485. PMID 20332664.
- Fabani MM, Abreu-Goodger C, Williams D, Lyons PA, Torres AG, Smith KG, Enright AJ, Gait MJ, Vigorito E (июль 2010 г.). «Эффективное ингибирование функции miR-155 in vivo пептидными нуклеиновыми кислотами». Исследования нуклеиновых кислот. 38 (13): 4466–4475. DOI : 10.1093 / NAR / gkq160. PMC 2910044. PMID 20223773.
- Тан Б., Сяо Б., Лю Цзы, Ли Н, Чжу Э.Д., Ли Б.С., Се К.Х., Чжуан Ю., Цзоу К.М., Мао XH (апрель 2010 г.). «Идентификация MyD88 как новой мишени для miR-155, участвующей в негативной регуляции воспаления, вызванного Helicobacter pylori». Письма FEBS. 584 (8): 1481–1486. DOI : 10.1016 / j.febslet.2010.02.063. PMID 20219467. S2CID 41984991.
- Фасси Фери Л., Кох М., Белоголова Е., Халил Х., Больц С., Калали Б., Молленкопф Х. Дж., Бейджье-Бомпадре М., Карлас А., Шнайдер Т., Чурин Ю., Герхард М., Мейер Т.Ф. (2010). «Helicobacter pylori индуцирует miR-155 в Т-клетках цАМФ-Foxp3-зависимым образом». PLOS ONE. 5 (3): e9500. Bibcode : 2010PLoSO... 5.9500F. DOI : 10.1371 / journal.pone.0009500. PMC 2830477. PMID 20209161.
- Сидоркевич М., Грек М., Йозвяк Б., Майда-Станиславска Е., Пекарска А., Бартковяк Дж. (2010). «Экспрессия предшественника микроРНК-155 в мононуклеарных клетках периферической крови пациентов с гепатитом С после противовирусного лечения». Acta Virologica. 54 (1): 75–78. DOI : 10,4149 / av_2010_01_75. PMID 20201617.
- Гета К., Молотский Н., Герчиков Н., Мор Э, Савион С., Фейн А., Тодер В., Шомрон Н., Торчинский А. (2010). «Тератоген-индуцированные изменения в экспрессии микроРНК-34, микроРНК-125b и микроРНК-155: корреляция с эмбриональным генотипом р53 и фенотипом конечностей». Биология развития BMC. 10: 20. DOI : 10,1186 / 1471-213X-10-20. PMC 2841584. PMID 20170545.
- Рай Д., Ким С.В., Маккеллер М.Р., Дахия П.Л., Агияр Р.К. (февраль 2010 г.). «Нацеливание SMAD5 связывает микроРНК-155 с путем TGF-бета и лимфомагенезом». Труды Национальной академии наук Соединенных Штатов Америки. 107 (7): 3111–3116. Bibcode : 2010PNAS..107.3111R. DOI : 10.1073 / pnas.0910667107. PMC 2840369. PMID 20133617.
- Cremer TJ, Ravneberg DH, Clay CD, Piper-Hunter MG, Marsh CB, Elton TS, Gunn JS, Amer A, Kanneganti TD, Schlesinger LS, Butchar JP, Tridandapani S (2009). «Индукция MiR-155 F. novicida, но не вирулентным F. tularensis, приводит к подавлению SHIP-регуляции и усилению провоспалительного цитокинового ответа». PLOS ONE. 4 (12): e8508. Bibcode : 2009PLoSO... 4.8508C. DOI : 10.1371 / journal.pone.0008508. PMC 2794384. PMID 20041145.
- Forrest AR, Kanamori-Katayama M, Tomaru Y, Lassmann T, Ninomiya N, Takahashi Y, de Hoon MJ, Kubosaki A, Kaiho A, Suzuki M, Yasuda J, Kawai J, Hayashizaki Y, Hume DA, Suzuki H (февраль 2010 г.)). «Индукция микроРНК, mir-155, mir-222, mir-424 и mir-503, способствует дифференцировке моноцитов посредством комбинаторной регуляции». Лейкоз. 24 (2): 460–466. arXiv : 1007.2689. DOI : 10.1038 / leu.2009.246. PMID 19956200. S2CID 2333658.
- Педерсен И.М., Отеро Д., Као Э., Милетик А.В., Хотер С., Ральфкиер Э., Рикерт Р.С., Гронбек К., Дэвид М. (август 2009 г.). «Onco-miR-155 нацелен на SHIP1, чтобы способствовать TNF-зависимому росту В-клеточных лимфом». EMBO Молекулярная медицина. 1 (5): 288–295. DOI : 10.1002 / emmm.200900028. PMC 2771872. PMID 19890474.
- Хэ М., Сюй З., Дин Т., Куанг Д.М., Чжэн Л. (октябрь 2009 г.). «МикроРНК-155 регулирует продукцию воспалительных цитокинов в опухоль-ассоциированных макрофагах посредством нацеливания на C / EBPbeta». Клеточная и молекулярная иммунология. 6 (5): 343–352. DOI : 10.1038 / cmi.2009.45. PMC 4003217. PMID 19887047.
- Тили Э., Кроче СМ, Мишай Дж.Дж. (2009). «miR-155: на стыке воспаления и рака». Международные обзоры иммунологии. 28 (5): 264–284. DOI : 10.1080 / 08830180903093796. PMID 19811312. S2CID 205589961.
- Шталь Х.Ф., Фаути Т., Ульрих Н., Бопп Т., Кубах Дж., Руст В., Лабхарт П., Алексиадис В., Беккер С., Хафнер М., Вейт А., Лентер М.С., Йонулейт Х., Шмитт Э., Меннерих Д. (2009). «Ингибирование miR-155 сенсибилизирует CD4 + Th-клетки для подавления, опосредованного TREG». PLOS ONE. 4 (9): e7158. Bibcode : 2009PLoSO... 4.7158S. DOI : 10.1371 / journal.pone.0007158. PMC 2743997. PMID 19777054.
- Bolisetty MT, Dy G, Tam W, Beemon KL (декабрь 2009 г.). «Штамм вируса ретикулоэндотелиоза Т индуцирует miR-155, который нацелен на JARID2 и способствует выживанию клеток». Журнал вирусологии. 83 (23): 12009–12017. DOI : 10,1128 / JVI.01182-09. PMC 2786729. PMID 19759154.
- Ван Б., Маджумдер С., Нуово Г., Кутай Х., Волиния С., Патель Т., Шмитген Т.Д., Кроче С., Гошал К., Джейкоб С.Т. (октябрь 2009 г.). «Роль микроРНК-155 на ранних стадиях гепатоканцерогенеза, индуцированного холин-дефицитной и аминокислотной диетой у мышей C57BL / 6». Гепатология. 50 (4): 1152–1161. DOI : 10.1002 / hep.23100. PMC 2757532. PMID 19711427.
- Pottier N, Maurin T, Chevalier B, Puisségur MP, Lebrigand K, Robbe-Sermesant K, Bertero T, Lino Cardenas CL, Courcot E, Rios G, Fourre S, Lo-Guidice JM, Marcet B, Cardinaud B, Barbry P, Мари Б (2009). «Идентификация фактора роста кератиноцитов как мишени для микроРНК-155 в фибробластах легких: участие в эпителиально-мезенхимальных взаимодействиях». PLOS ONE. 4 (8): e6718. Bibcode : 2009PLoSO... 4.6718P. DOI : 10.1371 / journal.pone.0006718. PMC 2726943. PMID 19701459.
- Сяо Б., Лю З., Ли Б.С., Тан Б., Ли В., Го Г, Ши И, Ван Ф, Ву И, Тонг В.Д., Гуо Х., Мао XH, Цзоу QM (сентябрь 2009 г.). «Индукция микроРНК-155 во время инфекции Helicobacter pylori и ее отрицательная регулирующая роль в воспалительной реакции». Журнал инфекционных болезней. 200 (6): 916–925. DOI : 10.1086 / 605443. PMID 19650740.
- Ворм Дж., Стенванг Дж., Петри А., Фредериксен К.С., Обад С., Эльмен Дж., Хедтьярн М., Страаруп Е.М., Хансен Дж. Б., Кауппинен С. (сентябрь 2009 г.). «Молчание микроРНК-155 у мышей во время острой воспалительной реакции приводит к дерепрессии c / ebp Beta и подавлению G-CSF». Исследования нуклеиновых кислот. 37 (17): 5784–5792. DOI : 10.1093 / NAR / gkp577. PMC 2761263. PMID 19596814.
- Costinean S, Sandhu SK, Pedersen IM, Tili E, Trotta R, Perrotti D, Ciarlariello D, Neviani P, Harb J, Kauffman LR, Shidham A, Croce CM (август 2009 г.). «Инозитол-5-фосфатаза, содержащая домен с гомологией 2 Src, и белок бета, связывающий энхансер CCAAT, нацелены на miR-155 в B-клетках трансгенных мышей Emicro-MiR-155». Кровь. 114 (7): 1374–1382. DOI : 10.1182 / кровь-2009-05-220814. PMC 2727407. PMID 19520806.
- Ruggiero T, Trabucchi M, De Santa F, Zupo S, Harfe BD, McManus MT, Rosenfeld MG, Briata P, Gherzi R (сентябрь 2009 г.). «ЛПС индуцирует регуляторный белок-зависимый процессинг сплайсинга KH-типа предшественников микроРНК-155 в макрофагах». Журнал FASEB. 23 (9): 2898–2908. DOI : 10.1096 / fj.09-131342. PMID 19423639. S2CID 588328.
- Мартинес-Нуньес RT, Луафи Ф., Фридманн П.С., Санчес-Эльснер Т. (июнь 2009 г.). «МикроРНК-155 модулирует способность дендритных клеток (ДК) связывать патогены путем подавления ДК-специфической молекулы-3 межклеточной адгезии, захватывающей неинтегрин (DC-SIGN)». Журнал биологической химии. 284 (24): 16334–16342. DOI : 10.1074 / jbc.M109.011601. PMC 2713543. PMID 19386588.
- О'Коннелл Р.М., Чаудхури А.А., Рао Д.С., Балтимор Д. (апрель 2009 г.). «Инозитолфосфатаза SHIP1 является основной мишенью miR-155». Труды Национальной академии наук Соединенных Штатов Америки. 106 (17): 7113–7118. Bibcode : 2009PNAS..106.7113O. DOI : 10.1073 / pnas.0902636106. PMC 2678424. PMID 19359473.
- Kohlhaas S, Garden OA, Scudamore C, Turner M, Okkenhaug K, Vigorito E (март 2009 г.). «Передний край: miR-155-мишень Foxp3 способствует развитию регуляторных Т-клеток». Журнал иммунологии. 182 (5): 2578–2582. DOI : 10.4049 / jimmunol.0803162. PMID 19234151.
- Сеппи М., Перейра П.М., Дунанд-Сотье И., Баррас Э., Райт В., Сантос М.А., Пьер П. (февраль 2009 г.). «МикроРНК-155 модулирует путь передачи сигнала интерлейкина-1 в активированных дендритных клетках человека, происходящих из моноцитов». Труды Национальной академии наук Соединенных Штатов Америки. 106 (8): 2735–2740. Bibcode : 2009PNAS..106.2735C. DOI : 10.1073 / pnas.0811073106. PMC 2650335. PMID 19193853.
- Habbe N, Koorstra JB, Mendell JT, Offerhaus GJ, Ryu JK, Feldmann G, Mullendore ME, Goggins MG, Hong SM, Maitra A (февраль 2009 г.). «МикроРНК miR-155 - биомаркер ранней неоплазии поджелудочной железы». Биология и терапия рака. 8 (4): 340–346. DOI : 10,4161 / cbt.8.4.7338. PMC 2692997. PMID 19106647.
- Юнг И., Агияр RC (январь 2009 г.). «Экспрессия MicroRNA-155 и результат в диффузной большой B-клеточной лимфоме». Британский журнал гематологии. 144 (1): 138–140. DOI : 10.1111 / j.1365-2141.2008.07424.x. PMC 4654117. PMID 19016736.
- Румыния П., Лулли В., Пелози Е., Биффони М., Пешле С., Марциали Г. (ноябрь 2008 г.). «МикроРНК 155 модулирует мегакариопоэз на уровне предшественников и предшественников, воздействуя на факторы транскрипции Ets-1 и Meis1». Британский журнал гематологии. 143 (4): 570–580. DOI : 10.1111 / j.1365-2141.2008.07382.x. PMID 18950466. S2CID 9025761.
- Чжао Й, Яо Й, Сюй Х, Ламбет Л., Смит Л. П., Кгосана Л., Ван Х, Наир В. (январь 2009 г.). «Функциональный ортолог MicroRNA-155, кодируемый онкогенным вирусом болезни Марека». Журнал вирусологии. 83 (1): 489–492. DOI : 10,1128 / JVI.01166-08. PMC 2612317. PMID 18945769.
- Гатто Г., Росси А., Росси Д., Кроенинг С., Бонатти С., Маллардо М. (ноябрь 2008 г.). «Латентный мембранный белок 1 вируса Эпштейна-Барра трансактивирует транскрипцию miR-155 через путь NF-kappaB». Исследования нуклеиновых кислот. 36 (20): 6608–6619. DOI : 10.1093 / NAR / gkn666. PMC 2582607. PMID 18940871.
- Рахадиани Н., Такакува Т., Треснасари К., Мори Е., Аозаса К. (декабрь 2008 г.). «Скрытый мембранный белок-1 вируса Эпштейна-Барра индуцирует экспрессию кластера интеграции В-клеток, предшественника микроРНК-155, в клеточных линиях В-лимфомы». Сообщения о биохимических и биофизических исследованиях. 377 (2): 579–583. DOI : 10.1016 / j.bbrc.2008.10.007. PMID 18926796.
- Kong W, Yang H, He L, Zhao JJ, Coppola D, Dalton WS, Cheng JQ (ноябрь 2008 г.). «MicroRNA-155 регулируется путем трансформирующего фактора роста бета / Smad и способствует пластичности эпителиальных клеток, воздействуя на RhoA». Молекулярная и клеточная биология. 28 (22): 6773–6784. DOI : 10.1128 / MCB.00941-08. PMC 2573297. PMID 18794355.
- Лу Ф., Вайдмер А., Лю К. Г., Волиния С., Кроче С. М., Либерман П. М. (ноябрь 2008 г.). «Индуцированная вирусом Эпштейна-Барра miR-155 ослабляет передачу сигналов NF-kappaB и стабилизирует латентную персистентность вируса». Журнал вирусологии. 82 (21): 10436–10443. DOI : 10,1128 / JVI.00752-08. PMC 2573162. PMID 18753206.
- Дорсетт Y, Макбрайд К.М., Янкович М., Газумян А., Тай TH, Роббиани Д.Ф., Ди Вирджилио М., Рейна Сан-Мартин Б., Хайдкамп Г., Швикерт Т.А., Айзенрайх Т., Раевски К., Нуссенцвейг М.С. (май 2008 г.). «МикроРНК-155 подавляет вызванную активацией цитидиндезаминазу-опосредованную транслокацию Myc-Igh». Иммунитет. 28 (5): 630–638. DOI : 10.1016 / j.immuni.2008.04.002. PMC 2713656. PMID 18455451.
- Teng G, Hakimpour P, Landgraf P, Rice A, Tuschl T., Casellas R, Papavasiliou FN (май 2008 г.). «МикроРНК-155 является негативным регулятором цитидиндезаминазы, индуцированной активацией». Иммунитет. 28 (5): 621–629. DOI : 10.1016 / j.immuni.2008.03.015. PMC 2430982. PMID 18450484.
- Инь Кью, Макбрайд Дж., Фьюэлл К., Лейси М., Ван Х, Лин З, Кэмерон Дж., Флемингтон Е.К. (июнь 2008 г.). «МикроРНК-155 представляет собой индуцированный вирусом Эпштейна-Барр ген, который модулирует регулируемые вирусом Эпштейна-Барра пути экспрессии генов». Журнал вирусологии. 82 (11): 5295–5306. DOI : 10,1128 / JVI.02380-07. PMC 2395216. PMID 18367535.
- Чжан Т., Не К., Там В. (сентябрь 2008 г.). «BIC эффективно обрабатывается до микроРНК-155 в клетках лимфомы Беркитта». Лейкоз. 22 (9): 1795–1797. DOI : 10.1038 / leu.2008.62. PMID 18354490.
- Ван М., Тан Л.П., Дейкстра М.К., ван Лом К., Робертус Дж. Л., Хармс Дж., Блокзейл Т., Коойстра К., ван Тверь МБ, Розати С., Виссер Л., Йонген-Лавренчич М., Клюин П.М., ван ден Берг А. ( Май 2008 г.). «Анализ miRNA при В-клеточном хроническом лимфоцитарном лейкозе: центры пролиферации, характеризующиеся низкой экспрессией miR-150 и высокой экспрессией BIC / miR-155». Журнал патологии. 215 (1): 13–20. DOI : 10.1002 / path.2333. PMID 18348159. S2CID 29470560.
- О'Коннелл Р.М., Рао Д.С., Чаудхури А.А., Болдин М.П., Таганов К.Д., Николл Дж., Пакетт Р.Л., Балтимор Д. (март 2008 г.). «Устойчивая экспрессия микроРНК-155 в гемопоэтических стволовых клетках вызывает миелопролиферативное расстройство». Журнал экспериментальной медицины. 205 (3): 585–594. DOI : 10,1084 / jem.20072108. PMC 2275382. PMID 18299402.
- Рай Д., Каранти С., Юнг И., Дахия П.Л., Агияр Р.К. (февраль 2008 г.). «Скоординированная экспрессия микроРНК-155 и предсказанные гены-мишени в диффузной большой B-клеточной лимфоме». Генетика и цитогенетика рака. 181 (1): 8–15. DOI : 10.1016 / j.cancergencyto.2007.10.008. PMC 2276854. PMID 18262046.
- Gottwein E, Mukherjee N, Sachse C, Frenzel C, Majoros WH, Chi JT, Braich R, Manoharan M, Soutschek J, Ohler U, Cullen BR (декабрь 2007 г.). «Вирусная микроРНК функционирует как ортолог клеточного miR-155». Природа. 450 (7172): 1096–1099. Bibcode : 2007Natur.450.1096G. DOI : 10,1038 / природа05992. PMC 2614920. PMID 18075594.
- Вигорито Э., Перкс К.Л., Абреу-Гуджер С., Бантинг С., Сян З., Кольхаас С., Дас П.П., Миска Е.А., Родригес А., Брэдли А., Смит К.Г., Рада С., Энрайт А.Дж., Толлнер К.М., Макленнан И.С., Тернер М. ( Декабрь 2007 г.). «микроРНК-155 регулирует образование плазматических клеток с переключенным классом иммуноглобулинов». Иммунитет. 27 (6): 847–859. DOI : 10.1016 / j.immuni.2007.10.009. PMC 4135426. PMID 18055230.
- Инь Кью, Ван Х, Макбрайд Дж., Фьюэлл С., Флемингтон Э. (февраль 2008 г.). «Активация В-клеточного рецептора вызывает экспрессию BIC / miR-155 через консервативный элемент AP-1». Журнал биологической химии. 283 (5): 2654–2662. DOI : 10.1074 / jbc.M708218200. PMC 2810639. PMID 18048365.
- Тили Э., Мишай Дж. Дж., Чимино А., Костинян С., Думитру С. Д., Адаир Б., Фаббри М., Альдер Х., Лю К. Г., Калин Г. А., Кроче С. М. (октябрь 2007 г.). «Модуляция уровней miR-155 и miR-125b после стимуляции липополисахаридом / TNF-альфа и их возможная роль в регулировании ответа на эндотоксиновый шок». Журнал иммунологии. 179 (8): 5082–5089. DOI : 10.4049 / jimmunol.179.8.5082. PMID 17911593.
- Gironella M, Seux M, Xie MJ, Cano C, Tomasini R, Gommeaux J, Garcia S, Nowak J, Yeung ML, Jeang KT, Chaix A, Fazli L, Motoo Y, Wang Q, Rocchi P, Russo A, Gleave M, Дагорн Дж. К., Иованна Дж. Л., Перевозчик А, Пебуск М. Дж., Дюзетти, штат Нью-Джерси (октябрь 2007 г.). «Экспрессия ядерного белка 1, индуцированная опухолевым белком 53, подавляется miR-155, и ее восстановление ингибирует развитие опухоли поджелудочной железы». Труды Национальной академии наук Соединенных Штатов Америки. 104 (41): 16170–16175. Bibcode : 2007PNAS..10416170G. DOI : 10.1073 / pnas.0703942104. PMC 2042180. PMID 17911264.
- Скальский Р.Л., Самолс М.А., Плезанс КБ, Босс И.В., Рива А., Лопес М.С., Бейкер Х.В., Ренне Р. (декабрь 2007 г.). «Связанный с саркомой герпесвирус Капоши кодирует ортолог miR-155». Журнал вирусологии. 81 (23): 12836–12845. DOI : 10,1128 / JVI.01804-07. PMC 2169101. PMID 17881434.
- Сетупати П., Борел С., Гагнебин М., Грант Г.Р., Дойч С., Элтон Т.С., Хатцигеоргиу А.Г., Антонаракис С.Е. (август 2007 г.). «Человеческая микроРНК-155 на хромосоме 21 дифференциально взаимодействует со своей полиморфной мишенью в 3'-нетранслируемой области AGTR1: механизм функциональных однонуклеотидных полиморфизмов, связанных с фенотипами». Американский журнал генетики человека. 81 (2): 405–413. DOI : 10.1086 / 519979. PMC 1950808. PMID 17668390.
- Мартин М.М., Бакенбергер Дж. А., Цзян Дж., Малана Г. Дж., Нуово Дж. Дж., Чотани М., Фельдман Д. С., Шмитген Т. Д., Элтон Т. С. (август 2007 г.). «Полиморфизм A / C рецептора ангиотензина II типа 1 человека +1166 ослабляет связывание микроРНК-155». Журнал биологической химии. 282 (33): 24262–24269. DOI : 10.1074 / jbc.M701050200. PMC 2413065. PMID 17588946.
- Родригес А., Вигорито Е., Клэр С., Уоррен М. В., Кутте П., Сонд Д. Р., ван Донген С., Грокок Р. Дж., Дас П. П., Миска Е. А., Ветри Д., Оккенхауг К., Энрайт А. Дж., Дуган Г., Тернер М., Брэдли А. (апр. 2007). «Потребность в bic / microRNA-155 для нормальной иммунной функции». Наука. 316 (5824): 608–611. Bibcode : 2007Sci... 316..608R. DOI : 10.1126 / science.1139253. PMC 2610435. PMID 17463290.
- Thai TH, Calado DP, Casola S, Ansel KM, Xiao C, Xue Y, Murphy A, Frendewey D, Valenzuela D, Kutok JL, Schmidt-Supprian M, Rajewsky N, Yancopoulos G, Rao A, Rajewsky K (апрель 2007 г.). «Регуляция ответа зародышевого центра с помощью микроРНК-155». Наука. 316 (5824): 604–608. Bibcode : 2007Sci... 316..604T. DOI : 10.1126 / science.1141229. PMID 17463289. S2CID 8174458.
- О'Коннелл Р.М., Таганов К.Д., Болдин М.П., Ченг Г., Балтимор Д. (январь 2007 г.). «МикроРНК-155 индуцируется во время воспалительной реакции макрофагов». Труды Национальной академии наук Соединенных Штатов Америки. 104 (5): 1604–1609. Bibcode : 2007PNAS..104.1604O. DOI : 10.1073 / pnas.0610731104. PMC 1780072. PMID 17242365.
- Мартин М.М., Ли Э.Дж., Бакенбергер Дж.А., Шмитген Т.Д., Элтон Т.С. (июль 2006 г.). «МикроРНК-155 регулирует экспрессию рецептора ангиотензина II типа 1 человека в фибробластах». Журнал биологической химии. 281 (27): 18277–18284. DOI : 10.1074 / jbc.M601496200. PMID 16675453.
- Чунг К.Х., Харт С.С., Аль-Бассам С., Эйвери А., Тейлор Дж., Пател П.Д., Войтек А.Б., Тернер Д.Л. (2006). «Экспрессионные векторы полицистронной РНК-полимеразы II для РНК-интерференции на основе BIC / miR-155». Исследования нуклеиновых кислот. 34 (7): e53. DOI : 10.1093 / NAR / gkl143. PMC 1435982. PMID 16614444.
- Там В., Дальберг Дж. Э. (февраль 2006 г.). «miR-155 / BIC как онкогенная микроРНК». Гены, хромосомы и рак. 45 (2): 211–212. DOI : 10.1002 / gcc.20282. PMID 16252262. S2CID 8513721.
- Клювер Дж., Хараламбиева Е., де Йонг Д., Блокзейл Т., Якобс С., Крузен Б. Дж., Поппема С., ван ден Берг А. (февраль 2006 г.). «Отсутствие экспрессии BIC и микроРНК miR-155 в первичных случаях лимфомы Беркитта». Гены, хромосомы и рак. 45 (2): 147–153. DOI : 10.1002 / gcc.20273. PMID 16235244. S2CID 16897980.
- Цзян Дж., Ли Э.Дж., Шмитген Т.Д. (январь 2006 г.). «Повышенная экспрессия микроРНК-155 в линиях лимфобластоидных клеток, трансформированных вирусом Эпштейна-Барра». Гены, хромосомы и рак. 45 (1): 103–106. DOI : 10.1002 / gcc.20264. PMID 16175574. S2CID 19138209.
- Kluiver J, Poppema S, de Jong D, Blokzijl T, Harms G, Jacobs S, Kroesen BJ, van den Berg A (октябрь 2005 г.). «BIC и miR-155 высоко экспрессируются в лимфомах Ходжкина, первичных средостенных и диффузных больших В-клеточных лимфомах». Журнал патологии. 207 (2): 243–249. DOI : 10.1002 / path.1825. PMID 16041695. S2CID 14329069.
- Eis PS, Tam W, Sun L, Chadburn A, Li Z, Gomez MF, Lund E, Dahlberg JE (март 2005 г.). «Накопление miR-155 и BIC РНК в человеческих В-клеточных лимфомах». Труды Национальной академии наук Соединенных Штатов Америки. 102 (10): 3627–3632. Bibcode : 2005PNAS..102.3627E. DOI : 10.1073 / pnas.0500613102. PMC 552785. PMID 15738415.
- Мецлер М., Вильда М., Буш К., Фиманн С., Боркхардт А. (февраль 2004 г.). «Высокая экспрессия предшественника микроРНК-155 / BIC РНК у детей с лимфомой Беркитта». Гены, хромосомы и рак. 39 (2): 167–169. DOI : 10.1002 / gcc.10316. PMID 14695998. S2CID 10009892.
внешние ссылки
 pre-mir-155 вторичная структура и сохранение последовательности.
pre-mir-155 вторичная структура и сохранение последовательности. Рисунок 1. Схематическое изображение MIR155HG (инвентарный номер NC_000021). Этот ген занимает 13024 п.н., состоит из трех экзонов и кодирует некодирующую первичную миРНК (pri-miRNA) размером 1500 п.н. (номер доступа NR_001458). Расположение пре-Мир-155 обозначено оранжевой рамкой.
Рисунок 1. Схематическое изображение MIR155HG (инвентарный номер NC_000021). Этот ген занимает 13024 п.н., состоит из трех экзонов и кодирует некодирующую первичную миРНК (pri-miRNA) размером 1500 п.н. (номер доступа NR_001458). Расположение пре-Мир-155 обозначено оранжевой рамкой.  Рисунок 2. Последовательность стволовой петли pre-mir-155, которая созревает из транскрипта pri-miRNA. Последовательность зрелой miR-155 (miR-155-5p) показана зеленым, а последовательность зрелой miR-155 * (miR-155-3p) показана красным.
Рисунок 2. Последовательность стволовой петли pre-mir-155, которая созревает из транскрипта pri-miRNA. Последовательность зрелой miR-155 (miR-155-5p) показана зеленым, а последовательность зрелой miR-155 * (miR-155-3p) показана красным.  Рисунок 4. Дополнительные спаривания оснований между MIR-155-5p и человеческого SPI1 (селезенку фокус вируса, образующего провирусной интеграции онкоген) (также известный как PU.1) мРНК. Сайт связывания miR-155-5p расположен на 46–53 парах оснований ниже стоп-кодона мРНК SPI1. Необходимая пара оснований «исходной последовательности» обозначена жирным тире.
Рисунок 4. Дополнительные спаривания оснований между MIR-155-5p и человеческого SPI1 (селезенку фокус вируса, образующего провирусной интеграции онкоген) (также известный как PU.1) мРНК. Сайт связывания miR-155-5p расположен на 46–53 парах оснований ниже стоп-кодона мРНК SPI1. Необходимая пара оснований «исходной последовательности» обозначена жирным тире.