РНК-индуцированный комплекс сайленсинга, или RISC, представляет собой мультипротеиновый комплекс, в частности рибонуклеопротеин, который включает одну цепь одноцепочечного фрагмента РНК (оцРНК), такого как микроРНК ( миРНК) или двухцепочечной малой интерферирующей РНК (миРНК). Однонить действует как шаблон для RISC для распознавания комплементарной информационной РНК (мРНК) транскрипта. После обнаружения один из белков в RISC, называемый Argonaute, активирует и расщепляет мРНК. Этот процесс называется РНК-интерференцией (РНКи), и он обнаруживается у многих эукариот ; это ключевой процесс подавления гена и защиты от вирусных инфекций.
Биохимическая идентификация RISC была проведена Грегори Хэнноном и его коллегами в лаборатории Колд-Спринг-Харбор. Это произошло всего через пару лет после открытия РНК-интерференции в 1998 году Эндрю Файром и Крейгом Мелло, которые разделили Нобелевскую премию по физиологии и медицине 2006 года.
 Drosophila melanogaster
Drosophila melanogaster Хэннон и его коллеги попытались идентифицировать механизмы РНКи, участвующие в сайленсинге гена дцРНК в клетках Drosophila. Клетки Drosophila S2 были трансфицированы экспрессионным вектором lacZ для количественной оценки экспрессии гена с помощью β- активность галактозидазы. Их результаты показали, что котрансфекция lacZ дцРНК значительно снижает активность β-галактозидазы по сравнению с контрольной дцРНК. Следовательно, дцРНК контролируют экспрессию гена через последовательность комплементарности.
. Затем клетки S2 трансфецировали дцРНК Drosophila циклином E. Циклин E является важным геном для перехода клеточного цикла в фазу S. Циклин E дцРНК остановил клеточный цикл на G1фазе (перед S-фазой). Следовательно, РНКи могут нацеливаться на эндогенные гены.
Кроме того, дцРНК циклина E только уменьшала РНК циклина E - аналогичный результат был также показан с использованием дцРНК, соответствующей циклину A, который действует в S, G2 и M фаз клеточного цикла. Это показывает характерный признак РНКи: пониженные уровни мРНК соответствуют уровням добавленной дцРНК.
Чтобы проверить, является ли наблюдаемое ими снижение уровней мРНК результатом прямого воздействия на мРНК (как предполагают данные из других систем), клетки S2 дрозофилы трансфицировали дцРНК циклина E дрозофилы или дцРНК lacZ и затем инкубировали с синтетическими мРНК для циклина E или lacZ.
Клетки, трансфицированные дцРНК циклина E, демонстрировали деградацию только транскриптов циклина E - транскрипты lacZ были стабильными. Напротив, клетки, трансфицированные дцРНК lacZ, демонстрировали деградацию только транскриптов lacZ, но не транскриптов циклина E. Их результаты привели Хэннона и его коллег к предположению, что РНКи разлагает мРНК-мишень за счет «специфичной для последовательности нуклеазной активности». Они назвали нуклеазу ферментом RISC.
 Домен PIWI белка Argonaute в комплексе с двухцепочечной РНК.
Домен PIWI белка Argonaute в комплексе с двухцепочечной РНК. РНКаза III Dicer помогает RISC в РНК-интерференции, расщепляя дцРНК на 21-23 нуклеотидные длинные фрагменты с двухнуклеотидным 3 ' свес. Эти фрагменты дцРНК загружаются в RISC, и каждая цепь имеет различную судьбу на основе феномена правила асимметрии.
 Часть пути интерференции РНК с различными способами, которыми RISC может заглушить гены через своего мессенджера РНК.
Часть пути интерференции РНК с различными способами, которыми RISC может заглушить гены через своего мессенджера РНК. RISC использует связанную направляющую цепь для нацеливания на комплементарные 3'-нетранслируемые области (3'UTR) транскриптов мРНК с помощью пары оснований Уотсона-Крика. RISC теперь может регулировать экспрессию генов транскрипта мРНК несколькими способами.
Наиболее понятной функцией RISC является деградация целевой мРНК, которая снижает уровни транскрипта, доступного для трансляции с помощью рибосом. Существует два основных требования для деградации мРНК:
деградация мРНК локализована в цитоплазматических телах, называемых P-тельцами.
RISC может модулировать загрузку рибосом и дополнительных факторов в трансляции в подавляют экспрессию связанного транскрипта мРНК. Репрессия трансляции требует только частичного совпадения последовательностей между направляющей цепью и целевой мРНК.
Трансляция может регулироваться на этапе инициации посредством:
Трансляция может регулироваться на этапах после инициации посредством:
До сих пор существуют предположения о том, является ли репрессия трансляции через инициацию и пост-инициацию взаимоисключающей.
Некоторые RISC способны напрямую нацеливаться на геном, рекрутируя гистоновые метилтрансферазы для образования гетерохроматина в ген локус и, таким образом, подавление гена. Эти RISC принимают форму РНК-индуцированного комплекса подавления транскрипции (RITS). Наиболее изученным примером является дрожжевой RITS.
Механизм не совсем понятен, но RITS разрушают растущие транскрипты мРНК. Было высказано предположение, что этот механизм действует как «самоусиливающаяся петля обратной связи », поскольку деградированные растущие транскрипты используются РНК-зависимой РНК-полимеразой (RdRp) для генерации большего количества миРНК.
RISC, по-видимому, играют роль в деградации ДНК во время соматического развития макронуклеуса у простейших Tetrahymena. Это похоже на образование гетерохроматина и подразумевается как защита от вторжения генетических элементов.
Полная структура RISC все еще не решена. Во многих исследованиях сообщается о диапазоне размеров и компонентов для RISC, но не совсем ясно, связано ли это с наличием ряда комплексов RISC или с различными источниками, которые используются в различных исследованиях.
| Сложный | Источник | Известные / очевидные компоненты | Расчетный размер | Видимая функция в пути РНКи |
|---|---|---|---|---|
| Dcr2-R2D2 | D. клетки S2 melanogaster | Dcr2, | ~ 250 кДа | Процессинг дцРНК, связывание миРНК |
| RLC (A) | D. melanogaster эмбрионы | Dcr2, R2D2 | NR | процессинг дцРНК, связывание миРНК, предшественник RISC |
| Holo-RISC | D. melanogaster эмбрионы | назад 2, Dcr1, Dcr2, Fmr1 / Fxr, R2D2, Tsn, | ~80S | Target- Связывание и расщепление РНК |
| RISC | D. клетки S2 melanogaster | Ago2, Fmr1 / Fxr, Tsn, Vig | ~ 500 кДа | Связывание и расщепление РНК-мишени |
| RISC | D. клетки S2 melanogaster | Ago2 | ~ 140 кДа | Связывание и расщепление целевой РНК |
| Fmr1-ассоциированный комплекс | D. клетки S2 melanogaster | L5, L11, 5S рРНК, Fmr1 / Fxr, Ago2, Dmp68 | NR | Возможное связывание и расщепление целевой РНК |
| Минимальный RISC | HeLa клеток | eIF2C1 (Ago1) или eIF2C2 (Ago2) | ~ 160 кДа | Связывание и расщепление целевой РНК |
| miRNP | HeLa клетки | eIF2C2 (ago2), Gemin3, Gemin4 | ~ 550 кДа | ассоциация миРНК, связывание и расщепление целевой РНК |
назад, Аргонавт; Dcr, Dicer; Dmp68, ортолог D. melanogaster РНК-развиндазы p68 млекопитающих; eIF2C1, фактор инициации трансляции эукариот 2C1; eIF2C2, фактор инициации трансляции эукариот 2C2; Fmr1 / Fxr, ортолог D. melanogaster белка умственной отсталости fragile-X; miRNP, комплекс miRNA-белок; NR, не сообщается; Цн, Тюдор-стафилококковая нуклеаза; Vig, интронный ген vasa.
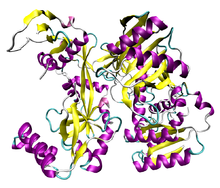 Полноразмерный белок аргонавта из архей вида Pyrococcus furiosus.
Полноразмерный белок аргонавта из архей вида Pyrococcus furiosus. Несмотря на это, очевидно, что белки Argonaute присутствуют и необходимы для функционирования. Кроме того, есть сведения о некоторых ключевых белках (помимо Argonaute) внутри комплекса, которые позволяют RISC выполнять свои функции.
Белки аргонавтов представляют собой семейство белков, обнаруженных в прокариотах и эукариотах. Их функция у прокариот неизвестна, но у эукариот они отвечают за РНКи. У человека Argonautes восемь членов семейства, из которых только Argonaute 2 участвует исключительно в целевом расщеплении РНК в RISC.
 Комплекс загрузки RISC позволяет загружать фрагменты дцРНК (генерируемые Dicer) в Argonaute 2 (с с помощью TRBP) как часть пути интерференции РНК.
Комплекс загрузки RISC позволяет загружать фрагменты дцРНК (генерируемые Dicer) в Argonaute 2 (с с помощью TRBP) как часть пути интерференции РНК. RISC-нагружающий комплекс (RLC) является важной структурой, необходимой для загрузки дцРНК-фрагментов в RISC с целью нацеливания на мРНК. RLC состоит из дайсера, трансактивирующего РНК-связывающего белка (TRBP ) и Argonaute 2.
Dicer связывается с TRBP и Argonaute 2 для облегчения переноса фрагментов дцРНК, генерируемых Dicer, в Argonaute 2.
Более недавние исследования показали, что человеческая РНК-геликаза A может способствовать RLC.
Недавно идентифицированными членами RISC являются SND1 и MTDH. SND1 и MTDH являются онкогенами и регулируют экспрессию различных генов.
| Protein | Виды белок обнаружен |
|---|---|
| Dcr1 | D. melanogaster |
| Dcr2 | D. melanogaster |
| R2D2 | D. melanogaster |
| Ago2 | D. melanogaster |
| Dmp68 | D. melanogaster |
| Fmr1/Fxr | D. melanogaster |
| Цн | Д. melanogaster |
| Виг | Д. melanogaster |
| Полирибосомы, компоненты рибосом | D. melanogaster, Т. brucei |
| eIF2C1 (Назад1) | H. sapiens |
| eIF2C2 (Назад2) | H. sapiens |
| Gemin3 | H. sapiens |
| Близнецы4 | H. sapiens |
Аго, Аргонавт; Dcr, Dicer; Dmp68, ортолог D. melanogaster РНК-развиндазы p68 млекопитающих; eIF2C1, фактор инициации трансляции эукариот 2C1; eIF2C2, фактор инициации трансляции эукариот 2C2; Fmr1 / Fxr, ортолог D. melanogaster белка умственной отсталости fragile-X; Цн, Тюдор-стафилококковая нуклеаза; Vig, интронный ген vasa.
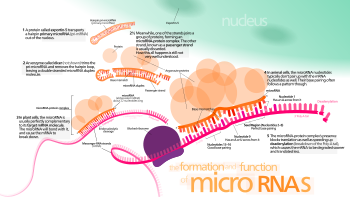 Диаграмма активности RISC с миРНК
Диаграмма активности RISC с миРНК Пока неясно, как активированный комплекс RISC определяет местоположение мРНК-мишеней в клетке, хотя было показано, что этот процесс может происходить в ситуациях, не связанных с продолжающейся трансляцией белка с мРНК.
Эндогенно экспрессируемая миРНК у многоклеточных животных обычно не идеально комплементарна большому количеству генов и, таким образом, они модулируют экспрессию посредством репрессии трансляции. Однако в растениях этот процесс имеет гораздо большую специфичность в отношении мРНК-мишени, и обычно каждая миРНК связывается только с одной мРНК. Большая специфичность означает, что деградация мРНК более вероятна.