lactose operon (lac operon) представляет собой оперон, необходимый для транспорта и метаболизма лактозы в кишечной палочке и многих других кишечных бактериях. Хотя глюкоза является предпочтительным источником углерода для большинства бактерий, lac-оперон обеспечивает эффективное переваривание лактозы, когда глюкоза недоступна благодаря активности бета-галактозидазы. Ген регуляция lac-оперона была первым генетическим регуляторным механизмом, который необходимо четко понять, поэтому он стал передовым примером прокариотической регуляции гена. По этой причине это часто обсуждается на вводных курсах молекулярной и клеточной биологии. Эту систему метаболизма лактозы использовали Франсуа Жакоб и Жак Моно, чтобы определить, как биологическая клетка знает, какой фермент синтезировать. Их работа над lac-опероном принесла им Нобелевскую премию по физиологии в 1965 году.
Бактериальные опероны - это полицистронные транскрипты, которые способны производить множественные белки из одного транскрипта мРНК. В этом случае, когда лактоза требуется в качестве источника сахара для бактерии, могут экспрессироваться три гена оперона lac и транслироваться их последующие белки: lacZ, lacY и lacA. Продуктом гена lacZ является β-галактозидаза, которая расщепляет лактозу, дисахарид, на глюкозу и галактозу. lacY кодирует бета-галактозид пермеазу, мембранный белок, который внедряется в цитоплазматическую мембрану, обеспечивая клеточный транспорт лактозы в ячейка. Наконец, lacA кодирует галактозидацетилтрансферазу.

 lac-оперон. Вверху: репрессировано, внизу: активно.. 1: РНК-полимераза, 2: Репрессор, 3: Промотор, 4: Оператор, 5: Лактоза, 6: lacZ, 7: lacY, 8: lacA.
lac-оперон. Вверху: репрессировано, внизу: активно.. 1: РНК-полимераза, 2: Репрессор, 3: Промотор, 4: Оператор, 5: Лактоза, 6: lacZ, 7: lacY, 8: lacA. Было бы расточительно производить ферменты, когда нет лактозы или если есть предпочтительный источник энергии, такой как глюкоза. Lac-оперон использует двухкомпонентный механизм контроля, чтобы гарантировать, что клетка расходует энергию, производя ферменты, кодируемые lac-опероном, только при необходимости. В отсутствие лактозы lac-репрессор, lacI, останавливает производство ферментов, кодируемых lac-опероном. Lac-репрессор всегда экспрессируется, если с ним не связывается соиндуктор. Другими словами, он транскрибируется только в присутствии низкомолекулярного соиндуктора. В присутствии глюкозы белок-активатор катаболита (CAP), необходимый для выработки ферментов, остается неактивным, а EIIA отключает пермеазу лактозы, чтобы предотвратить перенос лактозы в клетку.. Этот механизм двойного контроля вызывает последовательное использование глюкозы и лактозы в двух различных фазах роста, известных как diauxie.
 Структура лактозы и продуктов ее расщепления.
Структура лактозы и продуктов ее расщепления. Только lacZ и lacY, по-видимому, необходимы для лактозы катаболизма.
Для описания фенотипов бактерий, включая E. coli, используются трехбуквенные сокращения.
Примеры включают:
В случае Lac клетки дикого типа являются Lac и могут использовать лактозу в качестве источника углерода и энергии, в то время как мутантные производные Lac не могут использовать лактозу. Обычно используются те же три буквы (строчные, курсив) для обозначения генов, участвующих в конкретном фенотипе, где каждый другой ген дополнительно выделяется дополнительной буквой. Ферменты lac-генами кодируют lacZ, lacY и lacA. четвертый ген lac - это lacI, кодирующий репрессор лактозы - «I» означает индуцибельность.
Можно различать структурные гены, кодирующие ферменты, и регуляторные гены, кодирующие белки, которые влияют на экспрессию генов. Текущее использование расширяет фенотипическую номенклатуру до применимы к белкам: таким образом, LacZ является белковым продуктом гена lacZ, β-галактозидазы. Различные короткие последовательности, которые не являются генами, также влияют на экспрессию генов, включая промотор lac, lac p, и оператор lac, lac o. Хотя это не является строго стандартным использованием, мутации, влияющие на lac o, по историческим причинам называются lac o.
Конкретный контроль генов lac зависит от доступности субстрата лактозы для бактерии. Белки не производятся бактериями, когда лактоза недоступна в качестве источника углерода. Гены lac организованы в оперон ; то есть они ориентированы в одном и том же направлении, непосредственно примыкающем к хромосоме, и транскрибируются в единую полицистронную молекулу мРНК. Транскрипция всех генов начинается со связывания фермента РНК-полимеразы (RNAP), ДНК-связывающего белка, который связывается со специфическим участком связывания ДНК, промотором , непосредственно перед генами. Связыванию РНК-полимеразы с промотором способствует cAMP -связанный белок-активатор катаболита (CAP, также известный как рецепторный белок цАМФ). Однако ген lacI (регуляторный ген для lac оперона) продуцирует белок, который блокирует связывание РНКП с оператором оперона. Этот белок может быть удален только тогда, когда аллолактоза связывается с ним и инактивирует его. Белок, который образуется геном lacI, известен как lac-репрессор. Тип регуляции, которому подвергается lac-оперон, называется отрицательно индуцибельным, что означает, что ген отключается регуляторным фактором (lac-репрессором), если не добавляется какая-либо молекула (лактоза). Из-за наличия белка-репрессора lac генные инженеры, заменяющие ген lacZ другим геном, должны будут выращивать экспериментальные бактерии на агаре с доступной на нем лактозой. В противном случае ген, который они пытаются экспрессировать, не будет экспрессироваться, поскольку белок-репрессор все еще блокирует связывание RNAP с промотором и транскрибирование гена. После удаления репрессора РНКП затем переходит к транскрипции всех трех генов (lacZYA) в мРНК. Каждый из трех генов в цепи мРНК имеет свою собственную последовательность Шайна-Далгарно, поэтому гены транслируются независимо. Последовательность ДНК E. coli lac оперон, lacZYA мРНК и гены lacI доступны в GenBank (просмотр).
Первый механизм контроля является регуляторным ответом на лактозу, который использует внутриклеточный регуляторный белок, называемый репрессором лактозы, чтобы препятствовать выработке β-галактозидазы в отсутствие лактозы. Ген lacI, кодирующий репрессор, расположен рядом с lac-опероном и всегда экспрессируется (конститутивно). Если в ростовой среде отсутствует лактоза, репрессор очень плотно связывается с короткой последовательностью ДНК сразу после промотора в начале lacZ, называемой оператором lac. Связывание репрессора с оператором мешает связыванию РНКП с промотором, и поэтому мРНК, кодирующая LacZ и LacY, создается только на очень низких уровнях. Однако, когда клетки растут в присутствии лактозы, метаболит лактозы, называемый аллолактозой, производимый из лактозы продуктом гена lacZ, связывается с репрессором, вызывая аллостерический сдвиг. Измененный таким образом репрессор не может связываться с оператором, позволяя RNAP транскрибировать гены lac и тем самым приводя к более высоким уровням кодируемых белков.
Второй механизм контроля представляет собой ответ на глюкозу, в котором используется гомодимер протеина-активатора катаболита (CAP) для значительного увеличения продукции β-галактозидазы в отсутствие глюкозы. Циклический аденозинмонофосфат (цАМФ) представляет собой сигнальную молекулу, распространенность которой обратно пропорциональна уровню глюкозы. Он связывается с CAP, что, в свою очередь, позволяет CAP связываться с сайтом связывания CAP (последовательность ДНК длиной 16 п.н. перед промотором слева на диаграмме ниже, примерно на 60 п.н. выше сайта начала транскрипции), что помогает РНКП связывается с ДНК. В отсутствие глюкозы концентрация цАМФ высока, и связывание ЦАП-цАМФ с ДНК значительно увеличивает производство β-галактозидазы, позволяя клетке гидролизовать лактозу и высвобождать галактозу и глюкозу.
Недавно было показано, что исключение индуктора блокирует экспрессию lac-оперона при наличии глюкозы. Глюкоза транспортируется в клетку с помощью PEP-зависимой фосфотрансферазной системы. Фосфатная группа фосфоенолпирувата переносится через каскад фосфорилирования, состоящий из общих белков PTS (фосфотрансферазной системы) HPr и EIA и глюкозоспецифических белков PTS EIIA и EIIB, цитоплазматического домена переносчика глюкозы EII. Транспорт глюкозы сопровождается ее фосфорилированием с помощью EIIB, отводя фосфатную группу от других белков PTS, включая EIIA. Нефосфорилированная форма EIIA связывается с lac-пермеазой и предотвращает попадание лактозы в клетку. Следовательно, если присутствуют и глюкоза, и лактоза, транспорт глюкозы блокирует транспорт индуктора lac-оперона.
 Тетрамерный LacI связывает две операторные последовательности и вызывает образование петель ДНК. Каждая из двух димерных функциональных субъединиц LacI (красный + синий и зеленый + оранжевый) связывает последовательность оператора ДНК (помечена). Эти две функциональные субъединицы связаны в области тетрамеризации (помечены); таким образом, тетрамерный LacI связывает две операторные последовательности. Это позволяет тетрамерному LacI вызывать образование петель ДНК.
Тетрамерный LacI связывает две операторные последовательности и вызывает образование петель ДНК. Каждая из двух димерных функциональных субъединиц LacI (красный + синий и зеленый + оранжевый) связывает последовательность оператора ДНК (помечена). Эти две функциональные субъединицы связаны в области тетрамеризации (помечены); таким образом, тетрамерный LacI связывает две операторные последовательности. Это позволяет тетрамерному LacI вызывать образование петель ДНК. lac-репрессор представляет собой четырехкомпонентный белок, тетрамер, с идентичными субъединицами. Каждая субъединица содержит мотив спираль-поворот-спираль (HTH), способный связываться с ДНК. Сайт оператора, где связывается репрессор, представляет собой последовательность ДНК с инвертированной симметрией повтора. Два полусайта ДНК оператора вместе связываются с двумя субъединицами репрессора. Хотя две другие субъединицы репрессора ничего не делают в этой модели, это свойство не понималось в течение многих лет.
В конце концов было обнаружено, что два дополнительных оператора участвуют в регуляции lac. Один (O 3) расположен примерно на -90 п.н. выше O 1 в конце гена lacI, а другой (O 2) примерно на + 410 п.н. ниже O 1 в ранней части lacZ. Эти два сайта не были обнаружены в ранних работах, потому что они имеют повторяющиеся функции, а отдельные мутации не сильно влияют на репрессию. Единичные мутации либо O 2, либо O 3 имеют только 2-3-кратный эффект. Однако их важность демонстрируется тем фактом, что двойной мутант, дефектный как по O 2, так и по O 3, резко депрессируется (примерно в 70 раз).
В текущей модели lac-репрессор одновременно связан как с основным оператором O 1, так и с O 2 или O 3. Промежуточная ДНК выходит из комплекса. Избыточный характер двух второстепенных операторов предполагает, что важен не конкретный зацикленный комплекс. Одна идея состоит в том, что система работает через модем; если связанный репрессор на мгновение освобождается от O 1, привязка к второстепенному оператору удерживает его поблизости, так что он может быстро восстановить связь. Это увеличивает сродство репрессора к O 1.
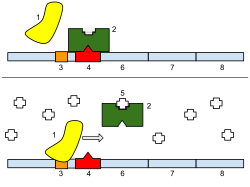 1: РНК-полимераза, 2: Репрессор, 3: Промотор, 4: Оператор, 5: Лактоза, 6: lacZ, 7: lacY, 8: lacA. Наверх : Ген практически выключен. Аллолактозы, ингибирующей lac-репрессор, не существует, поэтому репрессор плотно связывается с оператором, что препятствует связыванию РНК-полимеразы с промотором, что приводит к отсутствию транскриптов мРНК laczya. Внизу : ген включен. Аллолактоза ингибирует репрессор, позволяя РНК-полимеразе связываться с промотором и экспрессировать гены, что приводит к продукции LacZYA. В конце концов, ферменты переваривают всю лактозу до тех пор, пока не останется аллолактоза, способная связываться с репрессором. Затем репрессор свяжется с оператором, останавливая транскрипцию генов LacZYA.
1: РНК-полимераза, 2: Репрессор, 3: Промотор, 4: Оператор, 5: Лактоза, 6: lacZ, 7: lacY, 8: lacA. Наверх : Ген практически выключен. Аллолактозы, ингибирующей lac-репрессор, не существует, поэтому репрессор плотно связывается с оператором, что препятствует связыванию РНК-полимеразы с промотором, что приводит к отсутствию транскриптов мРНК laczya. Внизу : ген включен. Аллолактоза ингибирует репрессор, позволяя РНК-полимеразе связываться с промотором и экспрессировать гены, что приводит к продукции LacZYA. В конце концов, ферменты переваривают всю лактозу до тех пор, пока не останется аллолактоза, способная связываться с репрессором. Затем репрессор свяжется с оператором, останавливая транскрипцию генов LacZYA. Репрессор представляет собой аллостерический белок, то есть он может принимать одну из двух слегка отличающихся форм, которые находятся в равновесии с друг друга. В одной форме репрессор будет связываться с ДНК оператора с высокой специфичностью, а в другой форме он потерял свою специфичность. Согласно классической модели индукции, связывание индуктора, аллолактозы или IPTG, с репрессором влияет на распределение репрессора между двумя формами. Таким образом, репрессор со связанным индуктором стабилизируется в конформации, не связывающейся с ДНК. Однако эта простая модель не может быть исчерпывающей, потому что репрессор довольно стабильно связан с ДНК, однако он быстро высвобождается при добавлении индуктора. Следовательно, кажется очевидным, что индуктор также может связываться с репрессором, когда репрессор уже связан с ДНК. До сих пор не совсем известно, каков точный механизм связывания.
Неспецифическое связывание репрессора с ДНК играет решающую роль в репрессии и индукции Лак-оперона. Сайт специфического связывания для белка-репрессора Lac является оператором. Неспецифическое взаимодействие опосредуется, главным образом, заряд-зарядовыми взаимодействиями, в то время как связывание с оператором усиливается гидрофобными взаимодействиями. Кроме того, существует множество неспецифических последовательностей ДНК, с которыми репрессор может связываться. По сути, любая последовательность, не являющаяся оператором, считается неспецифической. Исследования показали, что без наличия неспецифического связывания индукция (или нерепрессия) Lac-оперона не могла бы происходить даже при насыщенных уровнях индуктора. Было продемонстрировано, что без неспецифического связывания базальный уровень индукции в десять тысяч раз меньше, чем обычно. Это связано с тем, что неспецифическая ДНК действует как своего рода «сток» для белков-репрессоров, отвлекая их от оператора. Неспецифические последовательности уменьшают количество доступного репрессора в клетке. Это, в свою очередь, снижает количество индуктора, необходимого для разуплотнения системы.
 IPTG
IPTG 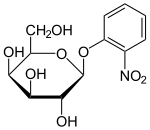 ONPG
ONPG  X-gal
X-gal  аллолактоза
аллолактоза Ряд производных или аналогов лактозы описаны полезные для работы с lac-опероном. Эти соединения в основном представляют собой замещенные галактозиды, в которых глюкозный фрагмент лактозы заменен другой химической группой.
Используемый экспериментальный микроорганизм François Jacob и Jacques Monod был обычной лабораторной бактерией, E. coli, но многие из основных регуляторных концепций, которые были открыты Jacob и Monod, являются фундаментальными для клеточного регуляция у всех организмов. Ключевая идея состоит в том, что белки не синтезируются, когда они не нужны - E. coli сохраняет клеточные ресурсы и энергию, не производя три белка Lac, когда нет необходимости метаболизировать лактозу, например, когда доступны другие сахара, такие как глюкоза. В следующем разделе обсуждается, как E. coli контролирует определенные гены в ответ на метаболические потребности.
Во время Второй мировой войны компания Monod тестировала эффекты сочетания сахаров в качестве источников питательных веществ для E. coli и B. subtilis. Моно продолжал аналогичные исследования, которые были проведены другими учеными с бактериями и дрожжами. Он обнаружил, что бактерии, выращенные с двумя разными сахарами, часто демонстрируют две фазы роста. Например, если были предоставлены и глюкоза, и лактоза, сначала метаболизировалась глюкоза (фаза роста I, см. Рис. 2), а затем лактоза (фаза роста II). Лактоза не метаболизировалась в течение первой части диауксической кривой роста, поскольку β-галактозидаза не образовывалась, когда в среде присутствовали и глюкоза, и лактоза. Моно назвал это явление диаукси.
 . Рисунок 2: «Двухфазная» кривая роста Моно
. Рисунок 2: «Двухфазная» кривая роста Моно Затем Моно сосредоточил свое внимание на индукции образования β-галактозидазы, которая происходила, когда лактоза была единственным сахаром в культуральная среда.
Концептуальный прорыв Jacob и Monod заключался в распознавании различия между регуляторными веществами и сайтами, в которых они действуют, изменяя экспрессию генов. Бывший солдат, Джейкоб использовал аналогию с бомбардировщиком, который выпускал смертельный груз после получения специальной радиопередачи или сигнала. Для работающей системы требуются как наземный передатчик, так и приемник в самолете. Теперь предположим, что обычный передатчик сломан. Эту систему можно заставить работать, установив второй функциональный передатчик. В отличие от этого, по его словам, рассмотрим бомбардировщик с неисправной ствольной коробкой. Поведение этого бомбардировщика не может быть изменено введением второго исправного самолета.
Для анализа регуляторных мутантов оперона lac Джейкоб разработал систему, с помощью которой вторая копия генов lac (lacI с его промотором и lacZYA с промотором и оператором) могла быть введена в одну клетку. Культуру таких бактерий, которые являются диплоидными по генам lac, но в остальном нормальными, затем проверяют на регуляторный фенотип. В частности, определяется, образуются ли LacZ и LacY даже в отсутствие IPTG (из-за того, что репрессор лактозы, продуцируемый мутантным геном, нефункционален). Этот эксперимент, в котором гены или кластеры генов тестируются попарно, называется тестом комплементации.

. Этот тест проиллюстрирован на рисунке (lacA для простоты опущен). Сначала показаны определенные гаплоидные состояния (т. Е. Клетка несет только одну копию генов lac). Панель (а) показывает репрессию, (b) показывает индукцию IPTG, и (c) и (d) показывают влияние мутации на ген lacI или на оператора, соответственно. На панели (е) показан тест комплементации для репрессора. Если одна копия генов lac несет мутацию в lacI, а вторая копия является диким типом для lacI, результирующий фенотип является нормальным, но lacZ экспрессируется при воздействии индуктора IPTG. Говорят, что мутации, затрагивающие репрессор, рецессивны по отношению к дикому типу (и этот дикий тип является доминирующим), и это объясняется тем фактом, что репрессор представляет собой небольшой белок, который может диффундировать в клетке. Копия оперона lac, смежная с дефектным геном lacI, эффективно блокируется белком, продуцируемым из второй копии lacI.
Если тот же эксперимент проводится с использованием мутации оператора, получается другой результат (панель (f)). Фенотип клетки, несущей один мутантный и один операторный сайт дикого типа, заключается в том, что LacZ и LacY продуцируются даже в отсутствие индуктора IPTG; поскольку поврежденный сайт оператора не позволяет связывать репрессор для ингибирования транскрипции структурных генов. Операторная мутация является доминирующей. Когда сайт оператора, с которым должен связываться репрессор, поврежден мутацией, присутствие второго функционального сайта в той же клетке не влияет на экспрессию генов, контролируемых мутантным сайтом.
Более сложная версия этого эксперимента использует помеченные опероны, чтобы различать две копии генов lac и показать, что нерегулируемый структурный ген (ы) является (являются) одним (ами) рядом с мутантным оператором (панель (g). Например, предположим, что одна копия отмечена мутацией, инактивирующей lacZ, так что она может продуцировать только белок LacY, тогда как вторая копия несет мутацию, затрагивающую lacY, и может продуцировать только LacZ. В этой версии только копия lac-оперона, смежная с мутантным оператором, экспрессируется без IPTG.Мы говорим, что операторная мутация является цис-доминантной, она доминантна для дикого типа, но затрагивает только копию оперона, которая непосредственно примыкает к нему.
Это объяснение вводит в заблуждение в важном смысле, потому что оно исходит из описания эксперимента, а затем объясняет результаты в терминах модели. Но на самом деле часто бывает так, что модель идет первой, и эксперимент разработан специально для проверки t он модель. Джейкоб и Моно сначала предположили, что в ДНК должен быть участок со свойствами оператора, а затем разработали свои тесты дополнения, чтобы показать это.
Преобладание мутантов-операторов также предполагает процедуру их особого отбора. Если регуляторные мутанты выбираются из культуры дикого типа с использованием фенил-Gal, как описано выше, операторные мутации редки по сравнению с мутантами-репрессорами, поскольку размер мишени очень мал. Но если вместо этого мы начнем со штамма, который несет две копии всей области lac (то есть диплоид для lac), репрессорные мутации (которые все еще происходят) не восстанавливаются, потому что комплементация вторым, геном lacI дикого типа дает фенотип. Напротив, мутация одной копии оператора дает мутантный фенотип, потому что он доминирует над второй копией дикого типа.
Объяснение диауксии зависело от характеристики дополнительных мутаций, влияющих на гены lac, помимо тех, которые объясняются классической моделью. Впоследствии были идентифицированы два других гена, cya и crp, которые картированы далеко от lac и которые при мутации приводят к снижению уровня экспрессии в присутствии IPTG и даже в штаммах бактерий, лишенных репрессора или оператора. Открытие цАМФ в E. coli привело к демонстрации того, что мутанты, дефектные по гену cya, но не по гену crp, могут быть восстановлены до полной активности путем добавления цАМФ в среду.
Ген cya кодирует аденилатциклазу, которая продуцирует цАМФ. У мутанта cya отсутствие цАМФ делает экспрессию генов lacZYA более чем в десять раз ниже, чем обычно. Добавление цАМФ корректирует низкую экспрессию Lac, характерную для мутантов cya. Второй ген, crp, кодирует белок, называемый белком-активатором катаболита (CAP) или рецепторным белком цАМФ (CRP).
Однако ферменты метаболизма лактозы образуются в в небольших количествах в присутствии как глюкозы, так и лактозы (иногда называемой протекающей экспрессией) из-за того, что репрессор LacI быстро связывается / диссоциирует с ДНК, а не плотно с ней связывается, что может дать время РНКП для связывания и транскрипции мРНК lacZYA. Утечка экспрессии необходима для того, чтобы обеспечить метаболизм некоторого количества лактозы после того, как источник глюкозы израсходован, но до того, как экспрессия lac полностью активируется.
Вкратце:
Задержка между фазами роста отражает время, необходимое для производства достаточных количеств ферментов, метаболизирующих лактозу. Во-первых, регуляторный белок CAP должен собраться на промоторе lac, что приведет к увеличению продукции lac мРНК. Более доступные копии lac мРНК приводят к продукции (см. перевод ) значительно большего количества копий LacZ (β-галактозидаза, для метаболизма лактозы) и LacY (пермеаза лактозы для транспортировки лактозы в клетку). После задержки, необходимой для повышения уровня ферментов, метаболизирующих лактозу, бактерии вступают в новую быструю фазу клеточного роста.
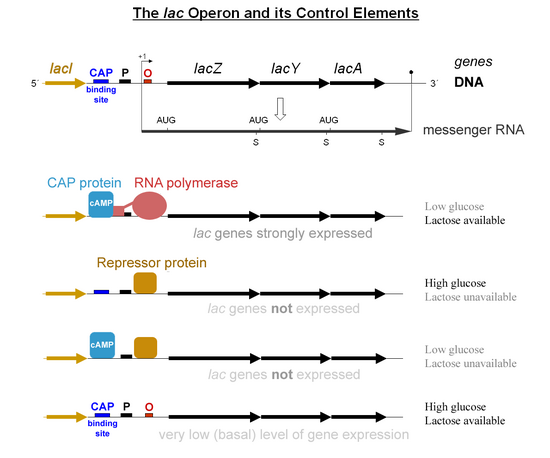 lac operon подробно
lac operon подробно Две головоломки репрессии катаболита связаны на то, как уровни цАМФ связаны с наличием глюкозы, и, во-вторых, почему клетки должны беспокоить. После расщепления лактозы фактически образуется глюкоза и галактоза (легко превращаются в глюкозу). С точки зрения метаболизма, лактоза является таким же хорошим источником углерода и энергии, как и глюкоза. Уровень цАМФ связан не с внутриклеточной концентрацией глюкозы, а со скоростью транспорта глюкозы, которая влияет на активность аденилатциклазы. (Кроме того, транспорт глюкозы также ведет к прямому ингибированию пермеазы лактозы.) О том, почему кишечная палочка работает таким образом, можно только догадываться. Все кишечные бактерии ферментируют глюкозу, что говорит о том, что они часто с ней сталкиваются. Возможно, что небольшая разница в эффективности транспорта или метаболизма глюкозы по сравнению с лактозой позволяет клеткам таким образом регулировать lac-оперон.
lac ген и его производные можно использовать в качестве репортерного гена в ряде методов бактериальной селекции, таких как двухгибридный анализ, в котором успешное связывание транскрипционного активатор для конкретной промоторной последовательности необходимо определить. В чашках LB, содержащих X-gal, изменение цвета с белых колоний на оттенок синего соответствует примерно 20–100 единицам β-галактозидазы, тогда как тетразолий лактоза и среды для лактозы MacConkey имеют диапазон 100–1000 единиц, являясь наиболее чувствительными в верхней и нижней частях этого диапазона соответственно. Поскольку лактозные и тетразолиевые лактозные среды MacConkey зависят от продуктов распада лактозы, они требуют наличия генов lacZ и lacY. Таким образом, многие методы слияния лака, которые включают только ген lacZ, подходят для планшетов с X-gal или ONPG жидких бульонов.