 | |
| Имена | |
|---|---|
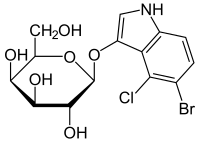
| Название IUPAC 5-бром-4-хлор-3-индолил-β-D-галактопиранозид | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.027.855 |
| MeSH | X-gal |
| PubChem CID | |
| UNII | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C14H15BrClNO 6 |
| Молярная масса | 408,629 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
X-gal (также сокращенно BCIG для 5-бром-4-хлор-3-индолил-β- D-галактопиранозид) представляет собой органическое соединение, состоящее из галактозы, связанной с замещенным индолом. Это соединение было синтезировано Джеромом Хорвицем и сотрудниками в Детройте, штат Мичиган, в 1964 году. Официальное химическое название часто сокращается до менее точных, но также менее громоздких фраз, таких как бромхлориндоксилгалактозид. X из индоксила может быть источником X в сокращении X-gal. X-gal часто используется в молекулярной биологии для проверки наличия фермента, β-галактозидазы. Он также используется для определения активности этого фермента в гистохимии и бактериологии. X-gal является одним из многих индоксилгликозидов и сложных эфиров, которые дают нерастворимые синие соединения, подобные красителю индиго, в результате гидролиза, катализируемого ферментами.
X-gal является аналогом лактозы, и поэтому может быть гидролизован ферментом β-галактозидаза, который расщепляет β- гликозидную связь в D-лактозе. X-gal при расщеплении β-галактозидазой дает галактозу и 5-бром-4-хлор-3-гидроксииндол - 1 . Последний затем самопроизвольно димеризуется и окисляется до 5,5'-дибром-4,4'-дихлор- индиго - 2, сильно синего продукта, который нерастворим. Сама X-gal бесцветна, поэтому наличие продукта синего цвета можно использовать в качестве теста на наличие активной β-галактозидазы. Это также позволяет использовать бактериальную β-галактозидазу (так называемую lacZ) в качестве репортера в различных приложениях.
 .
.
In при клонировании гена, X-gal используется в качестве визуального индикатора того, экспрессирует ли клетка функциональный фермент β-галактозидаза в методике, называемой сине-белый скрининг. Этот метод скрининга - удобный способ отличить успешный продукт клонирования от других неудачных.
Метод скрининга «синий / белый» основан на принципе α-комплементации гена β-галактозидазы, где фрагмент гена lacZ (lacZα) в плазмиде может дополнять другой мутант ген lacZ (lacZΔM15) в клетке. Оба гена сами по себе продуцируют нефункциональные пептиды, однако при совместной экспрессии, например, когда плазмида, содержащая lacZα, трансформируется в клетки lacZΔM15, они образуют функциональную β-галактозидазу. Присутствие активной β-галактозидазы может быть обнаружено при выращивании клеток в чашках, содержащих X-gal, продукт синего цвета, осажденный внутри клеток, дает характерные синие колонии. Однако сайт множественного клонирования, где представляющий интерес ген может быть лигирован в плазмидный вектор, находится внутри гена lacZα. Таким образом, успешное лигирование разрушает ген lacZα, следовательно, α-комплементация также нарушается, и функциональная β-галактозидаза не может образовываться, что приводит к образованию белых колоний. Затем клетки, содержащие успешно лигированную вставку, можно легко отличить по ее белой окраске от неудачных синих. Примером векторов клонирования, используемых для этого теста, являются pUC19, векторы pGem-T, и для этого также требуется использование конкретных штаммов-хозяев E. coli, таких как DH5α, который несет мутантный ген lacZΔM15. X-Gal также содержит IPTG (изопропил-β-D-1-тиогалактопиранозид). IPTG - это аналог лактозы по химической структуре. Однако IPTG не может гидролизоваться β-галактозидазой. IPTG используется в качестве индуктора, который связывается с lac-репрессором, высвобождая ДНК и обеспечивая транскрипцию. Таким образом, присутствие IPTG в чашке с агаром увеличивает синтез β-галактозидазы.
X-gal имеет ряд вариантов, которые представляют собой похожие молекулы с небольшими различиями, служащие в основном для производства другие цвета, кроме синего, в качестве сигнала.
| Краткое название | Длинное название | Цвет |
|---|---|---|
| Blue-Gal, Bluo-Gal | 5-бром-3-индолил β-D-галактопиранозид | Темно-синий |
| Rose-Gal, Salmon-Gal, Y-Gal, Red-Gal | 6-Хлор-3-индолил-β-D-галактопиранозид | Розовый |
| Фиолетовый-β-D-Gal | 5-Йод-3-индолил-β-D-галактопиранозид | Фиолетовый |
| Пурпурный глюкозид, Magenta-GLC, Magenta gal | 5-бром-6-хлор-3-индолил-β-D-глюкопиранозид | пурпурный |
| зеленый-β-D-гал | N-метилиндолил-β- D-галактопиранозид | Зеленый |
| MUG, MUGA | 4-Метилумбеллиферил β-D-галактопиранозид | Флуоресцентный (λ ex = 365, λ em = 455) |
В двухгибридном анализе β-галактозидаза может использоваться в качестве репортера для идентификации белков, которые взаимодействуют с друг друга. В этом методе библиотеки генома могут быть проверены на взаимодействие белков с использованием дрожжевой или бактериальной системы. При успешном взаимодействии между проверяемыми белками это приведет к связыванию домена активации с промотором. Если промотор связан с геном lacZ, продукция β-галактозидазы, которая приводит к образованию колоний с синим пигментом в присутствии X-gal, будет, следовательно, указывать на успешное взаимодействие между белками. Этот метод может быть ограничен скринингом библиотек размером менее примерно 10. Успешное расщепление X-gal также создает заметно неприятный запах из-за испарения индола.