| Альфа- амилаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Амилаза слюны человека: ион кальция ион виден бледным цветом хаки, ион хлорида - зеленым. PDB 1SMD Амилаза слюны человека: ион кальция ион виден бледным цветом хаки, ион хлорида - зеленым. PDB 1SMD | |||||||||
| Идентификаторы | |||||||||
| Номер EC | 3.2.1.1 | ||||||||
| Номер CAS | 9000-90-2 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| GH13 каталитический домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Циклодекстринглюканотрансфераза (ec2.4.1.19) (cgtase) Циклодекстринглюканотрансфераза (ec2.4.1.19) (cgtase) | |||||||||
| Идентификаторы | |||||||||
| Символ | Альфа-амилаза | ||||||||
| Pfam | PF00128 | ||||||||
| Pfam клан | CL0058 | ||||||||
| InterPro | IPR006047 | ||||||||
| SCOPe | 1ppi / SUPFAM | ||||||||
| суперсемейство OPM | 117 | ||||||||
| белок OPM | 1wza | ||||||||
| CAZy | GH13 | ||||||||
| CDD | cd11338 | ||||||||
| |||||||||
| С-концевой бета-листовой домен альфа-амилазы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
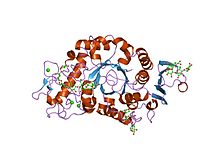 Кристаллическая структура неактивного мутанта изофермента 1 альфа-амилазы ячменя (amy1) d180a в комплексе с мальтогептаозой Кристаллическая структура неактивного мутанта изофермента 1 альфа-амилазы ячменя (amy1) d180a в комплексе с мальтогептаозой | |||||||||
| Идентификаторы | |||||||||
| Символ | Альфа-амил_C2 | ||||||||
| Pfam | PF07821 | ||||||||
| InterPro | IPR012850 | ||||||||
| |||||||||
| Альфа-амилаза, С-концевой бета-домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
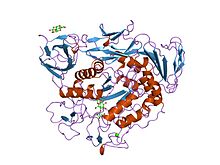 комплекс мальтотриозы предварительно кондиционированного мутанта циклодекстрингликозилтрансферазы комплекс мальтотриозы предварительно кондиционированного мутанта циклодекстрингликозилтрансферазы | |||||||||
| Идентификаторы | |||||||||
| Символ | Альфа-амилаза_C | ||||||||
| Pfam | PF02806 | ||||||||
| Pfam клан | CL0369 | ||||||||
| InterPro | IPR006048 | ||||||||
| SCOPe | 1ppi / SUPFAM | ||||||||
| |||||||||
Альфа-амилаза, (α-амилаза) представляет собой фермент EC 3.2.1.1, который гидролизует альфа-связи больших альфа-связанных полисахаридов, таких как крахмал и гликоген, с получением глюкозы и мальтоза. Это основная форма амилазы, обнаруживаемая у людей и других млекопитающих. Он также присутствует в семенах, содержащих крахмал в качестве запаса пищи, и выделяется многими грибами. Он является членом семейства гликозидгидролаз 13.
Хотя амилаза обнаруживается во многих тканях, она наиболее заметны в панкреатическом соке и слюне, каждая из которых имеет свою собственную изоформу человеческой α-амилазы. Они по-разному ведут себя при изоэлектрическом фокусировании, а также могут быть разделены при тестировании с использованием специфических моноклональных антител. У человека все изоформы амилазы связаны с хромосомой 1p 21 (см. AMY1A ).
Амилаза содержится в слюне и расщепляет крахмал на мальтозу и декстрин. Эта форма амилазы также называется «птиалин», что было названо шведским химиком Йенсом Якобом Берцелиусом. Название происходит от греческого слова πτυω (я плюю), потому что это вещество было получено из слюны. Он расщепляет большие нерастворимые молекулы крахмала на растворимые крахмалы (амилодекстрин и), производя последовательно более мелкие крахмалы и, в конечном итоге, мальтозу. Птиалин действует на линейные α (1,4) гликозидные связи, но для гидролиза соединения требуется фермент, который действует на разветвленные продукты. Амилаза слюны инактивируется в желудке с помощью желудочной кислоты. В желудочном соке, доведенном до pH 3,3, птиалин полностью инактивировался за 20 минут при 37 ° C. Напротив, 50% активности амилазы сохранялось после 150 минут воздействия желудочного сока при pH 4,3. И крахмал, субстрат для птиалина, и продукт (короткие цепи глюкозы) способны частично защищать его от инактивации желудочной кислотой. Птиалин, добавленный в буфер с pH 3,0, полностью инактивируется за 120 минут; однако добавление крахмала на уровне 0,1% привело к сохранению 10% активности, а аналогичное добавление крахмала до уровня 1,0% привело к примерно 40% активности, остающейся через 120 минут.
Ген амилазы претерпел дупликацию в процессе эволюции, и исследования гибридизации ДНК показывают, что у многих людей есть несколько тандемных повторов гена. Число копий гена коррелирует с уровнями амилазы в слюне, измеренными с помощью анализа белковыми блоттингами с использованием антител к амилазе человека. Число копий гена связано с очевидным эволюционным воздействием диет с высоким содержанием крахмала. Например, у японца было 14 копий гена амилазы (один аллель с 10 копиями, а второй аллель с четырьмя копиями). Японская диета традиционно содержала большое количество рисового крахмала. Напротив, у индивида биака было шесть копий (по три копии на каждый аллель). Биака - охотники-собиратели тропических лесов, которые традиционно придерживались диеты с низким содержанием крахмала. Перри и его коллеги предположили, что увеличенное количество копий гена амилазы слюны могло повысить выживаемость, совпадающую с переходом на крахмалистую диету во время эволюции человека.
Панкреатическая α-амилаза случайным образом расщепляет α (1-4) гликозидные связи из амилозы с образованием декстрина, мальтоза или мальтотриоза. Он использует механизм двойного смещения с сохранением аномерной конфигурации. У людей амилаза слюны произошла из ее копии.
Тест на амилазу легче выполнить, чем на липазу, что делает его основным тест, используемый для выявления и мониторинга панкреатита. Медицинские лаборатории обычно измеряют панкреатическую амилазу или общую амилазу. Если измерять только амилазу поджелудочной железы, увеличение не будет отмечено при паротите или другой травме слюнной железы.
Однако из-за небольшого количества, время имеет решающее значение при отборе крови для этого измерения. Кровь следует брать вскоре после приступа боли при панкреатите, в противном случае она быстро выводится почками.
α-амилаза слюны использовалась в качестве биомаркера для стресс и в качестве суррогатного маркера активности симпатической нервной системы (СНС), не требующей анализа крови.
Повышенные уровни в плазме крови человека обнаруживаются при:
Показания общей амилазы более чем в 10 раз превышают верхний предел нормы (ВГН), что указывает на панкреатит. ВГН в 5–10 раз может указывать на кишечную непроходимость или двенадцатиперстную кишку или почечную недостаточность, и ниже повышение обычно встречается при заболевании слюнных желез.
Активность α-амилазы в зерне измеряется, например, с помощью числа падения Хагберга – Пертена, теста для оценки повреждений проростков или Phadebas метод.
α-Амилаза используется в производстве этанола чтобы разбить крахмал в зернах на сбраживаемый сахар.
Первым этапом производства кукурузного сиропа с высоким содержанием фруктозы является обработка кукурузного крахмала α-амилазой с образованием более коротких цепей сахаров олигосахаридов.
α-амилаза, называемая «термамил», полученная из Bacillus licheniformis, также используется в некоторых моющих средствах, особенно в средствах для мытья посуды и моющих средств для удаления крахмала.
См. амилаза для большего количества применений семейства амилазы в целом.
α-амилаза продемонстрировала эффективность в разрушении полимикробных бактериальных биопленок путем гидролиза α (1-4) гликозидных связей внутри структурных экзополисахаридов матрикса внеклеточного полимерного вещества (EPS).
Сообщается, что молекула трис ингибирует ряд бактериальных α-амилаз, поэтому их не следует использовать в трис-буфере.
Для определения активности α-амилазы доступно несколько методов, и разные отрасли промышленности склонны полагаться на разные методы. Йодный крахмальный тест, являющийся развитием йодного теста, основан на изменении цвета, поскольку α-амилаза разлагает крахмал, и обычно используется во многих областях. Аналогичным, но производимым промышленностью тестом является тест амилазы Phadebas, который используется в качестве качественного и количественного теста во многих отраслях промышленности, таких как моющие средства, различные продукты из муки, зерна и солода, а также в судебной биологии.
α-Амилазы содержат ряд отдельных белковых доменов. каталитический домен имеет структуру , состоящую из восьмицепочечного альфа / бета-ствола, который содержит активный сайт, прерванный ~ 70- аминокислотой кальций- связывающий домен, выступающий между бета-цепью 3 и альфа-спиралью 3, и карбоксиконцевым греческим ключевым доменом бета-ствол. Некоторые альфа-амилазы содержат домен бета-листа, обычно на С-конце. Этот домен организован в виде пятицепочечного антипараллельного бета-листа. Некоторые альфа-амилазы содержат полностью бета-домен, обычно на конце C.